CN1124524A - 由可相互对折叠合的构件构成的色谱测定装置 - Google Patents
由可相互对折叠合的构件构成的色谱测定装置 Download PDFInfo
- Publication number
- CN1124524A CN1124524A CN94192256A CN94192256A CN1124524A CN 1124524 A CN1124524 A CN 1124524A CN 94192256 A CN94192256 A CN 94192256A CN 94192256 A CN94192256 A CN 94192256A CN 1124524 A CN1124524 A CN 1124524A
- Authority
- CN
- China
- Prior art keywords
- doubling
- sample
- analyte
- chromatographic media
- specificity combination
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/505—Containers for the purpose of retaining a material to be analysed, e.g. test tubes flexible containers not provided for above
- B01L3/5055—Hinged, e.g. opposable surfaces
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5023—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures with a sample being transported to, and subsequently stored in an absorbent for analysis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/90—Plate chromatography, e.g. thin layer or paper chromatography
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/90—Plate chromatography, e.g. thin layer or paper chromatography
- G01N30/91—Application of the sample
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/5302—Apparatus specially adapted for immunological test procedures
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
- G01N33/54386—Analytical elements
- G01N33/54387—Immunochromatographic test strips
- G01N33/54388—Immunochromatographic test strips based on lateral flow
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/558—Immunoassay; Biospecific binding assay; Materials therefor using diffusion or migration of antigen or antibody
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0809—Geometry, shape and general structure rectangular shaped
- B01L2300/0825—Test strips
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/04—Moving fluids with specific forces or mechanical means
- B01L2400/0403—Moving fluids with specific forces or mechanical means specific forces
- B01L2400/0406—Moving fluids with specific forces or mechanical means specific forces capillary forces
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/26—Conditioning of the fluid carrier; Flow patterns
- G01N30/28—Control of physical parameters of the fluid carrier
- G01N30/30—Control of physical parameters of the fluid carrier of temperature
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S435/00—Chemistry: molecular biology and microbiology
- Y10S435/805—Test papers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S435/00—Chemistry: molecular biology and microbiology
- Y10S435/81—Packaged device or kit
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S435/00—Chemistry: molecular biology and microbiology
- Y10S435/97—Test strip or test slide
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S435/00—Chemistry: molecular biology and microbiology
- Y10S435/975—Kit
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S436/00—Chemistry: analytical and immunological testing
- Y10S436/805—Optical property
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S436/00—Chemistry: analytical and immunological testing
- Y10S436/807—Apparatus included in process claim, e.g. physical support structures
- Y10S436/81—Tube, bottle, or dipstick
Abstract
一种与免疫测定一起使用的色谱测定装置。该装置包括(1)一第一可对折构件(11),它有一个能够接收要测定的试样的试样制备区,和(2)一第二可对折构件,它有一色谱介质(14);第一和第二可对折构件可叠合起来,使试样制备区(13)将要测试的试样施加到色谱介质上。用一种肉眼可检测的标记物检测分析物。这种装置可以组装在试验箱,同时也公开了应用这种装置的测定方法,既包括夹心法也包括竞争法。
Description
本发明涉及用于测定试样的特性的测试条、整体构成的壳体和内装有试验条和壳体的箱,以及利用这些试验条和壳体测定试样特性的一些方法。
有许多用于检测和/或测定分析物,尤其是具有生物问题的分析物的分析系统,其中包括一些色谱测定系统。用这种系统经常测定的分析物中有:
(1)激素,如人类绒毛膜促性腺激素(human chorionicgonadotropin)(HCG),它通常是作为人类怀孕的一种标志来测定的;
(2)抗原,尤其是对细菌的、病毒的和原生动物病原(protozoan pathogens)具有特异性的抗原,如链球菌(Streplococcus),肝炎病毒(hepetitis virus),和贾第鞭毛虫(Grardia);
(3)抗体,尤其是由于由病原体感染引发的抗体,如针对幽门螺杆菌(Helicobacter pylori)细菌的抗体,和针对人类免疫缺陷病毒(HTV)的抗体;
(4)其它蛋白质,如血红蛋白(hemoglobin),它通常用于测定粪便隐血,是肠胃紊乱如结肠癌的一种早期指示。
(5)酶,如天冬氨酸氨基转移酶(aspartateaminolransferase),乳酸盐脱氢酶(lactate dehydrogenase),碱性磷酸盐(alkaline phosphatase),和谷氨酸脱氢酶(glutamatedehydrogenase),通常作为生理功能和组织损伤的指示来测定;
(6)药物,既包括医疗用药品,如抗生素,安定剂(tranquilizers)和抗惊厥剂(anticon vulsants),也包括非法毒品,如可卡因,海洛因和马力球哪(mariguana);
(7)环境污染剂,如杀虫剂(pesticides)和芳香族碳氢化合物(aromatic hydrocarbons);和
(8)维生素。
医生和医务技术人员经常使用这种色谱系统用以对各种病况和紊乱进行快速的现场诊断和医疗监测。这种色谱系统也越来越多地由病人自己在家中使用,来监测这些病况和紊乱。
在这种系统中最重要的系统是“薄层”系统,其中,一种溶剂(移动相)在一个薄而平的吸收剂介质上移动。
在能够用这种薄层系统实施的测试中最重要的试验是免疫测定,这种免疫测定依赖于抗原或半抗原与相应的抗体之间的特异性相互作用。人们知道用免疫测定法作为检测医疗上重要的分子的存在和/或数量的手段已经有一定的时间了。早在1956年,J.M.Singer就报导了利用一种免疫基的胶乳粘合试验来检测一种与类风湿关节炎有关联的因素(参见Singer等人的文章,美国医疗杂志22:888-892页,1956年)。
在与免疫测定一起使用的色谱技术中有一种称为免疫色谱法的方法。一般地,这种技术采用一种暴露试剂(disclosingreagent)或颗粒,这种暴露试剂或颗粒已连接到一个针对要测定的分子的抗体上,形成一个结合物。这个结合物然后与一个试样混合,如果试样中存在要测定的分子,与暴露试剂直接的抗体就结合到要测定的分子上,由此指示出要测定的分子是存在的。这种暴露试剂或颗粒或以用颜色、磁性、放射性、与另一个分子的特异性反应、或另一种物理的或化学的特性加以识别。采用的特异性反应随着要测定的分子和要测试的试样的性质的不同而不同。
免疫色谱测定法分成两个主要的类别:即“夹心法”和“竞争法”,这是按照要检测的抗原-抗体复合物的性质和产生这种复合物所要求的反应的顺序来分类的。要检测的抗原本身可以是一种抗体,如在血清学测定中对幽门螺杆菌有特异性的抗体。在这种情况下,要检测的抗体可以被结合到一种特异性抗原上。另一种方式是,要检测的抗原可以利用一种结合到针对要检测的分析物的第一抗体上的加标记的第二抗体间接地得到检测。
一般地,夹心免疫色谱法要求将可能含有要测定的分析物的试样与分析物的抗体相混合。这些抗体是活动的,并且典型地,被连接到一种标记物或一种暴露试剂上,例如染色胶乳(dyedlatex)、胶肪金属胶(colloidal metal sol),或者一种放射性同位素。然后将这种混合物施加到一个色谱介质上,该色谱介质含有一个针对要研究的分析物的固定抗体的带区或区域。这种色谱介质通常是一种类似于一个量尺的小片条形状。当要测定的分子和加标记的抗体的复合物到达色谱介质上的固定抗体区域时,就发生结合,而被结合的加标记的抗体被设定在该区域中,这就指示出存在着要测定的分子。这种技术可以用于获得定量的或半定量的结果。
美国专利文件第4,168,146号(Grubb等人)和第4,366,241号(Tom等人)中描述了一些在试验条上进行的夹心法免疫测定的例子,此处引用这两篇专利文献作为参考。
在竞争法免疫测定中,标记物的典型情况是一种加标记的分析物或分析物的模拟物,它为了与一个抗体结合而与试样中任何不加标记的分析物竞争。典型的情况是采用竞争法免疫测定来检测诸如半抗原这样的分析物,其中,每个半抗原都是单克隆的并只能够结合一个抗体分子。在美国专利文件第4,235,601(Deutsch等人),第4,442,204(Liotta)和第5,208,535(Buechler等人中公开了一些竞争法免疫测定装置的例子。这些文献在此引用作为参考。
目前存在的采用试验条的色谱技术是有用的,但它们有一些缺陷。许多试样,如粪便试样,含有可能会堵塞色谱介质的孔的颗粒物质,而大大地阻碍了免疫色谱过程。其它一些试样,如血液,含有细胞和有色组分,使得难以读出试验结果。即使试样不产生干扰,也常常难以用现有的色谱试验装置将试样施加到色谱介质上,以使试样前沿在色谱介质中均匀地移动,保证试样到达在其中要以一种均匀的直线的方式发生结合的区域中。
由于要测定的试样特性的不同或要实施的测定的不同性质,现有试验条也存在一些其它问题。这种装置不实用于实施洗涤步骤,在为了提高敏感性,减少本底,常常要求有这种洗涤步骤。而且在装置内难以进行预培养步骤,而且在许多情况下是不可能的。
此外,需要一种能够实施范围宽广的分离的免疫色谱测定装置,例如从牛奶中分离脂肪,或分离有机化学物,如从甲苯中分离苯。
试样的制备和废物的产生是现有的免疫色谱法装置和技术所面临的其它问题。由污染的血液或血液组分所扩散的疾病如艾滋病和肝炎的不断传播已经使这些问题更加严重。将一个试样(如粪便)和一个取样器(如一个喉咙拭片)直接施加到色谱介质上几乎是不可能的。在试样能够加到色谱介质上之前通常需要进行一些提取和预处理反应。典型地,这些反应是由实施试验的医生或技术人员在几个小的容器,如试管或迈克福志(microfuge)管中进行的,这需要使用传输装置,如吸液管。这样,所有这些装置都受到污染而必须用特殊措施进行处理,以便那些可能无意地接触到这些废物的工人或人员不会被感染。
医务人员或技术人员所用的现有色谱装置的另一个局限性是它们不能实施双向的或两维的色谱法。很久以来人们就知道这些技术是很有力的分析工具,但它们相对于简单的单向色谱法而言则很复杂,使得它们很难用于医生的办公室或医疗实验室中的试验条装置上。
因此,需要有一种能够进行宽广范围的色谱测定的先进测定装置。这种装置应该能够处理各种类型的免疫测定,包括夹心法和竞争法,以及应用色谱法的其它类型的测定。这种装置应该能够直接接收一种可能被污染的试样或一种试样制备装置,以便消除对提取容器和传输装置的需要。这样的一种装置,最好的是为一种试验条的形式,也应该能够对有色的试样或含有颗粒的试样实施免疫色谱测定,而不会发生干扰,并且能够将试样均匀地传送到色谱介质上,以改善试验的准确度和精度。此外,这种改进的试验条应该能够在医疗实验室或医生办公室中使用时实施双向或两维的色谱法。
我们已经开发了一种满足于这些需要的测定装置,这种测定装置改善了对生物研究的分析物所进行的测定,同时简化了测定的实施过程并且避免了污染。这种装置能够实施所有类型的免疫测定,包括夹心法免疫测定、竞争法免疫测定,和采用这些原理的各种组合的测定。这种装置能够实施其中要检测的抗原本身是一种抗体,如幽门螺杆菌抗体的血清测定。这种装置能够实施这样的测定,其中要检测的抗原是通过用一种结合到针对分析物的第一抗体上的加标记的第二抗体间接检测的。
一种按照本发明的测定装置利用压力将液体从一个可对折构件传输到另一个可对折构件上,而且也驱使液体流过色谱介质。该压力不仅加快了装置的工作速度,而且也能够实施附加的步骤,例如用于在单一的装置中除去干扰颗粒组分的提取步骤。压力是通过用位于每个可对折构件上的接合件如互锁件将可对折的构件保持在一起而产生的。更好的情况是施加一个预定压力,以保证测定过程的每个步骤的最佳地实施。
此外,这种装置能够实施其它类型的特异性结合测定,例如:(1)基于特异性结合蛋白质,如植物凝血素、激素受体,或它们的特异性配体的病毒受体的亲合力的测定;(2)基于其相应的底物或抑制剂的酶的亲合力的测定;或(3)基于按照Watson-Crick基础配对方案的一个核酸(DNA或RNA)节(Segment)对一个互补核酸节的亲合力的测定。
这种装置包括:
(1)至少两个基本上平面的可对折构件,其中的一个基本上平面的可对折构件在其表面上有一个色谱介质;和
(2)用于将可对折构件相互对折叠合并在其上施加压力的部件,该压力大到足以能沿着一个大致垂直于可对折构件的方向将液体从一个可对折构件传输到另一个可对折构件上,从而将试样施加到色谱介质上,以检测和/或测定其上的分析物。
按照本发明的装置也可以包括:
(1)至少三个基本上平面的可对折构件,其中一个基本上平面的可对折构件在其表面上有一个色谱介质,该色谱介质具有一第一端和一第二端;
(2)用于以至少两种不同的组合成对地将可对折构件相互对折叠合并在其上施加压力的部件,该压力大到足以能沿着一个大致垂直于可对折构件的方向将液体从一个可对折构传输到另一个可对折构件,从而将一种试样施加到色谱介质上并通过色谱介质从第一端流动到第二端,以检测和/或测定色谱介质上的分析物;
(3)至少一个点样器和一个吸收体,它们位于其中的一个可对折构件上并这样地设置,即当其上设有点样器和吸收体的可对折构件与其上设有色谱介质的可对折构件相互对折叠合后,则将一第二液体施加到色谱介质上并通过色谱介质从第二端流动到第一端,由此使通过色谱介质的流动反向,在接着通过色谱介质的流动反向后对分析物作出检测和/或测定。
在一个方面,按照本发明的色谱测定装置包括:
(1)一个包含一个适于接收一个要测定的试样的试样制备区的第一可对折构件;和
(2)一个包含一个色谱介质的第二可对折构件。
适用于夹心法免疫测定的色谱测定装置的一个实施例包括:
(1)一个第一可对折构件;它包括:
(a)一个具有一第一端和一第二端的色谱介质;
(b)一个与色谱介质的第一端有作用性接触的检测器点样垫;
(c)一个与检测器点样垫有作用性接触并与色谱介质的第一端间接接触的传导体;
(d)一个与色谱介质的第二端有作用性接触的吸收体;和
(2)一第二可对折构件,它包含一个用于接收要测试的试样的试样制备区。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合后,则使试样制备区与传导体接触,而将要测试的试样施加到传导体上,然后通过检测器点样垫流到色谱介质的第一端。
典型的情况是,试样制备区含有至少一种用于处理试样的试剂。在某些情况下,如在测定一种尿样或血清试样时,不需要对试样进行提取或其它处理。也是典型的情况是,检测器点样垫含有一个针对分析物的、其形式为通过向检测器点样垫中加入一种含水液体能被溶解的第一特异性结合体,该第一特异性结合体用一种可检测的标记物来标记,色谱介质进一步包含一个其面积大大小于色谱介质的面积的检测区。在这个布置中,该检测区包括在其上固定有一种针对分析物的特异性结合体,这样,如果试样中存在分析物,则在检测区中形成一个包括第一特异性结合体、分析物和第二特异性结合体的三元复合物。
更好的情况是,可检测的标记物是一种可用肉眼检测的标记物。
更好的情况是,第一和第二可对折构件由一个铰链连接。典型地,该铰链是含水液体不能透过的。可对折构件最好也包含周边直立的壁,当将装置闭合并锁定时,这些壁则靠接地接合起来。
一种试验箱可以在分开的容器中包括前面所述的色谱测定装置和一种针对分析物的、标记有一种可检测的标记物的并要被施加到检测器点样垫上的特异性结合体,或者,如果检测器点样垫含有一种可溶解的加标记的第一特异性结合体时,试验箱可以包括测定装置和一种用于溶解加标记的特异性结合体的含水液体。可以设计构造类似的试验箱,用于本发明的测定装置的其它实施例。
一种利用这种测定装置实施一种夹心法免疫测定,以检测和/或测定在一种试样中的一种分析物的方法,它包括以下步骤:
(1)将含水试样施加到色谱测定装置的检测器点样垫上,检测器点样垫上含有一种可溶解的加标记的第一特异性结合体;
(2)将色谱测定装置的第一和第二可对折构件相互对折叠合,这样,含有含水液体的试样溶解在检测器点样垫中的加标记的特异性结合体,并且该试样和被溶解的加标记的特异性结合体被施加到传导体上;
(3)使试样和加标记的特异性结合体在传导体中移动,然后至少通过一部分色谱介质,使得加标记的特异性结合体给出试样中存在分析物和/或分析物的数量的一种可检测的指示;和
(4)观测和/或测定在至少一部分色谱介质上的加标记的特异性结合体,以便检测和/或测定分析物。
在该实施例的另一方案中,第二可对折构件也包含一个与试样制备区有作用性接触的第一检测器点样垫。在这个方案中,第二检测器点样垫含有一个针对分析物的、其形式为通过将一种试样加到试样制备区中而能被溶解的第二特异性结合体,该第二特异性结合体用一种可检测的标记来标记。第二检测器点样垫是这样设置,使得将试样施加到试样制备区而溶解第二特异性结合体,从而试样制备区含有一种由试样和加标记的第二特异性结合体构成的混合物。加标记的第一和第二特异性结合体最好是相同的并且用相同的标记物来标记。
本发明的测定装置的另一个实施例包括:
(1)一第一可对折构件,它包含:
(a)一个具有一第一端和一第二端的色谱介质;
(b)一个与色谱介质的第一端有作用性接触的传导体;
(2)一第二可对折构件,它含有:
(a)一个用于接收要测定的试样的试样制备区;和
(b)一个与试样制备区隔离开的吸收体。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合后,则使试样制备区与传导体有作用性接触,而将要测试的试样施加到传导体上,使之然后流到色谱介质的第一端,同时使吸收体与色谱介质的第二端有作用性接触,而从色谱介质的第二端抽取液体。将吸收体移动到第二可对折构件上时可以应用一个较大的吸收体,这在要求测定一个相对较大体积的试样时可能是有利的。
本发明的将吸收体设置在第二可对折构件上的测定装置的另一个方案包括一个位于第一可对折构件上的试样制备区、一个色谱介质、和一个与试样制备区和色谱介质的第一端有作用性接触的传导体,从而传导体将试样制备区和色谱介质进行桥接。第二可对折构件有一个点样器和一个与点样器隔离开的吸收体,点样器含有一种针对一种分析物的、其形式为通过向点样器中加入一种含水液体能被溶解的特异性结合体。点样器中所含的特异性结合体用一种可检测的标记物来标记。在这个装置中,当将第一和第二可对折构件相互对折叠合后,则使点样器与试样制备区有作用性接触,从而当已经将一种试样加到试样制备区时,则对分析物的加标记的特异性结合体就被溶解,并导致吸收体与色谱介质的第二端有作用性接触,从而从色谱介质中抽取液体。
在本发明的将吸收体设置在第二可对折构件上的测定装置的另一个方案中,第一可对折构件包含一个色谱介质和一个传导体。第二可对折构件含有一第一点样器。一第二点样器和一吸收体。吸收体与第一和第二点样器隔离开。第一和第二点样器这样地设置在第二可对折构件上,使得当第一和第二可对折构件未对折叠合时,它们不处于有作用性接触。吸收体这样地设置,使得当第一和第二可对折构件相互对折叠合后,它与色谱介质的第二端有作用性接触。第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合后,则导致传导体与第一点样器有作用性接触,并导致传导体与第二点样器有作用性接触,由此导致第一和第二点样器相互间有作用性接触。
在这个装置中,第二点样器可以包含一个检测器点样垫,检测器点样垫含有一种可溶解形式的加标记的第一特异性结合体。
一种应用本发明的这种装置的方法包括将试样施加到第一点样器上,并将第一和第二可对折构件相互对折叠合,从而使试样溶解检测器点样垫中的加标记的特异性结合体,色谱法和检测步骤如上所述。
本发明的将一个吸收体设置在第二可对折构件上的另一个测定装置包括:
(1)一第一可对折构件;它包含:
(a)一个具有一第一端和一第二端的色谱介质;
(b)一个与色谱介质的第一端有作用性接触的传导体;
(c)一个检测器点样垫,它与传导体直接接触,并设置得与色谱介质的第一端间接接触;和
(2)一第二可对折构件;它含有:
(a)一个试样点样垫;和
(b)一个与试样点样垫隔离开的吸收体。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当第一和第二可对折构件相互对折叠合时则导致:
(1)试样点样垫将试样施加到检测器点样垫上,由此通过传导体施加到色谱介质的第一端;
(2)吸收体与色谱介质的第二端有作用性接触。
一种采用这种方案的测定装置的检测方法类似于上面所述的那些方法。
本发明的将一个吸收体设置在第二可对折构件上的另一个方案的测定装置包括:
(1)一第一可对折构件;它包含:
(a)一个具有一第一端和一第二端的色谱介质;
(b)一个与色谱介质的第一端直接接触的检测器点样垫;
(2)一第二可对折构件;它包含:
(i)一个试样点样垫;和
(ii)一个与试样点样垫隔离开的吸收体。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当第一和第二可对折构件相互对折叠合时,则除了检测器点样垫直接与色谱介质的第一端相邻的区域外,将使检测器点样垫和试样点样垫接触。将这个装置的第一和第二可对折构件相互对折叠合后导致;
(1)要测试的试样被施加到检测器点样垫上,然后施加到色谱介质的第一端;和
(2)吸收体与色谱介质的第二端有作用性接触。
本发明的将一个吸收体设置在第二可对折构件上的另一个测定装置包括:
(1)一第一可对折构件;它包含:
(a)一个具有一第一端和一第二端的色谱介质;
(b)一个传导体,它是这样设置的,即当第一和第二可对折构件未对折叠合时,它不与色谱介质的第一端有作用性接触;和
(2)一第二可对折构件;它包含:
(i)一第一点样器;
(ii)一第二点样器;
(iii)一个与第一和第二点样器隔离开的吸收体,第一和第二点样器是这样设置在第一可对折构件上的,即当第一和第二可对折构件未对折叠合时,它们之间不处于有作用性接触。
在这个装置中,第一和第二可对折构件的结构是这样设置的,即当将第一和第二可对折构件相互对折叠合时,则有:
(1)导致传导体与第一点样器有作用性接触,传导体与第二点样器有作用性接触,以及第二点样器与色谱介质的第一端有作用性接触,由此使第一和第二点样器相互间处于有作用性接触,使第一和第二点样器的内含物被施加到色谱介质上;和
(2)导致吸收体与色谱介质的第二端有作用性接触。
本发明适用于实施夹心法免疫测定的测定装置的另一个实施例能够用一部分试样洗涤色谱介质,以除去未结合的加标记的特异性结合体,减少本底。这个实施例包括:
(1)一第一可对折构件;它包含:
(a)一个具有一第一端和一第二端的色谱介质;
(b)一个与色谱介质的第一端有作用性接触的传导体;
(c)一个与色谱介质的第二端有作用性接触的吸收体;
(2)一个含有一个点样器的第二可对折构件,点样器被分成两个扇区(sector):
(a)一第一扇区,其含有一个针对分析物的、其形式为通过将一种含水液体加到点样器中而能被溶解的第一特异性结合体,该第一特异性结合体用一种可检测的标记物来标记;和
(b)一个不合有加标记的特异性结合体的第二扇区。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使点样器的第一扇区,而不是第二扇区与传导体直接接触,将点样器的第一扇区的内含物施加到色谱介质上。在将点样器的第一扇区的内含物施加到色谱介质上之后,接着将点样器的第二扇区的内含物施加到色谱介质上,以提供一次洗涤。
本发明的另一个实施例包含能利用一种加标记的分析物的模拟物来实施竞争法免疫测定的的测定装置。这个实施例的一个方案包括:
(1)一第一可对折构件;它包含:
(a)一个具有一第一端和一第二端的色谱介质,且在它上面的一个大大小于其面积的分散区域中固定有分析物或它的一个免疫学模拟物;
(b)一个与色谱介质的第一端有作用性接触的第一传导体;知
(c)一个与色谱介质的第二端有作用性接触的第二传导体;
(2)一第二可对折构件,它有一第一点样器,第一点样器含有一个针对分析物的、其形式为通过将一种第一含水液体加到第一点样器中而能被溶解的第一特异性结合体;
(3)一第三可对折构件;它包含:
(a)一第二点样器,第二点样器含有一个针对分析物的、其形式为通过一种第二含水液体加到第二点样器中而能被溶解的第二特异性结合体,第二特异性结合体用一种可检测的标记物来标记,
(b)一个与第二点样器隔离开的吸收体。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使第一传导体与第一点样器有作用性接触,从而使第一点样器的内含物被施加到色谱介质,并至少流过一部分色谱介质。第一和第三可对折构件的结构是这样设计的,即当将第一和第三可对折构件相互对折叠合时,则使吸收体与第一传导体有作用性接触从而从色谱介质中抽取液体。将第一和第三可对折构件相互对折叠合时,也使第二点样器与第二传导体有作用性接触,从而第二点样器的内含物被施加到色谱介质,并至少流过一部分色谱介质,这部分色谱介质与抽吸第一点样器的内含物所通过的部分是重叠的。
在这个装置中,第一特异性结合体和加标记的第二特异性结合体最好都是分析物的抗体,更好的是,固定的分析物或其模拟物包括共价地连接到一种对分析物缺乏特异性结合活性的蛋白质上的分析物。
一种应用这种测定装置通过竞争法免疫测定来检测一种分析物的方法包括:
(1)将试样施加到色谱测定装置的第一点样器上,试样包含第一含水液体;
(2)将一种重新构成液体施加到第二点样器上,重新构成液体包含第二含水液体;
(3)将色谱测定装置的第一和第二可对折构件相互对折叠合,从而该试样和针对分析物的被溶解的特异性结合体被施加到第一传导体上,然后被施加到色谱介质的第一端上;
(4)使试样和被溶解的第一特异性结合体移动至少通过一部分色谱介质,阻断固定在离散区域中的免疫学模拟物上的结合点;
(5)将第一和第二可对折构件分离开,使之不再叠合在一起;
(6)将第一和第三可对折构件相互对折叠合,从而被溶解的加标记的第二特异性结合体被施加到第二传导体,然后被施加到色谱介质的第二端上;
(7)让被溶解的加标记的第二特异性结合体移动至少通过一部分色谱介质,这部分色谱介质与试样和被溶解的第一特异性结合体被抽吸所通过的整个色谱介质部分是重叠的,从而当试样中存在分析物时,由于试样和分析物与第一特异性结合体结合,加标记的第二特异性结合体就结合到固定在分散区域中的分析物或它的免疫学模拟物上;
(8)观测和/或测定分散区域中的第二特异性结合体,以便检测和/或测定分析物。
更好的情况是,这种方法进一步包括以下步骤,即在将试样施加到第一点样器上之后,对色谱测定装置进行培养,以便促进分析物和第一特异性结合体之间的反应。
在应用这种装置的测定方法的另一种选择方案中,除了将一第一重新构成的液体加到试样上外,还可以将其加到第一点样器上。
本发明的适用于竞争法免疫测定的测定装置的其它一些方案可以以类似的方式来应用。
本发明的用于实施竞争法免疫测定的测定装置的又一个方案包括:
(1)一第一可对折构件;它包含:
(a)一个具有一第一端和一第二端的色谱介质,且在它上面的一些其面积都大大小于色谱介质的分散的和非重叠的区域中固定有:
(i)对分析物的一种特异性结合体;和
(ii)一种次特异性结合体,该次特异性结合体能够与一个对分析物缺乏亲合力的特异性结合体对中的一个组分相结合,次特异性结合体设置得比第一特异性结合体更靠近色谱介质的第一端;
(b)一个与色谱介质的第一端有作用性接触的第一传导体;和
(c)一个与色谱介质的第二端有作用性接触的第二传导体;
(2)一第二可对折构件;它包含:
(a)一个含有一种分析物的模拟物的点样器,该分析物的模拟物包括与一个对分析物缺乏亲合力的特异性结合体对中的一个组分共价地相结合的、并能被次特异性结合体结合的分析物,特异性结合体对中的那个组分上标记有一种可检测的标记物,分析物的模拟物的形式为通过将一种含水液体加到点样器中而能被溶解;和
(b)一个与点样器隔离开的吸收体。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使第二传导体与点样器有作用性接触,从而将点样器的内含物施加到色谱介质上,并至少流过一部分色谱介质,同时使吸收体与第一传导体有作用性接触,以便从色谱介质中抽取液体。
装置的这个方案最好进一步包括一个铰接在第一可对折构件上的盖子,当将第一和第二可对折构件相互对折叠合时,盖子可以折叠在第一和第二可对折构件上面,盖子上开有孔口,用以在将第一和第二可对折构件相互对折叠合并且将盖子折叠在第一和第二可对折构件上面后观察至少一部分色谱介质。
更好的情况是,在这种方案中,第一特异性结合体是一个对分析物有特异性的抗体,而次特异性结合体是一个能够结合对分析物缺乏特异性的一种免疫球蛋白的第二抗体。更好的情况是,分析物的模拟物包括共价地连接到一种取自一种生物种类的免疫球蛋白上的分析物,而特异性结合体是这种生物种类有特异性的抗体。
这种方案可以进一步包括一个其上含有一个吸收体的第三可对折构件,吸收体是这样设置的,即当第一和第三可对折构件相互对折叠合后,则使吸收体与整个色谱介质和两个传导体接触。在这种方案中,在色谱介质的后面设有一个开孔,可以在第二可对折构件折叠到第一可对折构件上面和第三可对折构件折叠到第二可对折构件上面之后从后面观察至少一部分色谱介质。
在另一种变型中,固定在色谱介质上的次特异性结合体的面积被分成至少两个分散的且不重叠的带区,每个带区中的次特异性结合体的数量是确定的,从而由分析物的模拟物所结合的带区的数目指示出结合到检测区中的分析物的模拟物的数量,因而指示出测试试样中的分析物的浓度。
本发明的适用于实施竞争法免疫测定的测定装置的又一个方案采用一种生物素-抗生物素蛋白连接(link)。装置的这个方案包括:
(1)一第一可对折构件,它包含一个具有一第一端和一第二端的色谱介质,且在它上面的一些单独的、其面积都大大小于色谱介质的分散的和非重叠的区域中固定有:
(a)一种能够与生物素特异性结合的物质,该生物素选自由抗生物素蛋白(avidin),抗生物蛋白链菌素(Streptavidin),抗-生物素抗体,和它们的衍生物组成的组;
(b)一种次特异性结合体,该次特异性结合体能够与一个三元复合物特异性结合体地相结合,该三元复合物包括:(i)分析物;(ii)一个对分析物缺乏亲合力的特异性结合体对中的一个组分,该组合共价地结合到分析物上;和(iii)一个结合到特异性结合体对中的这个组分上的可检测的标记物;
(2)一第二可对折构件,它包含一第一点样器,该第一点样器含有一种针对分析物的、形式为通过将一种含水试样加到第一点样器中而能被溶解的第一特异性结合体,第一特异性结合体共价地结合到生物素上,第一特异性结合体不能被次特异性结合体结合;
(3)一第三可对折构件;它包括:
(a)一个含有三元复合物的第二点样器,三元复合物的形式为通过将一种第二含水液体加到第二点样器中而能被溶解;
(b)一个与第二点样器隔离开的吸收体。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使第一传导体与第一点样器有作用性接触,从而将第一点样器的内含物施加到色谱介质上,并至少被抽吸通过一部分色谱介质,其中,第一和第三可对折构件的结构是这样设计的,即当将第一和第三可对折构件相互对折叠合时,则使吸收体与第一传导体接触,从而从色谱介质中抽取液体,并使第二点样器与第二传导体有作用性接触,从而将第二点样器的内含物施加到色谱介质,并至少被抽吸通过与第一点样器的内含物被抽吸通过的那部分色谱介质相重叠的一部分色谱介质。
更好的是,第一特异性结合体是一种抗分析物的抗体。在三元复合物中的特异性结合体对的那个组分可以是家兔免疫球蛋白G,在这种情况下,次特异性结合体可以是山羊抗家兔(goatanti-rabbit)IgG。更好的是,能够特异性地结合生物素的物质是抗生物蛋白链菌素。
固定在色谱介质上的次特异性结合体的区域分成至少两个分散的且不重叠的带区,每个带区中的次特异性结合体的数量是确定的,从而由三元复合物结合的带区的数目指示出结合到检测上的三元复合物的数量,由此指示出试样中原始分析物的浓度。
本发明的适用于实施竞争法免疫测定的色谱测定装置的又一个方案包括:
(1)一第一可对折构件;它包含:
(a)一个具有一第一端和一第二端的色谱介质,且在它上面的一些其面积都大大小于色谱介质的单独的和非重叠的离散区域中固定有:
(i)一种能够结合针对分析物的特异性结合体的分析物的模拟物;和
(ii)一种次特异性结合体,该次特异性结合体能够与一个对分析物具有亲合力的特异性结合体对中的一个组分相结合,次特异性结合体本身缺乏对分析物的亲合力;
(b)一个与色谱介质的第一端有作用性接触的传导体;
(2)一个有一个点样器的第二可对折构件,点样器含有一种针对分析物的、形式为通过将一种含水液体加到点样器中而能被溶解的特异性结合体。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使传导体与点样器有作用性接触,从而将点样器的内含物施加到色谱介质上并使之至少通过一部分色谱介质。
更好的是,第一特异性结合体是对分析物有特异性的抗体,而分析物的模拟物包括共价地连接到一种蛋白上的分析物,该蛋白对分析物或分析物的特异性结合体缺乏特异性结合活性,更好的是,在不涉及分析物抗体的抗原结合点的生物种类-特异性相互作用的基础上,次特异性结合体与对分析物有特异性的抗体相结合。
在这个装置中,固定在色谱介质上的次特异性结合体的区域可以分成至少两个分散的且不重叠的带区,每个带区中的次特异性结合体的数量是确定的,从而由针对分析物的加标记的特异性结合体结合的带区的数目指示出结合到检测区上的针对分析物的加标记的特异性结合体的数量,由此指示出试样中分析物的数量。
本发明适用于实施竞争法免疫测定的测定装置的又一个方案是一种三构件型装置,它涉及试剂在色谱介质中迁移的两个步骤,这两个步骤发生在相同的方向上。这个装置包括:
(1)一第一可对折构件;它包含:
(a)一个具有一第一端和一第二端的色谱介质,且在它上面的一些单独的、其面积都大大小于色谱介质的离散的和非重叠的区域中固定有:
(i)一种针对分析物的特异性结合体;和
(ii)一种如前所述的次特异性结合体,该次特异性结合体能够与一个对分析物缺乏亲合力的特异性结合体对中的一个组分相结合,分析物的特异性结合体设置得更靠近色谱介质的第一端,
(b)一个与色谱介质的第一端有作用性接触的第一传导体,第一传导体能起着一第一点样器的功能;和
(c)一个与色谱介质的第二端有作用性接触的第二传导体;
(2)一第二可对折构件,它包含:
(a)一个含有如前所述的一种分析物的模拟物的第二点样器,该分析物的模拟物的形式为通过将一种含水液体加到点样器中而能被溶解;
(b)一个与第二点样器隔离开的第一吸收体;
(3)一个含有第二吸收体的第三可对折构件。
在这个装置中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使第二点样器与第一传导体有作用性接触,以及使第一吸收体与第二传导体有作用性接触。第一和第三可对折构件的结构是这样设计的,即当将第一和第三可对折构件相互对折叠合时,则使第二吸收体与第一传导体和色谱介质直接接触,从而从色谱介质中抽取液体。
通过参阅以下的说明、所附的权利要求书和附图,将会更好地理解本发明的这些和其它特征、结构、方法和优点。附图中:
图1A是本发明的两构件型色谱测定装置的一个实施例的示意图;
图1B是图1A所示两构件型色谱测定装置在两构件已经相互对折叠合后的示意图;
图2是本发明的两构件型色谱测定装置的另一个实施例的示意图,其中第一可对折构件包含一个试样制备区和一个与试样制备区不连通的色谱介质,及第二可对折构件包含一个传导体的连接件;
图3是本发明的两构件型色谱测定装置的又一个实施例的示意图,其中将一个试样制备区包含在第一可对折构件上;
图4是图3所示实施例的另一种选择方案的示意图,其中将一个吸收体设置于第二可对折构件上,而不是设置于第一可对折构件上;
图5是本发明的两构件型色谱测定装置的又一个实施例的示意图,其中将一个试样制备区和一吸收体设置在同一个可对折构件上;
图6是本发明的两构件型色谱测定装置的又一个实施例的示意图,其中将两个检测器点样垫设置于不同的可对折构件上;
图7是本发明的两构件型色谱测定装置的又一个实施例的示意图,其中将两个点样器设置于其中一个构件上;
图8是图7所示实施例的另一种选择方案的示意图,其中将一个吸收体设置于第二可对折构件上,而不是设置于第一可对折构件上;
图9是本发明的又一个实施例的示意图,其中在一个传导体和色谱介质之间包含一个间断部分,它在装置闭合时被桥接起来;
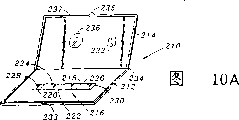
图10A是本发明的两构件型色谱测定装置的又一个实施例的示意图,其中包含一个与色谱介质处于有作用性接触的检测器点样垫;
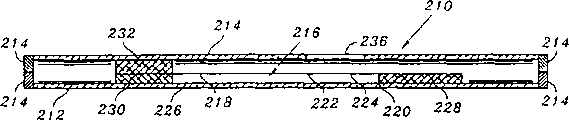
图10B是图10A所示的两构件型色谱测定装置的一个剖面后视图,其示出了处于相互对折叠合起来的构件的细节;
图11A是本发明的两构件型色谱测定装置的又一个实施例的示意图,它大体上类似于图10的实施例,但检测器点样垫与色谱介质则为直接接触;
图11B是图11A所示的两构件型色谱测定装置的一个剖面后视图,其示出了处于相互对折叠合起来的构件的细节;
图12A是本发明的适合于实施双向色谱过程的两构件型色谱测定装置的一个实施例的示意图;
图12B是图12A所示的两构件型色谱测定装置的一个顶视图,其示出了已经处于相互对折叠合起来的两个构件;
图13A是本发明的适合用于实施双向色谱过程的两个构件型色谱测定装置的又一个实施例的示意图,它有两个点样器和一个传导体;
图13B是图13A所示的两构件型色谱测定装置的一个顶视图,其示出了已经处于相互对折叠合起来的两个构件;
图14是本发明的两构件型色谱测定装置的又一个实施例的示意图,其中一个检测器点样垫设置于第一可对折构件上,而一个试样制备区设置于第二可对折构件上;
图15是本发明的两构件型色谱测定装置的又一个实施例的示意图,其中点样器被分成两个扇区,可以用不加标记的试样冲洗色谱介质;
图16A是适合用于实施双向色谱过程的两构件型色谱测定装置的又一个实施例的示意图,它带有一个盖子;
图16B是图16A所示的两构件型色谱测定装置的一个顶视图,其示出了已经牌相互对折叠合起来的两个构件;
图17A是本发明的一种三构件型色谱测定装置的示意图;
图17B是图17A所示的三构件型色谱测定装置的一个剖面后视图,其示出了处于相互对折叠合起来的构件的细节;
图18是本发明的三构件型色谱测定装置的又一个实施例的示意图,其中第三构件用于从整个色谱介质和两个传导体中吸收液体;
图19是本发明的一种多重型色谱测定装置的一个示意图,适用于测量一个或多个试样;
图20是本发明的一种多重型色谱测定装置的一个实施例的示意图,其中包含一个用于容纳试样的可收缩的槽;
图21是本发明的能接受一个试验卡的一种多重型色谱测定装置的一个不同实施例的示意图;
图22是本发明的能接受一个试验卡的一种多重型色谱测定装置的另一个实施例的示意图;
图23是本发明的一种三构件型色谱测定装置的一个实施例的示意图,它适用于利用一种与稳定在色谱介质上的一种分析物的模拟物结构的标记抗体实施一种竞争法免疫测定;
图24是一种带有盖子的两构件型色谱测定装置的一个示意图,它适用于利用一种加标记的分析物的模拟物实施一种竞争法免疫测定;
图25是一种三构件型色谱测定装置的一个示意图,它适用于利用一种加标记的分析物的模拟物实施一种单向竞争法免疫测定,其中第三构件用于从整个色谱介质和两个传导体中吸收液收;
图26是本发明的一种三构件型色谱测定装置的一个示意图,它适用于实施一种竞争法免疫测定,该装置采用一种生物素一抗生物素蛋折连接(link);
图27是一种适用于利用一种加标记的抗分析物的抗体实施一种竞争法免疫测定的两构件型色谱测定装置的一个示意图;以及
图28是本发明的一种测定装置的一个说明示意图,这个装置适用于接受一个签条或类似的试样装置,且设计成用于检测链球菌A抗原。
在本发明的上下文中,除非另有说明,以下术语定义如下:
特异性结合体(Specific Binding Partner):指借助于特异性非共价相互作用而发生相互作用的一对分子中的一个分子,其中相互作用取决于所涉及的分子的三维结构。典型的特异性结合体对包括:抗原-抗体,半抗原-抗体,激素-受体,核酸束(nucleicstrand)-补体梳酸束(strand),底物(substrate)-酶,抑制剂-酶,碳水化合物-外源凝集素,生物素-抗生物素蛋白,以及病毒-细胞受体。
作用性接触:指当两个固体构件不论是直接地,还是间接地接触时,如果一种含水液体能够借毛细作用或其它方式基本上不间断地从两个构件中的一个构件流动到另一个构件,则两个构件处于作用性接触。“直接接触”是指两个构件处于实际接触,例如边缘对边缘,或前面对后面。典型的情况是,当两个构件直接接触时,它们大约重叠0.5毫米至3毫米。但是两个构件可以用对接边缘放置。“间接接触”是指两个构件不是处于实际接触,而是由一个或多个导体桥连接起来。
有限容量:指在装置中进行正常的测定期间,位于装置中的一种吸收体(剂)要吸收液体,当吸收体被所吸收的液体浸透而饱和时,则这种吸收体具有有限容量。此时吸收体可以释放所吸收的额外液体并成为至少具有部分传导性。
分析物:术语“分析物”既包括要测定的实际的分子,也包括其模拟物和衍生物,此时这种模拟物和衍生物以基本上等同于分析物本身的方式与测定分析中采用的另一个分子相结合。
抗体:术语“抗体”既包括具有恰当特异性的完整的抗体分子,也包括抗体片段(包括Fab,F(ab′),和F(ab′)2片段),以及经过化学变型的完整的抗体分子和抗体片段,包含经体外亚单位再结合体所组成的杂交抗体。
次特异性结合体:指当一对特异性结合体相互作用时,这对特异性结合体中的一个组分结合的一个附加的特异性结合体称之为次特异性结合体。例如,一对特异性结合体可以包括贾第鞭毛虫病(Giardia)抗原和家兔抗贾第鞭毛虫病抗体。在这种情况下,次特异性结合体可以是山羊抗家兔IgG抗体。次特异性结合体可以对它要结合的一个抗体特异性结合体的品种、级别或次级是特异性的。另一种形式是,当其中的一个特异性结合体被用生物素标记后,次特异性结合体可以包含一个与抗生物素蛋白结合的分子。
为了方便读者和帮助读者理解本说明书公开内容的构成,给出了以下的内容概要,它以章节标题的形式陈述了本说明书公开内容的构成。
I.色谱测定装置
A.两构件型装置
1.总体布置
2.两构件型装置的具体实施例
a.在第二构件上设置有传导性连接件的装置
b.在第一可对折的构件上设有试样制备区的装置
c.在第二可对折的构件上设有吸收体(吸收剂)的装置
d.在同一个可对折的构件上设有试样制备区和吸收体的装置
e.在不同的可对折构件上设有两个检测器点样垫的装置
f.在同一可对折构件上包括有两个独立点样器的装置
g.在第二可对折的构件上设有两个点样器和一个吸收体的装置
h.在传导体和色谱介质之间设有间隙或间断的装置
i.在与色谱介质同一可对折构件上设有用于加标记的特异性结合体的垫的装置
j.检测器点样垫与色谱介质的第一端直接接触的装置
k.在第二可对折的构件上设有第二点样器和吸收体的双方向的装置
l.包括有两个点样器和一个传导体的双方向的装置
m.在第一构件上设有检测器点样垫的装置
n.设有提供洗涤的两扇区点样器的装置
B.带有盖子的两构件型装置
C.三构件型装置
D.多构件型装置
1.基本的多构件型装置
2.带有可收缩的槽(collapsible well)的多构件型装置
3.可以接受试验卡片的多构件型装置
H.用于竞争法测定分析的色谱测定装置
A.三构件双向流动装置
B.带有盖子的两构件双向流动装置
C.带有吸收体的三构件单向流动装置
D.应用生物素的特异性的三构件双向流动装置
E.用于竞争法抑制免疫测定分析的两构件型装置
III.在测定装置中应用的分析物和抗体
IV.试验箱(test kits)
I.色谱测定装置
本发明的一个方面包括尤其使用于测定生物试样中的分析物测定的色谱测定装置。这些装置适用于生物试样的直接点样,不需要初始的提取步骤,并且所具有结构能够使由颗粒或经着色的试样引起的对测定结果的干扰减小的最小程度。
该装置具有至少两个基本上平面的可对折构件,其中一个基本上平面的可对折构件在其表面上有一种色谱介质。
该装置还有用于对折可对折构件和向其上施加压力的部件。所施加的压力足以将液体从一个可对折构件沿基本上垂直于可对折构件的方向传送到另一个可对折构件上,从而将试样施加到色谱介质上,以便检测和/或测定其上的分析物。压力也驱使液体通过色谱介质,来加快色谱分析过程,从而在较少的时间内得出一个可检测的结果。此外,压力也使得在装置中实施一些步骤,例如提取步骤,成为可能,并且能够用于通过吸收体从色谱介质中除去多余的液体,以减少测定分析中的本底。压力是通过将可对折构件置于相对折叠位置并用连接件如锁件或扣紧件使构件保持在对折叠合位置而形成的。
按照本发明的装置,其结构的构成即可为夹心法测定分析又可为竞争法测定分析。
当装置被设计成用于实施一种夹心法免疫测定分析形式时,典型的情况是,至少装置的其中一个可对折构件上有一个相对于分析物的一第一加标记的特异性结合体。这个相对于分析物的第一加标记的特异性结合体处于一种能够被一种含水液体溶解的形式。用于溶解的含水液体可以是试样。第一加标记的特异性结合体设置在能使之与试样中的分析物反应的位置。
在一个适合实施一种夹心法免疫测定分析的装置中,色谱介质上包含有一第二加标记的特异性结合体的检测区,用于固定在其上的分析物。检测区大大地小于色谱介质。对这些构件进行布置,使得若在试样中有分析物时则在检测区处形成一个包含(1)第一加标记的特异性结合体,(2)分析物和(3)第二不加标记特异性结合体的三元复合物。
在一个适合实施一种竞争法免疫测定分析的装置中,色谱介质上在至少一个大大地小于色谱介质的区域中包含有一对特异性结合体中的一个组分,该特异性结合体对选自于由分析物或它的一个模拟物和该分析物的一个特异性结合体组成的组。可以有一些不同的布置用于本发明的适合实施竞争法免疫测定分析的装置。这些不同的布置描述如下。
在一个色谱介质中加入试样之后,典型地是利用一个可肉眼检测的加标记的组分检测和/或测定分析物。加标记的组分最好是分析物或者是它的一个联结到可肉眼检测的标记上的模拟物,或者是一个联结到一个可肉眼检测的标记上的分析物的特异性结合体。
本发明的测定装置可以设计成用于同时实施一个以上的测定。在这种装置中,基本上平面的构件中的一个上面至少有两个独立的不接触的色谱介质。
装置的一种变型尤其适用于双向色谱法,尽管并不局限于这种用途。这种装置至少有三个基本上平面的可对折构件。其中一个基本上平面的构件上其表面上有一个具有一第一端和一第二端的色谱介质。这种三构件装置也有至少以两种不同的组合成对地折合可对折构件并在其上施加压力的部件,利用象锁件或扣紧件这样的联结件将被折合的构件保持在一起。施加的压力足以将液体从一个可对折构件沿基本上垂直于可对折构件的方向传送到另一个可对折构件上,并驱使液体通过色谱介质,从而将试样施加到色谱介质上,使试样通过色谱介质从第一端流动到第二端。
装置还有至少一个点样器和一个吸收体,它们位于其中的一个可对折构件上,并这样地设置,即当其上设有点样器和吸收体的可对折构件被置于其上设有色谱介质的可对折构件相对叠合的位置时,则一第二液体被施加到色谱介质上。该第二液体通过色谱介质从第二端流动到第一端。它使通过色谱介质中的流动反向。在流动反向后对分析物进行检测和/或测定。
A.两构件型装置
本发明的测定装置的一个实施例是一种在一维空间内以单向流工作的两构件色谱测定装置。
1.两构件型装置的总体布置
总体上,本发明的两构件色谱测定装置包括:
(1)一第一可对折构件,它包含一个适于接受要测定的一种试样的试样制备区;和(2)一个包含一个色谱介质的第二可对折构件。
在这个装置中,当装置闭合时可以将第一和第二可对折构件置于相互对折叠合位置,从而使试样制备区将被测定的试样施加到色谱介质上。在使用时,典型地是在将一种检测试剂加到试样制备区之后将第一和第二可对折构件置于相互对折叠合位置。当将第一和第二可对折构件置于相互对折叠合位置后,试样制备区将试样和检测试剂施加到色谱介质上。在允许试样和检测试剂至少横向移过色谱介质的一部分,使得检测试剂给出分析物存在的和/或其数量的可检测指示后,则在至少一部分色谱介质中观察和/或测定检测试剂,其结果是检测和/或测定分析物。
只要可能,对这个基本装置的结构细节的描述也适用于本发明的其它两构件和三构件测定装置。
检测试剂包括上述用于分析物的第一特异性结合体,它也可以包括一些附加的组分。
依赖于检测区中的第二特异性结合体的密度和检测区的大小,这种方法可以给出分析物的一个定性和/或定量的指示。
典型地,为了获得结果,这种测定需要的时间为30秒至10分钟,更典型地是1至5分钟,包括试样在试样制备区上的培养(潜伏)期以及色谱分析本身所需要的时间。虽然根据分析物和特异性结合体的特性的不同,在某些情况下,可以在4℃或直到37℃或更高温度下实施这种测定,但典型地是在室温下实施这种测定的。在某些情况下,可能要求在较低的温度下,以便限制降解(degradation),而在某些其它情况下,在较高的温度下对合适的分析物和特异性结合体进行测定则可以使测定的速度加快。
色谱测定装置的这种总体布置示于图1A中。色谱测定装置10有一第一可对折构件11和一第二可对折构件12,第一可对折构件11包含一个试样制备区13,第二可对折构件12包含一个色谱介质14。色谱介质14有一第一端15和一第二端16,并且其还包含一个检测区17和一个控制区18。第一可对折构件11和第二可对折构件12由一个铰链19连接起来。第一可对折构件11和第二可对折构件12最好还包括使它们固定在相互对折叠合位置上的一些连接件。这些连接件可以包括锁件,例如锁件20和21,它们在第一可对折构件11和第二可对折构件12被置于相对的叠合位置上时相互接合。锁件20和21的结构和尺寸可以改变,以便在可对折构件11和12上施加的压力为最佳程度。最合适的压力程度可能取决于色谱介质14的厚度和结构,预计试样的体积,和其它一些因素。为了防止试样或试剂的泄漏,在第一和第二可对折构件11和12的周边上设置有一个密封凸缘或密封垫22。虽然一般还是应用连接件,如锁件20和21,和密封凸缘或密封垫22更好,但是构造出本发明的一个基本装置并不是必须有这些部件,第二可对折构件12有一第一窗口23,第一可对折构件11也可以有选择地有一第二窗口24,以便能从任一侧来观测色谱介质14。由第二窗口24可以从与施加试剂的表面相对的表面来观测色谱介质14。作为另一种选择,可以没有第一窗口23,而用第二窗口24来观测色谱介质14。一般地,本发明的两构件型装置即可以有一个窗口也可以有两个窗口(也称为开孔),以便即能通过没装有色谱介质14的可对折构件上来观测色谱介质14,如图1中的窗口23,也能通过装有色谱介质14的可对折构件来观测色谱介质14,如图1的窗口24。另一种方式是,可以用透明的或半透明的材料制作第一和/或第二可对折构件11和12,从而没有单独开的开孔或窗口也能观测色谱介质14。
图1B示出了在可对折构件11和12被置于相互对折叠合位置之后的装置10。包含有检测区17和控制区18的色谱介质14可以通过窗口23看到。试样制备区13在第一端15处或第一端15的附近与色谱介质14接触,从而试样制备区13中的物质可以流过包含检测区17和控制区18的色谱介质14。
装置10可以有选择地进一步包括一个与色谱介质14的第一端15有作用性接触的传导体25,如图1A所示。传导体25可以是一种能够传导一种含水液体而不会大量吸收该液体的材料,如纤维素材料或其它材料。可以用一种表面活性剂处理传导体25,以便能更均匀地将试剂施加到色谱介质14上。在设置传导体25的情况下,当第一和第二可对折构件11和12被置于相互对折叠合位置之后,试样制备区13最好与传导体25接触。
装置10可以进一步包括一个与色谱介质14的第二端16有作用性接触的吸收体26,以帮助将液体从第一端15通过色谱介质14引向第二端16,如图1A中所示。
试样制备区13可以用任何合适的材料制作,例如,纤维素、纸、尼龙、人造丝、玻璃纤维、羊毛、非织造合成材料,但不限于这些材料。可以选择试样制备区13的空隙度来过滤出试样(如全血液试样或粪便试样)中的细胞或颗粒物质。试样制备区13可以包含至少一种试剂,用于在将试样施加到色谱介质14上之前处理该试样。
可以用于试样制备区13中的试剂随着要施加到试样制备区13上的试样和要测定的分析物的不同而改变,它们可以包含调节pH值的酸或碱,稳定pH值的缓冲剂,与金属结合成螯合物的螯合剂(如EDTA或EGTA),溶解动物细胞的细胞膜或细菌的细胞壁以释放分析物的水解酶,酶的底物(作用物)或辅酶,等等,但也不局限于这些试剂。一种特别有用的提取试剂是亚硝酸钠和醋酸的一种混合物,用于产生亚硝酸。亚硝酸钠可以干化形式呈现在试样制备区13中,醋酸可以在加入试样以后再加到试样制备区13中。
试样,或一个取样装置,如喉咙签板或微孔过滤器,可以由操作者放置到试样制备区13上,如果需要,也可以加入其它试剂。
第一和第二可对折构件11和12的本体最好是用具有足够的不透水性而能够盛住实施测定所含有液体的层压硬纸板制成,也可以使用其它纤维素基的材料,如纸板或固体漂白的亚硫酸盐。或者用不透水的塑料材料制成上述本体。一种合适的塑料材料是诸如Lexan商标的聚碳酸脂塑料。
铰链19最好用不使含水液体可透过的材料制成,例如可以与第一和第二可对折构件11和12的本体使用的材料兼容相连的塑料,或者与之相同的材料。
典型地,色谱介质14、吸收体26、传导体25、和其它接受液体的部件都用粘胶剂固定到第一和第二可对折构件11和12的本体上。合适的粘胶剂在本技术领域是公知的。也可以采用其它的连接方法,如用订书钉钉住或用图钉钉住。
分析物的测定,或者利用分析物的一个加标记的特异性结合体来进行,或者利用分析物的特异性结合体的一个加标记的次特异性结合体来进行。在大多数情况下,更愿意采用分析物的一个加标记的特异性结合体。加标记的特异性结合体的标记最好是一种可肉眼检测的标记物,如一种胶态金属标记物。更好地是该胶态金属标记物是金、银、铜、铁、或锡;最好是金。在德迈(I.DeMey)的文章“金制探针的制备和使用”中描述了用金标记的抗体的制备方法,这篇文章刊登在1986年英国布里斯托尔的J.M.Polak&S.VanNoorden出版的杂志《免疫细胞化学:现代方法和应用》,第8章,第115-145页中,在此一并作参考。用胶态金标记的抗体可以在市场上买到,例如从密苏里州圣路易斯的Sigma化学公司购买。
另一种方式是,也可以采用其它的胶态标记物,如胶态硫标记物或染色二氧化硅标记物。在另一种较差的选择方案中,可肉眼检测的标记物可以是一种着色的胶乳标记物。也可以采用其它标记物,例如放射性标记。
虽然申请人并不一定想要受这一理论的约束,当含有一种试样的含水液体施加到一种用一个胶态金属标记物(如胶态金)所标记的可溶解特异性结合体上时,分析物和加标记的特异性结合体之间的反应速度是极快的。这种极快速度导致在分析物和加标记的特异性结合体的组合物被施加到色谱介质上之前分析物就基本上完全被标记。因此,在用本发明的测定装置进行一种单向色谱过程时,受色谱检测的对象主要是分析物和相应加标记的特异性结合体中的二元复合物。这可以使这种复合物从不与特异性结合体结合的污染体中分离出来,提高检测的精确性。
在本实施例中,置于试样制备区13中的加标记的特异性结合体最好呈能够通过向试样制备区中加入一种含水液体而溶解的形式。典型地,含水液体就是试样本身。在某些情况下,尤其是采用小的试样体积时,可能希望在试样制备区中加入附加的缓冲剂或其它含水液体。
在下面讨论的其它实施例中,加标记的特异性结合体可以置于色谱测定装置的一个构件上,该构件与试样制备区分开,但在实施检测期间与试样制备区相接触。在这些实施例中,加标记的特异性结合体最好以可溶解的形式置于这个构件上,并且在试样与该构件接触时被溶解。在某些情况下,可以在构件上加入一种不同于试样的单独的含水液体来溶解标记特异性结合体。
在第二可对折构件12上的色谱介质14是一个平的带条,典型地,带条是矩形的,其有一第一端15和一第二端16。在整个说明书中,术语“第一端”15是指色谱介质14上施加有试样的那一端,而术语“第二端”16是指相对的那一端。试样的原始流动方向是从色谱介质14的第一端15至第二端16。色谱介质14是一种适于用作对分析物和分析物-抗体结合体进行薄层色谱法测定的介质的材料构成,例如,硝化纤维素、尼龙、人造丝、纤维素、纸、或硅胶。如果需要,色谱介质14可以预处理或改型。典型的色谱介质14是半透明的,从而作为检测结果出现在其上的着色区可以从两侧观测到。
在一些应用中,较好的方式是在色谱介质14的顶部放置一第二柔性透明载体,以调节试样通过膜的流动,并防止迁移到膜的顶部上方。合适的柔性透明载体包括聚乙烯、乙烯树脂、聚脂薄膜、和玻璃纸。
当色谱测定装置10用于象夹心法免疫测定这样的测定时,色谱介质可以进一步包括一个大大小于色谱介质14的检测区17。这个检测区可以包含一个针对固定在其上而防止扩散的分析物的第二特异性结合体。第二特异性结合体可以以共价方式或非共价方式结合到色谱介质上。如果要测定的分析物是一个抗原或半抗原,那么第二特异性结合体可以是这个抗原或半抗原的一个抗体。另一方案是,分析物可以是一种抗体,而第二特异性结合体可以是一种能够被这个抗体所特异性结合的半抗原或抗原。
色谱介质14可以进一步包括一个大大小于色谱介质14的控制区18,并其与检测区17分离开。控制区18可以包括不扩散地固定在其上的分析物,以便结合在检测区17没有结合的加标记的抗体,形成一个三元“夹心”复合物。任何这样的抗体都被固定的分析物所结构,形成一个可检测区或可检测带。这对测定的操作和试剂的正确结合提供了一种检查,正如下文所述的那样。结合检测区17的第二特异性结合体和控制区18的分析物所用的方法是本领域公知的,不需要做进一步的说明。
另一方面,对于某些分析物来说,例如碳水化合物,将分析物稳定地固定在色谱介质14上也许很困难或者不可能。在这种情况下,控制区18可以包含一个对于加标记的抗分析物抗体具有特异性的抗体固定区。例如,如果分析物是链球菌A-特异性碳水化合物,加标记的抗体是针对链球菌A抗原具有特异性的家兔IgC,那么控制区18可以包含针对家兔IgC的山羊抗体。在这种情况下,为了在高分析物浓度下防止完全捕获检测区17中的加标记的抗分析物抗体,而产生加标记的抗分析物抗体从控制区18消失的结果,可能希望加入对于分析物不具有特异性的如标记的抗体,并且它与加标记的抗分析物抗体是不同的种类。这种抗体可以构成免疫学上中性的免疫球蛋白或一种在试样中未发现的一种分析物的抗体。控制区18则将包括抗体生物种类抗体或在试样中未发现的分析物。
这种装置可以有一些变型。在一种改型中,如上所述,试样制备区13可以进一步包含一个针对分析物、用一种可检测的标记予以标记的特异性结合体,加标记的特异性结合体的形式能够通过在试样制备区13中加入一种含水液体而溶解。含水液体可以是试样本身。加标记的特异性结合体可以冷冻干燥,或者可逆地沉淀析出,从而通过将试样加到试样制备区而使之溶解和移动。在这种变型中,不必在试样制备区13中加入一种检测试剂,因为通过将试样添加到试样制备区13中可以自动产生检测试剂。
在另一种变型中,与第二可对折构件上的色谱介质14的第一端15处于作用性接触的传导体25可以由一个具有有限容量的处于作用性接触的吸收体25a代替。吸收体25a设置在这样的位置上,即当在第一可对折构件11和第二可对折构件12被相对叠合起来时,它则与试样制备区13相接触,将试样施加到吸收体上。这在控制试样向色谱介质14中的流动,不使色谱介质14过载可能是有用的。
在这种变型中,吸收体25a可以包含一个针对分析物的。处于一种能够溶解的形式的加标记的特异性结合体,如上所述。在这种布置中,当第一可对折构件11和第二可对折构件12被相互对折叠合起来时,加标记的特异性结合体则被溶解,将试样施加到吸收体25a上。然后,试样和溶解的加标记的特异性结合体的组合物在其第一端15进入色谱介质14。
2.两构件型装置的具体实施例
a.在第二构件上有传导性连接件的装置
在本发明的一个两构件型装置的一个实施例中,第一可对折构件包括:
(1)一个试样制备区;和
(2)一个与试样制备区不连通的色谱介质。
第二可对折构件包括一传导性连接件。第一和第二可对折构件可以被相对叠合起来,使连接件在试样制备区和色谱介质之间建立一个连通;以便将试样施加到色谱介质。
这个实施例示于图2中。色谱测定装置40包括一第一可对折构件41和一第二可对折构件42。第一可对折构件包含一个试样制备区43和一个具有一第一端50和一第二端51的色谱介质44。色谱介质44有一个检测区45和一个控制区46。第二可对折构件42包含一个传导性连接件47。第一可对折构件41和第二可对折构件42由一个铰链48连接起来。第一可对折构件41和第二可对折构件42也包含诸如锁件52和53这样的接合件,一个垫子54包围着第一可对折构件41和第二可对折构件42。第二可对折构件42有一个可以观测色谱介质44的开孔49。
当第一可对折构件41和第二可对折构件42被相对叠合起来时,第一可对折构件41上的试样的制备区43和第二可对折构件42上的传导性连接件47接触,连接件47又与色谱介质44的第一端50接触,以将试样施加到色谱介质。
在图2中的装置的一些变型中,传导性连接件47可以包含一个针对分析物的、用一种可检测的标记予以标记的特异性结合体,加标记的特异性结合体处于能够通过加入一种含水液体而被溶解的形式。在这种变型中,将试样施加到试样制备区43。另一种方法是,试样制备区43可以用于加入针对分析物的、以液体形式的加标记的特异性结合体,试样本身加到传导性连接件47上。在又一种方案中,试样制备区43可以包含针对分析物的、可溶解的特异性结合体,试样也加到传导性连接件47上。
b.试样制备区在第一可对折构件上的装置
本发明的色谱测定装置的另一个实施例是一个在第一可对折构件上,亦即在其上有色谱介质的构件上包含一个试样制备区的装置。在该实施例中,典型的情况是,第二可对折构件包括一个点样器,它包含一个针对分析物的、呈可溶解形式的加标记的特异性结合体结合体。
在这个实施例中,当第一和第二可对折构件相互叠合后,点样器就与试样制备区接触,使加标记的特异性结合体溶解。
更好的情况是,第一可对折构件进一步包括一个传导体,且通过使试样制备区和色谱介质都与传导体有作用性接触,而实现试样制备区和色谱介质之间的作用性接触。
更好的情况是,第一可对折构件进一步包括一个与色谱介质的第二端有作用性接触的吸收体。
色谱介质最好是设计成上面所述的结构,其具有一检测区和一控制区。
测定装置的这个实施例示于图3中。色谱测定装置60具有一个第一可对折构件61和一第二可对折构件62。第一可对折构件61包含一个试样制备区63、一个与试样制备区63有作用性接触的传导体64,一个具有一第一端66和一第二端67的色谱介质65,和一个与色谱介质65的第二端67有作用性接触的吸收体68。色谱介质65包含一个检测区69和一个控制区70。第二可对折构件62包含一个点样器71,它最好有一个呈可溶解形式的加标记的特异性结合体。第一和第二可对折构件61和62由一个铰链72连接起来。第二可对折构件62包含一个窗口73,以观察至少一部分色谱介质65。第一和第二对折构件61和62具有诸如锁件74和75这样的接合件,一个垫子76包围住第一和第二可对折构件61和62。
在操作中,将一种试样施加到试样制备区63中。然后使第一和第二可对折构件61和62相互对折叠合在一起,使试样制备区63中的试样溶解点样器71的内含物,包含加标记的特异性结合体。然后通过试样制备区63和传导体64将试样制备区63和点样器71中的内含物施加到色谱介质65上。
C.吸收体在第二构件上的装置
在这个实施例的另一个方案中,可以将吸收体放置在第二可对折构件上,而不是放在第一可对折构件上。在这一方案中,当第一和第二可对折构件相互对折叠合后,吸收体则与色谱介质的第二端有作用性接触。这样可以考虑采用一个较大的吸收体,这在必须使用较大的试样时是所希望的,例如在检测只以低浓度下出现的一种分析物的情况下。
本实施例的这个替换方案示于图4中。色谱测定装置80包括一第一可对折构件81和一第二可对折构件82。第一可对折构件81包含试样制备区83,与试样制备区83有作用性接触的传导体83和具有一第一端86和一第二端87的色谱介质85,并带有检测区8和控制区89。第二可对折构件82包含点样器90和吸收体91,点样器90在第二可对折构件82上与吸收体91分隔开。第一和第二可对折构件81和82由一个铰链92连接。第二可对折构件82也有一个开孔93,用以观察至少一部分色谱介质85。第一和第二可对折构件81和82也包含如上所述的诸如锁件94和95的接合件和一个垫子96。
在使用中,试样被施加到试样制备区83,在该区中可以进行试样抽取或对试样的其它处理。然后试样通过流过传导体84而进入色谱介质85的第一端86,如上所述。当第一和第二可对折构件81和82相互对折叠合之后,点样器90与传导体84有作用性接触,以溶解点样器90中的加标记的特异性结合体,并将溶解的加标记的特异性结合体施加到传导体84上,然后施加到色谱介质85的第一端86,从而使溶解的加标记的特异性结合体进入色谱介质85中,同时也使吸收体91与色谱介质85的第二端87有作用性接触,而从色谱介质85中抽取液体。
d.试样制备区和吸收体在同一个可对折构件上的装置
本发明的色谱测定装置的另一个实施例是一个两构件装置,在该装置中,试样制备区和吸收体位于同一个可对折构件上。这在某些应用情况下具有优点表现在能够采用一个较大的吸收体,以便更快且更有效地从色谱介质的第二端抽取液体。
两构件色谱测定装置的这个实施例示于图5中。色谱装置100具有由一个铰链103连接在一起的一第一可对折构件101和一第二可对折构件102。第一可对折构件101包含一个具有一第一端105和一第二端106的色谱介质104,和一个与色谱介质104的第一端105有作用性接触的传导体107。色谱介质105一个检测区108和有选择地包含一个控制区109。
第二可对折构件102包含一个用以接收要测定的试样的试样制备区110和一个与试样制备区110间隔开的吸收体111。试样制备区110可以包含一个用于分析物的、呈可溶解形式的加标记的特异性结合体。第二可对折构件102上有一个开孔112,以观察色谱介质。第一和第二可对折构件101和102有诸如锁件113和114这样的接合件和一个垫子115,如上所述。
当第一和第二可对折构件101和102相互对折叠合后,试样制备区110与传导体107有作用性接触,将试样施加到传导体107,然后施加到色谱介质104的第一端105。吸收体111与色谱介质104的第二端106有作用性接触,以从色谱介质104的第二端106抽取液体。在其它方面,该装置的设计结构和操作都类似于上面图4中所描述的装置。
e.在不同的可对折构件上设有两个检测点样垫的装置
本发明的两构件测定装置的又一个实施例包含有在不同的可对折构件上的两上单独的检测器点样垫。当一种加标记的抗体只能在稀释形式下获得,且将其浓缩会使之变性或不能激活时,就希望采用大体积的加标记的特异性结合体,此时,装置采取这种布置结构就特别有用。
两构件的色谱测定装置的这个实施例示于图6中。色谱测定装置120包括有由一个铰链133连接起来的一第一可对折构件121和一第二可对折构件122。第一可对折构件121包含一个具有一第一端125和一第二端126的色谱介质124。色谱介质124包含一个检测区127和有选择地包含一个控制区128。
第一可对折构件121也有一个与色谱介质124的第一端125有作用性接触的第一检测器点样垫129。第一检测器点样垫129包含一个用于分析物的第一特异性结合体,第一特异性结合体为一种通过在第一检测器点样垫129中加入一种含水液体能够被溶解的形式。典型地,第一特异性结合体用一种可检测的标记予以标记。第一可对折构件121也有一个与第一检测器点样垫129有作用性接触的传导体130,从而第一检测器点样垫129将传导体130与色谱介质124的第一端125桥接起来。第一可对折构件121也有一个与色谱介质124的第二端126有作用性接触的吸收体131。
第二可对折构件122包含一个用以接收要测定的试样的试样制备区132。第二可对折构件122也有一个与试样制备区132有作用性接触的第二检测器点样垫133,且试样制备区132放置在第二检测器点样垫133的上面。试样制备区132和第二检测器点样垫133可以用一紧固件或粘胶剂保持在一起。第二检测器点样垫133的和试样制备区132设置在这样的位置上,即使得向试样制备区132施加的试样在进入第二检测器点样垫133之前必须通过试样制备区132。第二检测器点样垫133包含一个分析物的第二特异性结合体,第二特异性结合体为一种通过在试样制备区132中加入一种试样能够被溶解的形式。第二检测器点样垫133设置在这样的位置上,即使得施加在试样制备区132的试样能溶解第二特异性结合体,从而试样制备区132包含一种由试样和第二特异性结合体构成的混合物。
第二特异性结合体由一种可检测的标记物予以标记。更好的是,第一和第二特异性结合体是相同的,标记在第一和第二特异性结合体上的可检测的标记是相同的。
第二可对折构件122中也有一个用以观测至少一部分色谱介质124的开孔134,色谱介质包含检测区127和(如果有的话)控制区128。第一和第二可对折构件121和122也有诸如锁件135和136这样的接合件和一个垫子137,如上面针对基本的两构件型装置所述的那样。
当第一和第二可对折构件121和122相互对折叠合后,试样制备区132则与传导体130进行接触,将试样和第二特异性结合体施加到传导体130上,然后通过第一检测器点样垫129施加到色谱介质124的第一端125。因此,试样在施加到色谱介质124的第一端125进行色谱过程之前,依次地接触第二特异性结合体,然后接触第一特异性结合体这样导致较大体积的加标记的特异性结合体与试样接触,增加了测定的敏感性。
f.在同一个可对折构件上有两个分开的点样器的装置
本发明的色谱测定装置的又一个实施例包含有在同一个可对折构件上的两个分开的点样器。这两个点样器并不处在有作用性接触的状态,直到两个构件相互对折叠合后由在相对的构件上的一个传导体连接为止。
色谱测定装置的这个实施例示于图7中。色谱测定装置140包括一第一可对折构件141和一第二可对折构件142。第一可对折构件141包含有一个具有一第一端144和一第二端145的色谱介质143、一个与第一端144有作用性接触的传导体146、和一个与色谱介质143的第二端145有作用性接触的吸收体147。色谱介质143包含一个检测区148和一个控制区149。第二可对折构件142包括有一第一点样器(试样点样垫)150和一第二点样器(检测器点样垫)151。在第一和第二可对折构件141和142相互对折叠合之前,第一和第二点样器150和151并不处在有作用性接触的状态,当第一和第二可对折构件141和142相互对折叠合之后,第一点样器150与传导体146有作用性接触,而第二点样器151与传导体146和色谱介质143的第一端144有作用性接触。重叠的范围典型地为几个毫米,亦即足以保证液体传送。这就导致由传导体146将第一和第二点样器150和151桥接起来,从而第一和第二点样器150和151的内含物被施加到色谱介质143上。第一和第二可对折构件141和142由一个铰链152连接起来。第二可对折构件142上有一个用以观测色谱介质143的窗口153。第一和第二可对折构件141和142也有诸如锁件154和155这样的接合件和一个垫子156。
第一点样器150可以包括一个试样点样垫,而第二点样器151可以包括一个检测器点样垫,其上可以施加检测试剂。当第一和第二可对折构件141和142相互对折叠合之后,试样点样垫和检测器点样垫的内含物经传导体146被施加到色谱介质143上。
更好的方式是,第二点样器151(检测器点样垫)包含一个用于分析物的特异性结合体,该特异性结合体标记有一种可检测的标记物并且处于一种通过在第二点样器151中加入一种含水液体能够被溶解的形式。典型地,含水液体是试样本身,当第一和第二可对折构件141和142相互对折叠合后,该含水液体使加标记的特异性结合体溶解。在某些测定中,可能希望在检测器点样垫加入一种单独的重新构成的含水液体。另一种方案是,可以将加标记的特异性结合体的液体形式下施加到第二点样器151上。
g.在第二可对折构件上带有两个点样器和一个吸收体的装置
在这个实施例的又一种变型中,可以将吸收体从第一可对折构件(亦即含有色谱介质的可对折构件)上移置到第二可对折构件(亦即含有第一和第二点样器的可对折构件)上。这样可以使用较大的试样,这在检测在低浓度情况下存在的分析物时可能是所希望的。
这个变型示于图8中。色谱测定装置160有一第一可对折构件162和一第二可对折构件164。第一可对折构件162包含一个具有一第一端168和一第二端170的色谱介质166和一个与色谱介质166的第一端168有作用性接触的传导体172。色谱介质166包含有一个检测区174和一个控制区176。第二可对折构件164包含有一个第一点样器(试样点样垫)178和一第二点样器(检测器点样垫)180。第一点样器178和第二点样器180并不处于有作用性接触的状态,直到第一和第二可对折构件162和164被相互对折叠合后而将它们桥接起来为止,如上面在图7所示的测定装置中所述的那样。第二可对折构件164也包含一个吸收体182,吸收体182与第一和第二点样器178和180分离开。当第一和第二可对折构件162和164相互对折叠合后,由传导体172将第一和第二点样器178和180桥接起来,从而第一和第二点样器178和180的内含物被施加到色谱介质166上。同时,吸收体182与色谱介质166的第二端170进入有作用性接触,以从色谱介质166中吸收液体。第一和第二可对折构件162和164由一个铰链184连接起来。第二可对折构件164包含一个窗口186,用以观察色谱介质166。第一和第二可对折构件162和164也包含象锁件185和187这样的接合件和一个垫子188。
h.在传导体和色谱介质之间有间隙或中断部分的装置
这种装置的又一种变型包括在传导体和色谱介质之间有一个间隙或中断部分,从而液体流动的路线是从第一点样器,通过传导体,再通过第二点样器,最后通过色谱介质。
装置的这种变型示于图9中。色谱测定装置190具有一第一可对折构件191和一第二可对折构件192。第一可对折构件191包含一个具有一第一端194和一第二端195的色谱介质193,一个在色谱装置190处于打开位置时而不与色谱介质193的第一端194有作用性接触的传导体196,和一个与色谱介质193的第二端195有作用性接触的吸收体197。色谱介质193含有一个检测区198和一个控制区199。第二可对折构件192含有一第一点样器(试样点样垫)200和一第二点样器(检测器点样垫)201。在第一和第二可对折构件191和192相互对折叠合之前,第一和第二点样器200和201并不处在有作用性接触的状态。当通过闭合连接第一和第二可对折构件191和192的铰链203。使第一和第二可对折构件191和192相互对折叠合后,第一和第二点样器200和201由传导体196桥接起来并且第二点样器201接触色谱介质193。因此,液体流动的路线是从第一点样器200,通过传导体196,然后通过第二点样器201,再进入色谱介质193。第二可对折构件192上设有一个窗口193,用以观察色谱介质193。第一和第二可对折构件191和192也有象锁件204和205这样的接合件和一个垫子206,如上所述。
i.在与色谱介质相同的可对折构件上设有用于加标记的特异性结合体的垫的装置。
本发明的色谱测定装置的又一个实施例是一个含有一个位于与色谱介质同一个可对折构件上的、用于加标记的特异性结合体的垫的两构件装置。在这个装置中,试样点样器设置在另一个可对折构件上。
本发明的色谱测定装置的这个实施例示于图10A中。色谱测定装置210具有一第一可对折构件212和一第二可对折构件214。第一可对折构件212包含一个具有一第一端218和一第二端220的色谱介质216。色谱介质具有一个检测区222和有选择地包含一个控制区224,如上面对适合于夹心法免疫测定所用的测定装置的其它变型的描述的那样。第一可对折构件212也包含有一个与色谱介质216的第一端218有作用性接触的传导体226和一个与色谱介质216的第二端220有作用性接触的吸收体228。第一可对折构件212也有一个与传导体226直接接触的检测器点样垫230,并且处于与色谱介质216的第一端218间接接触的位置。第二可对折构件214有一个试样点样垫232。第一和第二可对折构件212和214由一个铰链234来连接。当第一和第二可对折构件212和214相互对折叠合后,试样点样垫232则与检测器点样垫230进行接触。第二可对折构件214包含一个窗口236,用以观察色谱介质216。第一和第二可对折构件212和214有象锁件233和235这样的接合件和一个密封垫237,如前所述。
装置210的一个截面后视图示于图10B中。图10B中所示的截面是沿图10A中的线10B截取的,它位于色谱介质216和铰链234之间,朝对着铰链234缘边方向看。图10B示出了相互对折叠合后的第一和第二可对折构件212和214。图中可见试样点样垫232与检测器点样垫230相接触。检测器点样垫230接触传导体226,传导体226又接触色谱介质216的第一端218。图中示出了色谱介质216的检测区222和控制区224。色谱介质216更接近于控制区224的第二端220接触吸收体228。
将第一和第二可对折构件212和214相互对折叠合起来,使试样点样垫232将要测试的试样施加到检测点样垫230上,由此通过传导体226将试样施加到色谱介质的第一端218上。
更好的情况是,检测器点样垫230含有一个针对分析物的第一特异性结合体,它处于能够通过在检测器点样垫230上加入一种含水液体而被溶解的形式,并且该第一特异性结合体标记有一种可检测的标记物。
最好的是,在将试样施加到试样点样垫232上之后,点样垫232的内含物包括一种含水液体,而加到检测器点样垫230上的含水液体包括试样点样器的内含物。在这种布置下,不需要用额外的液体来溶解加标记的特异性结合体。
在这种装置的一个变型中,吸收体不是设置在第一可对折构件上,而是设在第二可对折构件上。吸收体与同样设置在第二可对折构件上的试样点样垫分离开,在第一和第二可对折构件相互对折叠合后与色谱介质的第二端有作用性接触,如上面图5中所示。
j.检测器点样垫直接接触色谱介质的第一端的装置
这种装置的又一种变型是省去了检测器点样垫和色谱介质之间的传导体,从而检测器点样垫为直接接触色谱介质的第一端。在这种变型中,当第一和第二可对折构件相互对折叠合后,除了检测器点样垫与色谱介质的第一端直接相邻的区域外,检测器点样垫和试样点样垫处于接触状态。在检测器点样垫的这个区域中内有一个小的间隙或错位,从而试样不能直接从试样点样垫流动到色谱介质。一般这个间隙或错位的大小约为0.5~2毫米,更典型地,约为0.5~1毫米。
这种变型尤其适用于利用加标记的抗血红蛋白抗体检测粪便隐血,可以检测的血红蛋白的浓度相应于每100g粪便17毫升血(每克粪便含13毫克血红蛋白)之多,而不会由于高剂量“诱惑”(hook)效应产生假的阴性结果。
这个变型示于图11A中。色谱测定装置250具有一第一可对折构件252和一第二可对折构件254。第一可对折构件252包含一个具有一第一端258和一第二端260的色谱介质256。色谱介质256有一个检测区262和一个控制区264。第一可对折构件252也有一个与色谱介质256的第二端260有作用性接触的吸收体266,第一可对折构件252还有一个与色谱介质256的第一端258直接接触的检测器点样垫268。第二可对折构件254有一个试样点样垫270。第一和第二可对折构件252和254由一个铰链272连接起来。当第一和第二可对折构件252和254相互对折叠合后,除了在与色谱介质256的第一端258相接触的检则器点样垫268的端部处的一个窄间隙或错位274以外,试样点样垫270接触检测器点样垫268。这个间隙274防止施加到试样点样垫270上的试样直接地流入色谱介质266。第二可对折构件254上有一个窗口276,用以观察色谱介质256。第一和第二可对折构件252和254有象锁件278和280这样的接合件和一个密封垫282,如前所述。
图11B中示出了沿图11A所示装置250中的线11A截取的一个截面后视图。图11B所示的这个截面图是从图11A中色谱介质256和铰链272之间朝对着铰链272的边缘方向看所截取的视图。图11B示出了处于相互对折叠合状态下的第一可对折构件252和第一可对折构件254,铰链272处于闭合位置。如图所示,除了在最靠近色谱介质256的检测器点样垫268的端部处有一个小间隙274外,试样点样垫270与检测器点样垫268处于相接触状态。检测器点样垫268直接接触色谱介质256的第一端258。图中示出了色谱介质256的检测区262和控制区264。色谱介质256的较为靠近的控制区264的第二端260与吸收体266相接触。
k.在第二可对折构件上含有点样器和吸收体的双向装置
本发明的色谱测定装置的又一个实施例包括一种能够实施双向色谱法的装置。
色谱测定装置的这个实施例示于图12A中。测定装置300具有一第一可对折构件302和一第二可对折构件304。第一可对折构件302有一个具有一第一端308和一第二端310的色谱介质306,第一可对折构件302也有一个与色谱介质306的第一端308有作用性接触的第一点样器312。色谱介质306也包含一个检测器314,和有选择地包含一个控制区316,它位于检测区314和色谱介质306的第二端310之间。检测区314和控制区316的构成与前面对适用于夹心法免疫测定的装置的其它实施例讨论的情况一样。第二可对折构件304包含一个吸收体318,该吸收体可以是一个吸收垫,和一个第二点样器320。第一和第二可对折构件302和304由一个铰链322连接起来。第二可对折构件304包含一个窗口324,用以观察色谱介质306。第一和第二可对折构件302和304包含有接合件323和325,和一个密封垫326,如上所述。
当铰链322被闭合时,装置300呈现如图12B中的一个顶视图所示。从窗口324可以看见包含检测区314和控制区(如果有的话)316的色谱介质306。
在装置的这个实施例中,将一第一液体加到第一点样器312上可使第一液体被施加到色谱介质306的第一端308上。然后将第一和第二可对折构件302和304相互对折叠合,使得第二点样器320与色谱介质306的第二端310有作用性接触,从而将一第二液体施加到色谱介质306的第二端310上,同时也使吸收体318与第一点样器312发生有作用性接触,从而通过第一点样器312从色谱介质306中抽吸液体,而使流动反向。在操作这个装置时,试样被施加到第一点样器312上,而一种加标记的特异性结合体的一种溶液被施加到第二点样器320上。然后试样通过色谱介质306从第一端308向第二端310移动,从而试样中存在的任何分析物都被结合到检测区314处的固定的抗体上。当将第一和第二可对折构件302和304相互对折叠合后,加标记的特异性结合体则被施加到色谱介质306上,并通过色谱介质306从第二端310移动到第一端308。然后加标记的特异性结合体与结合在检测区314处的固定抗体上的任何分析物相结合,产生一种可检测的三元复合物。加标记的特异性结合体也与控制区316处的固定分析物或模拟物相结合,提供正确实施测定的一种指示。
1.含有两个点样器和一个传导器的双向装置
本发明的色谱测定装置的又一个实施例是一种适用于双向色谱法的装置,之包含有一个使流动反向的吸收体和一个与色谱介质有作用性接触的试剂垫。
色谱测定装置的这个实施例示于图13A中。测定装置340包括一第一可对折构件342和一第二可对折构件344。第一可对折构件342包括一个具有一第一端348和一第二端350的色谱介质346。与色谱介质346的第一端348相邻并且有作用性接触的是一第一点样器352。与色谱介质346的第二端350相邻并且有作用性接触的是一个传导体354。色谱介质346包含一个检测区356,和有选择地包含一个控制区358。第二可对折构件344包括一个吸收体360和一第二点样器362。第一和第二可对折构件342和344由一个铰链364连接起来。第二可对折构件344上有一个窗口366,用以观察色谱介质346。第一和第二可对折构件342和344包含接合件365和369,和一个密封垫368,如上所述。
当将第一和第二可对折构件342和344相互对折叠合后,则使吸收体360与第一点样器352有作用性接触,而使第二点样器362与传导体354有作用性接触,由此使流动反向,此时,包含检测区356和控制区(如果存在的话)358的色谱介质346的这部分在第一和第二可对折构件342和344相互对折叠合起来时可从第二可对折构件344中的窗口366观察到。
图13B示出了在第一和第二可对折构件342和344相互对折叠合后装置340的一个顶视图,此时通过第二可对折构件344中的窗口366可以看到检测区356和控制区358。
在这个装置中,第一点样器352可以包括一个试样点样垫,要测定的试样被施加到该试样点样垫上;第二点样器362可以包括一个其上施加缓冲剂的缓冲剂点样垫。第一点样器352(试样点样垫)可以包含至少一种试剂,用于在试样被施加到色谱介质上之前对试样进行处理,如前所述。第二点样器362(缓冲剂点样垫)典型地包含一种用于分析物的特异性结合体,该结合体处于能够通过加一种含水液体被溶解的形式,如前所述。
第一点样器352(试样点样垫)最好进一步包括一种惰性染料,从而可以用肉眼监测试样在色谱介质346中的流动。更好的是,惰性染料相对可检测标记物的颜色是一种对比色,例如,如果可检测标记物是粉红色胶态金,则惰性染料可以是兰色。通过观察惰性染料来监测试样的迁移。当试样迁移了一段足够长的距离后,例如为色谱介质346的长度的三分之二或四分之三之后,将第一和第二可对折构件342和344相互对折叠合后,使吸收体360与第一点样器352相接触。这就使试样通过色谱介质346的流动反向,从而能够在检测区356处捕获额外的分析物。此外也使第二点样器362与传导体354接触,而将含有已溶解的用于分析物的加标记特异性结合体的缓冲剂溶液被施加到色谱介质346上。缓冲剂溶液通过色谱介质346从第二端350向第一端348迁移。当它到达检测区356时,用于分析物的加标记的特异性结合体则结合到已经结合在检测区356上的分析物上。然后如前述那样对分析物实施检测和/或测定。
用于在将试样作为第一液体施加到第一点样器352时,第一和第二可对折构件342和344没有接触,因此有可能或者先将试样施加到第一点样器352上,或者先将缓冲剂施加到第二点样器362,以重新构造加标记的特异性结合体。
这种双向装置的一种变型是用一个具有有限容量的第一吸收体354a代替第一可对折构件342上的传导体354。在第二可对折构件344上的吸收体360则为一第二吸收体。第一可对折构件342上的有限容量的吸收体354a具有这样的特性,即在第二点样器362(其含有一种可溶解的加标记的特异性结合体)被置于与该吸收体354a有作用性接触,和第二吸收体360被置于与第一点样器352有作用性接触时,通过它可以将液体抽回。
m.检测器点样垫在第一构件上的装置
本发明的一个两构件色谱测定装置的又一个实施例有一个位于第一可对折构件上的检测器点样垫和一个位于第二可对折构件上的试样制备区。在这个装置中,检测器点样垫设置成与色谱介质的第一端有作用性接触的状态。检测器点样垫最好含有一种针对分析物的以能够通过向检测器点样垫加入一种含水液体而溶解的形式加标记的特异性结合体。该装置进二步包括一个与检测器点样垫有作用性接触并与色谱介质的第一端间接接触的传导体以及一个与色谱介质的第二端有作用性接触的吸收体。
在操作装置的这个实施例时,先将试样施加到第二可对折构件上的试样制备区,然后将第一和第二可对折构件相互对折叠合。这样试样制备区的内含物被施加到传导体上,然后通过检测器点样垫施加到色谱介质的第一端上。当试样到达检测器点样垫时,就使检测器点样垫的内含物溶解。当检测器点样垫的内含物含有一种针对分析物的特异性结合体时,试样从检测器点样垫中通过导致特异性结合体结合到存在于试样中的任何分析物上。
装置的这个实施例示于图14中。色谱测定装置380包括一第一可对折构件382和一第二可对折构件384。第一可对折构件382包含一个具有一第一端388和一第二端390的色谱介质386。第一可对折构件382也包含一个与色谱介质386的第一端388有作用性接触的检测器点样垫392、一个与检测器点样垫392有作用性接触的并和色谱介质386的第一端388间接接触的传导体394,一个与色谱介质386的一第二端390有作用性接触的吸收体396。色谱介质386包含一个检测区398和一个控制区400。第二可对折构件384包含一个试样制备区403。第一和第二可对折构件382和384由一个铰链404连接起来。第二可对折构件384中有一个的开口406。用以观测至少一部分色谱介质386。第一和第二可对折构件有接合件405和407,和一个密封垫408。
这个实施例的一个变形包含以能够溶解的形式设置在第一可对折构件382上也设置在第二可对折构件384上的一种针对分析物的特异性结合体。当可溶解的特异性结合体设置在第二可对折构件384上时,最好不将它直接设置在试样制备402中,而在设置在包围试样制备区402的一个区域403中,使得试样首先通过试样制备区402,然后移动到包围着试样制备区402的区域403中,溶解特异性结合体。例如,试样制备区402可以包含一张经合适处理的过滤纸,用一种胶或固定件固定在第二可对折构件384的表面上。这样在试样接触可溶解的特异性结合体之前就可以处理试样,例如,调节pH值,溶解完整的细胞,和/或除去颗粒物。这个实施例的这种变形可以提供一个较宽的动态范围,并且在可获得的抗体具有低的亲合力或者要检测低浓度的分析物时,会是有用的。
n.带有提供洗涤的两扇区点样器的装置
本发明的两构件测定装置的又一个实施例具有一个两扇区点样器,它在试样和加标记的特异性结合体混合物已经通过色谱介质之后,对没有与加标记的特异性结合体进行反应的试样提供洗涤。这个实施例的优点在于它提供了一个更清楚的背景,更容易读出微弱的阳性结果。
在该实施例中,第一可对折构件包含一个具有一第一端和一第二端的色谱介质,一个与色谱介质的第一端有作用性接触的传导体和一个与色谱介质的第二端有作用性接触的吸收体。第二可对折构件包含一个点样器,它被分为两个扇区;包含一个用于分析物的以可溶解形式的加标记的特异性结合体的第一扇区,和一个没有加标记的特异性结合体的第二扇区,当第一和第二可对折构件相互对折叠合后,使点样器的第一扇区而不是第二扇区与传导体直接接触,从而将点样器的第一扇区的内含物施加到传导体上,然后施加到色谱介质的第一端上。第二扇区与传导体处于间接接触,此时,第二扇区的内含物流过第一扇区,然后到达传导体。这样,在将点样器的第一扇区的内含物施加到传导体之后,接着将点样器的第二扇区的内含物施加到传导体。第二扇区的内含物(包含试样,但没有加标记的特异性结合体)用于从色谱介质中洗掉未结合的加标记的特异性结合体,从而减少在色谱介质中可看见的标记物的背景,而改善测定装置的读出性。这一点对于弱阳性测定来说特别有利。
测定装置的这个实施例示于图15中。色谱测定装置420包括一第一可对折构件422和一第二可对折构件424。第一可对折构件422包含一个具有一第一端428和一第二端430的色谱介质426,一个与色谱介质426的第一端428有作用性接触的传导体432、一个与色谱介质426的第二端430有作用性接触的吸收体434。第一可对折构件424有一个被分成两个扇区的点样器436;当第一和第二可对折构件422和424相互对折叠合后与传导体432直接接触的为第一扇区438,和当第一和第二可对折构件422和424相互对折叠合后与传导体432间接接触的为第二扇区440。色谱介质426包含一个检测区442和一个控制区444。第一和第二可对折构件422和424由一个铰链446连接起来。第二可对折构件424中有一个窗口448,用以观测至少一部分色谱介质426。第一和第二可对折构件422和424也有接合件423和425,和一个密封垫427,如上所述。
B.带有盖子的两构件型装置
本发明的色谱测定装置的又一个实施例是一个带有一个盖子的两构件型装置。
测定装置的这个实施例示于图16a中。色谱测定装置460包括一第一可对折构件462、一第二可对折构件464,和一个盖子466。第二可对折构件464由一第一铰链468铰接在第一可对折构件462的一侧边上,盖子466由一第二铰链470铰接在第一可对折构件462的相对的侧边上。第一可对折构件462包含一个具有一第一端474和一第二端476的色谱介质472。与色谱介质472的第一端474相邻且有作用性接触地设置在一个凹陷480中的是一第一点样器或试样垫478。第一点样器478可以包含一个试样制备区,该试样制备区可以包含至少一种用于在试样施加到色谱介质之前对试样进行处理的试剂,如上所述。第一点样器478也可以包含一种惰性染料,以指示色谱法的进程,如上所述。一第一吸收体482与色谱介质472的第二端476相邻且有作用性接触。色谱介质472包含一个检测区484和一个控制区486,并且有选择地用一条限制线588标记。限制线488也可以有选择地标记在第一可对折构件462上。第二可对折上464包括一第一点样器490,它典型地包含一种用于分析物的加标记的特异性结合体,和一第二吸收体492。盖子466有一第一开孔494。更好的是,第二可对折构件464有一第二开孔496。在这个装置中,第二可对折构件464和盖子466也包含接合件491和493。装置460用一个密封垫495包围住,如上所述。盖子466也可以有一个将其保持到位的接合件497。
图16B示出了这个装置460的一个顶视图,此时,第二可对折构件464折叠在第一可对折构件462之上,而盖子466折叠在第一可对折构件464的上面。通过盖子466的第一开孔494和第二可对折构件464的第二开孔496可以看到一部分色谱介质472,该色谱介质包含检测区484和控制区486。
在操作这个装置时,向第一点样器478加入一第一液体则使第一液体被施加到色谱介质472的第一端474。典型地,第一液体是一种可以包含一种分析物的试样。
在这个装置中,在第一可对折构件462中的凹陷480的作用是使第二吸收体492定位,从而可以使之至少部分地与色谱介质472直接接触,以便除去过多的试样,同时不使第一点样器478阻碍这种接触。
在使用中,将试样施加到第一点样器478上,从而色谱分析可以在色谱介质472中从第一端474行进到第二端476。当染料到达限制线488时,将第一和第二可对折构件462和464相互对折叠合,这就使第二点样器490与第一吸收体482有作用性接触,从而将第二液体施加到色谱介质472的第二端476,同时也使第二吸收体492与第一点样器478有作用性接触,从而经第一点样器478从色谱介质472中抽取液体。这使得色谱流反向,并将加标记的特异性结合体通过色谱介质472从第二端476向第一端474回抽。因此,这个装置对于双向色谱法是有用的。
盖子466可以折叠在第二可对折构件464的上面,以便将第二可对折构件464更牢固地锁定和保持在第一可对折构件462上。这样在装置使用完后就能作为一个医学记录更方便地储藏装置。
C.三构件型装置
本发明的色谱测定装置的又一个实施例是一种应用双向色谱法的三构件型装置。
三构件测定装置的这个实施例示于图17A中。测定装置520包括一第一可对折构件522、一第二可对折构件524,和一第三可对折构件526。第二可对折构件524由一第一铰链528铰接在第一可对折构件522的一侧边上,第三可对折构件526由一第二铰链530铰接在第一可对折构件522的相对的侧边上。第一可对折构件522包含一个具有一第一端534和一第二端536的色谱介质532。色谱介质532包含一个检测区538和一个控制区540。与色谱介质532的第一端534有作用性接触的是一第一传导体542,而与色谱介质532的第二端536有作用性接触的是一第二传导体544。第二可对折构件24可以包含一第一吸收体546和一第一点样器548,用于试样施加。典型地,第一点样器548包含一种用于分析物的以通过向第一点样器548中加入一种含水试样能够溶解的形式的特异性结合体。在第二可对折构件524中开有一第一开孔550,用以观测至少一部分色谱介质532。第一开孔550位于第一吸收体546和第一点样器548之间。第三可对折构件526包括一个用于一个加标记的次特异性结合体的第二点样器552,和一第二吸收体554。在第三可对折构件526中开有一第二开孔556,用以观测至少一部分色谱介质532。第二开孔556位于第二吸收体554和第二点样器552之间。当装置520闭合时,第二可对折构件524折叠在第一可对折构件522之上,而第三可对折构件526折叠在第一可对折构件522的上面,通过第一开孔550和第二开孔556(见图17B)至少可以看见一部分色谱介质532。第二和第三可对折构件524和526有接合件551和555,将它们保持在一起。一条柔性凸起或密封垫557包围着这些构件的边缘,而将试剂和试样保持在装置520内。接合件和一条凸起或密封垫的一种类似布置用于其它的三构件型装置,如下文所述。
在这个装置中,将第一和第二可对折构件522和524相互对折叠合使得第一吸收体546与第二传导体544有作用性接触和使得第一点样器548与第一传导体542有作用性接触,以将液体施加到色谱介质532上,从而通过至少一部分色谱介质532(包括检测区538和控制区540)抽吸施加到第一点样器548上的第一液体。
然后将第一和第二可对折构件522和524从相对对折叠合位置上拉开,而将第一和第三可对折构件522和526相互对折叠合。这使得第二传导体554与第一传导体542进入有作用性接触,以从色谱介质532中抽吸液体,并且使得第二点样器552与第二传导体544进入有作用性接触,而将液体施加到色谱介质532上。这就使流动反向,从而至少通过一部分色谱介质抽吸施加到第二点样器552上的一第二液体,经过这部分色谱介质已经沿着经过色谱介质532抽吸第一液体的方向的相反方向抽吸第一液体。第一、第二和第三可对折构件522,524和526具有这样的结构,即当第三可对折构件526与第一可对折构件522相互对折叠合后,可以将第二可对折构件524折叠在第一和第三可对折构件522和526的上面,以形成一个盖子。
在使用这种装置进行一种血清学测定时,在第二吸收体554和第一传导体542之间的稳定的压力是很重要的;以保证在加标记的次特异性结合体的前沿之前从色谱介质532中抽吸非特异性免疫球蛋白,或者保证在加标记的特异性抗分析物的前沿之前抽吸自由的分析物。如果抗免疫球蛋白标记和非特异性免疫球蛋白之间发生混合,那么非特异性免疫球蛋白使投免疫球蛋白标记(结合物)中性化,从而难以或不能标记被特异性捕获的免疫球蛋白。该装置的第三可对折构件526有助于维持所施加的压力的一致性,从而可靠地实现这种功能。这是本发明的测定装置的优点之一。
第一特异性结合体可以直接标记一个可检测标记物。另一种方式是采用间接标记第一特异性结合体。在间接标记的情况下,第一特异性结合体没有被加标记,而是通过利用第二点样器加入一个加标记的次特异性结合体,使该次特异性结合体与第一特异性结合体相结合来检测第一特异性结合体。间接标记方式在测试贾第鞭毛虫或其它抗原时尤其有用,因为用于这些抗原的在市场上能购得的抗体都很难被直接标记。当第一特异性结合体未被直接标记时,第二点样器552最好含有一种用于第一特异性结合体的加标记的次特异性结合体,如下面第III节中所述。
三构件装置的又一个实施例采用位于第三可对折构件上的一个吸收体,其设置成可以除去整个色谱介质中和与其有作用性接触的构件中的液体。其目的是除去可能产生一种背景颜色因而降低敏感性的多过试样。
这个实施例示于图18中。测定装置560有一第一、一第二和一第三可对折构件561,562和563。第二可对折构件562由一个第一铰链564铰接在第一可对折构件561的一侧边上,第三可对折构件563由一第二铰链565铰接在第一可对折构件561的另一侧边上。第一可对折构件561有一个具有一第一端567和一第二端568的色谱介质566。与色谱介质566的第一端567相邻并有作用性接触的是一第一点样器569。与色谱介质566的第二端568相邻并有作用性接触的是一个传导体570。色谱介质包含一个检测区571并有选择地包含一个控制区572。第二可对折构件562包括一第一吸收体573和一第二点样器574,典型地,第二点样器574含有一种针对分析物的以可溶解形式的加标记特异性结合体,第三可对折构件563包括一第二吸收体575,它基本上沿色谱介质566的长度延伸,以便在将第三可对折构件563与第一可对折构件561相互对折叠合后从色谱介质566、第一点样器569和传导体570中吸收液体。第一可对折构件561有一位于色谱介质后面的开孔576,用于在第一可对折构件561的背面处观察至少一部分色谱介质566。第二和第三可对折构件562和563也有如前所述的接合件577和579,和一个密封垫580。
在使用时,将要测试的试样施加到第一点样器569上,并将一种缓中剂溶液施加到第二点样器574。然后让试样流过包含检测区571和控制区572的色谱介质566。然后将第一和第二可对折构件561和562相互对折叠合起来,使第二点样器574接触第一点样器569,而第一吸收体573接触在色谱介质566的第二端568处的传导体570。这样就造成已溶解的原先位于第二点样器574中的加标记的特异性结合体流过色谱介质。在试样和已溶解的特异性结合体完全流过色谱介质566之后,将第三可对折构件563与第一可对折构件561相互对折叠合,从而第二吸收体575可以移去色谱介质566、第一点样器569、和传导体570中的液体。然后将第二可对折构件562折叠到第三可对折构件563的上面,并通过位于色谱介质566后面的开孔576观察包含检测区576和控制区568的色谱介质566。
D.多重型装置
本发明的色谱测定装置的又一种实施例是一种能够同时实施多重测定的多重型装置,这些测定可以对同一分析物实施,也可以对不同的分析物实施。一般地,通过在第一和第二可对折构件上,必要时也在第三可对折构件上设置多重色谱介质,试样制备区、点样器、传导体、吸收体和其它所需要的组分(元素),上面所述装置的所有型式都能适用于多重应用。
1.基本的多重型装置
本发明的一种型式的多重型测定装置示于图19中。测定装置590有一第一可对折构件592和一第二可对折构件594。第二可对折构件594由一个铰链596铰接在第一可对折构件592上。第一可对折构件592包括多个色谱介质598,每个色谱介质598具有一第一端600和一第二端602,和有一个检测区604及一个控制区606。每个色谱介质598的第二端602与一个吸收体608有作用性接触,以促使通过色谱介质的液体流动。每个色谱介质598都有一个单独的吸收体608。第二可对折构件594包含多个试样制备区610,每一个对应于一个色谱介质598。典型的情况是,每个试样制备区610含有用于要试验的分析物的以通过向试样制备区610加入一种液体试样而能够溶解的形式的加标记的特异性结合体。另一种方案是,在向试样制备区610中加入试样之前或之后,可以将液体形式的加标记的特异性结合体加到试样制备区610。将第一和第二可对折构件592和594相互对折叠合,使每个试样制备区610在第一端600处接触对应的色谱介质598。第二可对折构件594包含多个开孔612,每一个开孔612对应于一个色谱介质598。第一和第二可对折构件592和594包含如上所述的接合件614和616,和一个密封垫618。
这种多重型装置可以包含2~12或更多个试样制备区和色谱介质,这取决于使用该装置进行的测定情况。典型地,装置包含2~5个单独的试样制备区和色谱介质。
该装置的这个实施例可以用于利用同一种试样的不同分量试样来测定一些不同的分析物,或者用一些不同的试样测定同一种分析物,这后一种情况在以下的情况中进行的测定是极其有用的,即为了确定所注意的分析物,必须测定在不同时刻从同一病人身上取得的试样,例如粪便中的隐血;粪便隐血的存在通常由一天取一次或按一预定的时间间隔提取的一系列便样来确定的。另一种方式是,可以采用二次或多次测定作为控制或对照标准。
2.带有可收缩凹槽的多重型装置
在多重型装置的又一种变型中,至少一个试样制备区中可以有一个可收缩的凹槽,可以将一种抽取签条或其它含有试样的部件加入该凹槽中。在这种变型中,第一可对折构件进一步包括可以铰接折叠的翼板,当第一和第二可对折构件相互对折叠合后,这些铰接折叠的翼板则折叠在第二可对折构件的上面。
多重型装置的这种变型示于图20中。装置620具有一第一和第二可对折构件622和624。第二可对折构件624由一个铰链626铰接在第一可对折构件622上。在第一可对折构件622上还铰接有两个可折叠的翼板628和630。第一可对折构件622有一个控制凹槽632和一个可收缩的试样凹槽634,亦即它是由类似于海绵这样的材料制成的。第二可对折构件624有数个色谱介质636,在本实施例中为两个,每一个都有一个检测区638和一个控制区640。第二可对折构件624有一个开孔642,用于观察每个色谱介质636的一部分,色谱介质包括检测区638和控制区640。第一和第二可对折构件622和624有接合件641和643。当将第一和第二可对折构件622和624相互对折叠合后,控制凹槽632和可收缩凹槽634中的试样就被施加到相应的色谱介质636中,用以进行色谱分析。
3.能够接收试验卡片的多重型装置
多重型装置的又一种变型对于测定粪便隐血中的血红蛋白尤其有用。这种装置能够接收一个含有几个干燥的粪便试样(典型的情况是在连续的几天内留取的)的试验卡片。
这个装置示于图21中。测定装置660包括一第一可对折构件662,一个由一第一铰链666铰接在第一可对折构件662上的第二可对折构件664,和一个由一第二铰链670铰接在第一可对折构件662上的第三可对折构件668。第一可对折构件662适于接收一个其上装有几个干燥的标本674的试验卡片672。第二可对折构件664上面有一个试剂垫676。第三可对折构件668有多个色谱介质678,每个色谱介质都有如前所述的一个检测区680和一个控制区682。每个要测试的试样都有一个单独的色谱介质678。第三可对折构件668上有一个开孔684,用以观察至少一部分色谱介质678,每个色谱介质包括一检测区680和一控制区682。第二和第三可对折构件包含接合件681和685,装置660也如前面对三构件装置所述的那样有一个密封垫686。
在使用时,将含有多个干燥标本674的试验卡片672插入到第二可对折构件664中。第二可对折构件664折叠到含有试剂垫676的第一可对折构件662的上面,使试剂垫676接触试验卡片664上的多个干燥标本674,进而从干燥标本674中提取分析物。然后从第一可对折构件662上面打开第二可对折构件664。最后将第三可对折构件668折叠到第一可对折构件662的上面,以使试剂垫676上的内含物和从干燥标本上提取的分析物施加到色谱介质678上,由此可以发生色谱过程。
在这个装置中,试剂垫676含有一种用于分析物的标记有一种可检测标记物的以通过向试剂垫676加入一种含水试剂能够被溶解的形式的特异性结合体。所加入的试剂是用于要测定的分析物的一种提取试剂,如血红蛋白。
当将第二可对折构件664对折到第一可对折构件662的上面之后,分析物就从试验卡片672上的试样中提取出并结合到加标记的特异性结合体上,当随后将第三可对折构件668对折到第二可对折构件上面后,结合在加标记的特异性结合体上的任何分析物都通过色谱介质668迁移,并结合到每个色谱介质678中的检测区680上。
本发明的多重型装置的又一种变型是一种类似于图19所示的多重型装置,但它能接收一个试验卡片。该试验卡片包含多个试样,例如在进行一种粪便隐血检测时,这些试样是一些粪便试样。
这种变型示于图22中。测定装置700有一第一可对折构件702和一第二可对折构件704。第二可对折构件704由一个铰链706铰接到第一可对折构件702上。第一可对折构件702包括多个色谱介质708。每个色谱介质708都有一第一端710和一第二端712,并包括一个检测区718和一个控制区720。每个色谱介质708的第一端710和一个传导体714有作用性接触,而每个色谱介质708的第二端712与一个吸收体716有作用性接触。每个色谱介质708都对应有一个单独的传导体714和吸收体716。第一可对折构件702适于接收一个含有多个干燥标本724的试验卡片722,标本724设置成其能与每个传导体714有作用性接触。第二可对折构件704包括多个点样器726,每一个对应一个色谱介质708。更好的是,每个点样器726包含用于分析物的处于能被溶解的形式的加标记的特异性结合体。
在使用时,将一种缓冲剂或其它含水液体施加到每个点样器726上,以重新构造加标记的特异性结合体。将第一和第二可对折构件702和704相互对折叠合,使得每个点样器726被施加到对应的干燥标本724上,从而将每个干燥标本724和每个点样器726的内含物施加到每个传导体714上,并因此而施加到每个色谱介质708上。试验卡片722将每个标本724保持在其位上,使得它们能够接收点样器726的内含物,并使得标本724中的分析物被提取,与加标记的特异性结合体发生反应,并施加到传导体714上。第二可对折构件704包含多个开孔728,每个开孔对应一个色谱介质708,用以观察每个色谱介质708。第一和第二可对折构件702和704各有接合件725和727和一个密封垫730,以保持试样和试剂。
II.用于竞争法测定的色谱测定装置
结构上类似于前面所公开的那些装置的测定装置可以用于对单价分析物采用的竞争法测定。典型的单价分析物是半抗原,但是相同的原理可以用于测定任何是单价的分析物,如一个其上附加的抗体结合点被阻碍或改变的通常的多价抗原。可测定的分析物包括如下:
茶碱(theophylline),地谷新(digoxin),双异丙吡胺(disopyramide),利度卡因盐酸盐(lidocaine),普鲁卡因酰胺(procainamide),萘心安(prop ranolol),奎尼定(quinidin),氨基羟丁基卡那霉素A(amikacin),青霉素和其它一内酰胺抗生素,氯霉素,艮他霉素(gentamicin),卡那霉素,乙基紫苏霉素(netilmycin),托普霉素(tobramycin),三环抗抑郁剂(tricyclicantidepressants),乙琥胺柴浪丁(ethosuximide),苯巴比妥(phenobarbital)安定(diazepam),二苯基乙丙酰脲纳(phenytoin),普奈米东(primidone),丙戊酸(valproic acid),醋氨酚(acetaminophen),乙酰水杨酸(acetylsalicylic acid),布洛劳(ibuprofen),氨甲喋呤(methotrexate),毒品,如吗啡(morphine),可卡因,可待因(codeine),芬太尼(fentanyl),3-甲基芬太尼(3-methylfentanyl),安非他明(amphetamines),麦角酸二乙胺(lysergic acid diethylamide),苯环己哌啶(phencyclidine),和海洛因和它们的代谢物,DNP,1-取代的-4-羟基-2-硝基苯(1-substituted-4-hydroxy-2-nitrobenzenes),4-取代的-硝基三烷基苯胺盐(4-substituted-2-nitrotrialkylaniliniumsalt),和环境污染剂,如苯,甲苯(toluene),二甲苯(xylene),乙基苯(ethylbenzene),氯丹(chlordane),DDT和它的代谢物,2,4,-D,2,4,5-T,和阿特拉津(atrazine)。
适合用于进行这些测定的特异性结合体包括一些抗体和特异性结合蛋白质,但并不限于这些,后者的一个例子是从芽胞杆菌耐热硬脂酸(Bacillus stearothermophilus)隔离出来的毒霉素结合蛋白质(PBP)。
与以前适用于实施竞争法免疫测定的测定装置不同,本发明的这些装置的优点在于,在试样中存在的分析物会给出一个阳性结果或可检测的结果,每个结果都是以装置的检测区中的一条有色线形式出现。典型的情况是,在竞争法免疫测定中,一个可检测的信号的展开表示一个阴性结果(即没有分析物存在)。因此,在被观察的结果和检测之间存在一个相反的关系。本发明的这些装置产生一个在分析物浓度和可检测信号之间的直接关系,产生假阴性结果的可能性较小。这些装置也具有扩大的动态范围。
A.三构件双向流动装置
本发明用于竞争法测定的色谱测定装置的一个实施例是一种三构件双向流动装置。
该装置有三个可对折构件。第一可对折构件包含一个具有一第一端和一第二端的色谱介质,沿第一方向的流动是从第一端流向第二端及沿第二方向的流动是从第二端流向第一端。在色谱介质上的一个大大小于色谱介质的面积的分散区域中固定有分析物或它们免疫学模拟物。
一种较好的免疫学模拟物是一种共价地连接在一个蛋白质缺乏的、用于分析物的特异性结合活性体上的分析物,诸如通常的IgG或其它非免疫IgG。这种IgG最好抵制从要测定的分析物中被吸收,以便除去具有特异性结合活性的任何免疫球蛋白片段,无论是分析物的天然抗体,还是能够与分析物交叉反应的抗体。
半抗原与蛋白质,包含非免疫IgG的结合在本领域中是公知的,并且有过描述,例如参见P.Tijssen所撰写的“酶免疫测定的实践和理论”(1985年阿姆斯特丹.Elsevier)第279-296页。此处引用作为参考。简言之,含有羧基(carboxyl groups)的或者能够被羧化的(carboxylated)半抗原可以通过混合的酐(anhydride)反应,通过与一种水溶性碳化二亚胺(carbodiimide)反应,或者与N-羟基丁二酰胺(N-hydroxysuccinimide)的脂化反应而被偶合。通过诸如氧或氮的取代基与卤化酯(haloesters)的烷基化作用(alkylation),接着是脂的水解作用,或在类固醇的羟基或酮基上形成半琥珀酸酯(hemisuccinate)或羧甲基肟(carboxymethyloximes)这样的反应,可以进行羟化反应。
具有氨基类的半抗原,或者有能还原成氨基类的硝基类的半抗原可以转化成重氮化盐(diazonium salt),与弱碱性pH值下的蛋白质反应,生成芳香胺(aromatic amines)。具有脂肪胺(aliphatic amines)的半抗原可以用不同的方法结合到蛋白质上,这包括与碳化二亚胺(carbodiimides)的反应,与高双功能的(homobifunctional)试剂甲代亚苯基-2,4-聚氨脂(tolylene-2,4-diisocyanate)的反应,或者与马来酰亚胺(maleimide)化合物的反应。脂肪胺通过与P-硝基苯甲酰氯(nitrobenzoylchloride)反应,接着还原成P-氨基苯甲酰胺(P-amiobenzoylamide)也可以转变成芳香胺,在重氮化后与蛋白质相偶合。而且,具有双重功能的亚胺酸酯(imidate esters),如二甲基庚二酰亚胺酸酯(dimethylpimelimidate),二甲基已酰亚胺酸脂(dimethyladipimidate),或二甲基辛二酰亚胺酸酯(dimethysuberimidate),可以用于将含有氨基团的半抗原结合到蛋白质上。
含有硫羟(Thiol)的半抗原可以结合到有马来酰亚胺的蛋白质上,例如4-(N-马来酰亚胺基甲基)-环己烷-1-羧酸-N-羟基琥珀酰亚胺脂(4-(N-maleimidomethyl)-cyclohexane-1-carboxylic acid N-bydroxysuccinimide ester)。
对于具有羟基类的半抗原,一种乙醇功能(alcohol function)可以转变成半丁二酸脂(hemisuccinate),它引入一个可用于结合的碳基类。另一方面是,双功能的试剂癸二酰氯(sebacoyldichloride)将一种乙醇转变成一种酰基氨(phosgene),它然后与蛋白质反应。
酚可以用重氮化的P-氨基苯甲酸(P-nitrophenyl)(它引入一个碳基)激活,然后可以通过混合酐反应而与蛋白质进行反应。通过形成一种P-硝基苯苷(P-nitrophenyl glycoside)可以使糖激活,接着通过重氮化作用将硝基还原成一个氨基类。其它方法包含通过与高碘酸盐反应使糖的邻位二醇类(Vicinal glycol)分解成醛类,然后通过与硼氢化钠(sodium borohydride)的还原性烷化作用而与胺偶合。另一种方法是,含有羟基的半抗原在通过与碳酰氯反应,转变成氯甲酸酯(chlorocarbonates)之后可以被结合。
对于有乙醛或酮类的单抗原,可以通过形成O-羧甲基肟(O-carboxymethyloximes)引入碳基类。酮类也可用P-肼基苯甲酸(P-hydrazinobenzoic acid)衍生出,以产生碳基类,含有乙醛的半抗原可以通过形成席夫(schiff)基直接被结合,席夫基(Schiff bases)通过与一种还原剂如硼氢化钠反应而得到稳定。
色谱介质是硝基纤维素较好,分析物的模拟物则通过一种疏水性相互作用非共价地结合到硝基纤维素上。可以采用其它色谱介质,而分析物的模拟物也可以共价地结合到色谱介质上。
第一可对折构件进一步包括一个与色谱介质的第一端有作用性接触的第一传导体,和一个与色谱介质的第二端有作用性接触的第二传导体。
第二可对折构件包含一第一点样器,该第一点样器含有一个针对分析物的以通过向第一点样器加入一第一含水液体能够被溶解的形式的第一特异性结合体。第一点样液体可以是试样,但更好的是试样和一第一重新构成液体的组合物,其中先加入这种第一重新构成液体。
第三可对折构件包含一第二点样器,它含有一种针对分析物的以通过向第二点样器中加入一第二重新构成液体能够被溶解的形式的第二特异性结合体。第二特异性结合体上标记有一种可检测的标记物,更好地是一种肉眼可检测的标记物,如前面所公开的胶态金。第三可对折构件也含有一个与其上的第二点样器分隔开的吸收体。
第一和第二特异性结合体是针对分析物的典型抗体,它们可以是相同的,但不是必须相同。可以用单价抗体片段如Fab或Fab′片段代替完整的二价抗体。这在某些应用情况下可能更好,只要不要求在这种竞争法测定中让抗体分子与一个以上的对应分析物反应。
在使用中,将第一点样器上的第一特异性结合体溶解,较好的做法是只加入试样来溶解,或者也可以先加入一第一重新构成液体,再加入试样。第二点样器上的第二特异性结合体也通过加入一第二重新构成液体而被重新构成。典型地情况是,第一和第二重新构成液体是相同的。重新构成液体最好是一种缓冲液,它含有附加的成分,如螯合剂,清洁剂,抗菌剂和防腐剂。一种合适的重新构成液体的制备如下:即混合相等容积的磷酸盐缓冲液(0.1克分子,pH7.2,含80%的Tween-20)和HEPES缓冲液(2.5毫克分子,pH7.5,含0.005%氚核X-100,0.003%乙二胺四乙酸的四钠盐(tetrasodium EDTA)和0.65%叠氮化钠(sodiumazide))。较好的是,施加到第一和第二点样器的每一个上的重新构成液体的量是从约为5μl至200μl,更好的是从约为10μl~100μl,最好是20μl。施加的试样的量是在大约5μl~40μl的范围较好,最好是30μl。
在将试样施加到第一点样器上之后,将装置置于培养箱中,以使可溶解的特异性结合体溶解,并使第一特异性结合体与分析物反应,更好的情况是,培养期为约5分钟~30分钟左右,最好是大约15分钟。典型地情况是在室温下进行培养,但也可以在较低或较高的温度下进行。在较高温度下培养可以加快反应速度,而在较低温度下培养则可以是希望避免敏感试样受到氧化或其它分裂。
在培养之后,将第一和第二可对折构件相互对折叠合,使试样和已溶解的针对分析物的第一特异性结合体施加到第一传导体上,然后施加到色谱介质的第一端上。然后试样和已溶解的特异性结合体就可以通过至少一部分色谱介质移动,并通过固定在色谱介质上的分散区域中的分析物或免疫学模拟物。这一般需要大约10~20秒的时间。
此时,打开第一和第二可对折构件使之相互分离,并将第一和第三可对折构件相互对折叠合,使吸收体与第一传导体接触,和使第二点样器与第二传导体接触。这样,就使吸收体从色谱介质的第一端抽吸液体,从而使第二点样器将含有已溶解的加标记的特异性结合体的液体施加到色谱介质的第二端。更好的是,然后将第二可对折构件折叠在第一和第三可对折构件上面,以保证有足够液体从第二点样器中挤出而被吸收体吸收,由此使流动更有效地反向。通过将第二可对折构件折叠回来而加在色谱介质上的压力来促进流动的反向。
然后使加标记的已溶解的特异性结合体移动通过至少一部分色谱介质,这部分色谱介质与试样和第一特异性结合体通过的色谱介质部分相重叠,并包含含有固定分析物或免疫学模拟物的分散区域。如果分析物存在于试样中,那么加标记的特异性结合体就结合在分散区域中并被检测。如果可检测的标记物是一种肉眼可检测的标记,则在分散区域中可以看见一条线。
这种测定可以作为定性测定来实施,亦即一种“开/关”测定。在这种测定中,第一特异性结合体存在于一种浓度下,使之结合分散区中的实际上所有的固定分析物或其免疫学模拟物。分散区中结合到第一特异性结合体上的结合点被阻碍而不能进一步结合。如果分析物存在于试样中,则分析物结合第一特异性结合体,防止第一特异性结合体与分散区中的固定分析物或分析物的模拟物结合。这样,第二加标记的特异性结合体可以结合到分散区中的分析物或其免疫学模拟物上,给出一个可检测的信号。
一种定量测定方案可以在一个壳中采用两个或多个色谱介质,其中至少一个色谱介质作为一个控制标准来设计,作为一个参照物使用。
一种适用于竞争法测定的这种实施例的装置示于图23中。色谱测定装置740有一第一、一第二和一第三可对折构件742,744和746。第二可对折构件744由一第一铰链748铰接在第一可对折构件742的一侧边上,第三可对折构件746由一第二铰链750铰接在第一可对折构件742的另一侧边上。第一可对折构件742有一个具有一第一端754和一第二端756的色谱介质752,一第一传导体758与色谱介质752的第一端754有作用性接触,一个第二传导体760与色谱介质752的第二端756有作用性接触。色谱介质752也有如前面所述的一个分散区域762,其上固定有分析物或它的免疫学模拟物,作为信号读出。
第二可对折构件744有一第二点样器764,它含有用于分析物的以可溶解形式的一第一特异性结合体,试样最好施加到该结合体上。
第三可对折构件746有一第二点样器766,它含有用于分析物的、标记有一种可检测标记物的、并以通过向第二点样器766加入一第二含水液体以能够被溶解的形式存在的第二特异性结合体。第三可对折构件746有一个与第二点样器766分离开的吸收体768,第三可对折构件746也有一个用于观察至少一部分色谱介质752,包含分散区域762的开孔770,或者将一个开孔772设置在第一可对折构件742中的色谱介质75 2的分散区域762之后面,以便在装置740闭合后从装置740的后侧进行观察。第二和第三可对折构件744和746有接合件769和773,装置740有保持试剂用的一个密封垫774。
当将第一和第二可对折构件742和744相互对折叠合后,则使第一点样器764与第一传导体758有作用性接触,以使第一点样器764的内含物施加到第一传导体758,然后施加到色谱介质752的第一端754。当将第三和第一可对折构件746和742相互对折叠合后,则吸收体768与相邻于色谱介质752的第一端754的第一传导体758有作用性接触,而第二点样器766与相邻于色谱介质752的第二端756的第二传导体760有作用性接触,由此使色谱介质752中的液体流动反向。
B.带盖子的两构件双向流动装置
本发明的用于竞争法测定的色谱测定装置的一个第二实施例是一种带盖子的两构件双向流动装置。在这个实施例中,要测试的试样没有用抗体预先培养,而是直接施加到一介与色谱介质直接接触的传导体上。
用于竞争法免疫测定的色谱测定装置的这个第二实施例可以包括一第一可对折构件和一第二可对折构件。第一可对折构件有一个具有一第一和一第二端的色谱介质。色谱介质上固定有:(1)一个用于分析物的第一特异性结合体,和(2)一个能够结合对分析物缺乏亲合力的一对特异性结合体的次特异性结合体。这些组分放置在色谱介质上单独分散的且不重叠的区域中。次特异性结合体比用于分析物的第一特异性结合体更靠近色谱介质的第一端。更好的是,第一特异性结合体距离色谱介质中的次特异性结合体约0.25英寸(6.35毫米),以提高效率。
典型地,用于分析物的第一特异性结合体,如前所述的那样,是一种用于分析物的抗体或者一个抗体片段
典型地,次特异性结合体是一种这样的抗体,它能够基于一个种类特异的决定体而不是基于要结合的免疫球蛋白的抗体特异性(如果有的话)而结合另一个免疫球蛋白。例如,次特异性结合体可以是山羊抗家兔IgG抗体,该抗体结合所有家兔免疫球蛋白G分子,而与它们的免疫学特异性无关。
第一可对折构件也包含一个与色谱介质的第一端有作用性接触的第一传导体,和一个与色谱介质的第二端有作用性接触的第二传导体。更好的是,第一可对折构件有一条限制线来标记,该线表示在双向色谱过程中出现流动反向的位置。
第二可对折构件包含:(1)一个含有分析物的模拟物的点样器,模拟物以通过向点样器加入一种重新构成液体能够被溶解的形式;和(2)一个与点样器分隔开的吸收体。
分析物的模拟物是共价地连接到能够与次特异性结合体结合的一对特异性结合体的一个组分上的分析物。在分析物的模拟物中的特异性结合体对的这个组分标记有一个可检测的标记物,更好的是该可检测的标记物是一种肉眼可检测的标记物,该可肉眼检测标记物最好是一种金属胶如金、银或铜胶。
例如,当次特异性结合体是山羊抗家兔IgG时,与分析物结合的特异性结合体对的组分是通常的对分析物没有抗体活性的家兔IgG。
当青霉素是分析物时,适用于这种测定方案的一种分析物的模拟物的例子,是共价地连接到家兔IgG上的7-氨基头孢烷酸(7-amincephelosporanic acid),其中家兔IgG用胶态金标记。
当将第一和第二可对折构件相互对折叠合后,则使一第二传导体与点样器有作用性接触,从而将点样器的内含物施加到第二传导体上,并通过至少一部分色谱介质抽吸。同时也使吸收体与第一传导体有作用性接触,而从色谱介质的第一端抽吸液体,使色谱介质中的流动反向。
在向下流动的第一阶段期间,存在于一个阳性标本中的分析物无阻碍地通过色谱介质上的次特异性结合体的区域,然后结合在用于分析物的第一特异性结合体的区域上。对于一个阳性试样,在向上流动的第二阶段期间,加标记的分析物的模拟物被阻碍,不能结合到用于分析物的第一特异性结合体上,然后则结合到次特异性结合体上。如果试样没有分析物。那么在向下流动阶段期间就没有分析物结合到第一特异性结合体上,而在向上流动的第二阶段期间分析物的模拟物被结合到第一特异性结合体上,而不会到达次特异性结合体,从而在第二特异性结合体处没有显现出信号。
更好的是,装置进一步包括一个铰接在第一可对折构件上的盖子,从而当第一和第二可对折构件相互对折叠合后,盖子可以折叠在它们上面。在盖子上可以开一个开孔,以便能在第一和第二相互对折叠合之后观察其中的至少一部分色谱介质。或者将一个开孔设置在色谱介质后面,并从闭合的装置的背侧进行观察。
该装置也可以在一个壳体中设置两个或多个色谱介质,至少一个色谱介质设计成一种用于参照物的控制标准,以便半定量地或定量地指示存在于试样中的分析物的浓度。
在这个实施例的另一种变型中,次特异性结合体可以沿多重谱带固定在检测区中,从而用于结合到次特异性结合体上所存在的加标记的分析物的模拟物被滴定。测定每一个谱带中的次特异性结合体的数量,从而通过分析物的模拟物所结合的谱带数目指示出结合到检测区上的分析物的模拟物的数量,因此指示出试样中分析物的浓度。这种方法给出了分析物浓度的一种半定量估计估。典型地,在这种方案中,相对于分析物的第一特异性结合体,次特异性结合体在色谱介质上最近的谱带具有最低浓度的次特异性结合体,随后每个相继谱带具有大于在最低谱带中的浓度的次特异性结合体的浓度。
如果分析物的浓度足够高,使足够多的未结合的加标记的分析物的模拟物渗透到次特异性结合体的第一谱带,那么一些加标记的分析物的模拟物就会结合到次特异性结合体的第二谱带上。这样,在色谱介质的检测区处就会看见两条线。由此通过在检测区中出现一条、两条或三条线就相应地指示出分析物浓度的范围。
要测定的分析物的预计浓度范围决定着在检测区中出现一条或多条线的浓度,例如,采用尼古丁代射物可铁宁(Cotinine)时,在一种体液中有10ppb的浓度表示是很严重的被动吸烟,500ppb的浓度表示是一个主动吸烟者,而10,000ppb浓度则表示是一个烟瘾极大的吸烟者。可以这样布置测定装置,使得在检测区中,当可铁宁为10ppb时出现一条线,为500ppb时出现两条线,为10,000ppb时出现三条线。
在操作中,如前所述,将重新构成液体施加到点样器上,以溶解分析物的模拟物。然后将试样施加到第一传导体,并使之迁移到限制线。典型地,沿第一方向的色谱过程大约为5~25秒的时间,更典型的情况是大约为10秒。然后将第二可对折构件折叠在第一可对折构件上面,使它们相互叠合起来,再将盖子折叠在第一和第二可对折构件上面。在约为30秒~10分钟(典型地约为2分钟)的培养期之后,如果试样中存在分析物,则会在次特异性结合体处看到一条可见的线。试样和重新构成液体的优选体积在前面针对竞争法免疫测定装置的第一实施例中已经描述。
一个适用于这种实施例的竞争法免疫测定装置示于图24中。色谱测定装置780有一第一可对折构件782,一第二可对折构件784,和一个盖子786。第二可对折构件784由一第一铰链788铰接在第一可对折构件782的一侧边上,盖子786由一第二铰链790铰接在第一可对折构件782的另一侧边上。第一可对折构件782有一个具有一第一端794和一第二端796的色谱介质792。色谱介质792有一个其上固定有用于分析物的一第一特异性结合体的区域798,和一个其上固定有次特异性结合体的非重叠区域800。第一可对折构件782也包含一个与色谱介质792的第一端794有作用性接触的第一传导体802,和一个与色谱介质792的第二端796有作用性接触的第二传导体804。第一可对折构件782也包含一条限制线806,以指示在进行测定期间要使第一和第二可对折构件782和784相互对折叠合的点,以使液体流动反向。
第二可对折构件784包含一个点样器808,它具有以通过加入重新构成液体能够被溶解的形式的分析物的模拟物。第二可对折构件784也包含一个与点样器808分隔开的吸收体810和一个开孔814。当第一和第二可对折构件782和784相互对折叠合后,点样器808则与第二传导体804有作用性接触,而吸收体810与第一传导体802有作用性接触,以使液体流动反向。盖子786在其上开有一个开孔812,用以观察一部分色谱介质792。更好的情况是,由开孔812可以观察次特异性结合体区域800,而不是观察针对分析物的第一特异性结合体的区域798。第二可对折构件784和盖子786也包含接合件811和813。装置用一个密封垫815围住。
C.带吸收体的三构件单向流动装置
适用于竞争法免疫测定的这种实施例的又一种装置示于图25中。该装置有一第三构件,该第三构件含有从色谱介质和两个传导体上抽吸液体的吸收体或吸纸。当吸收体与色谱介质有作用性接触时,吸收体在色谱介质的一个较大部分上延伸。色谱测定装置820有一第一、一第二和一第三可对折构件822、824和826。第一可对折构件824由一第一铰链828铰接在第一可对折构件822的一侧上,第三可对折构件826由一第二铰链830铰接在第一可对折构件822的另一侧边上。第一可对折构件822有一个具有一第一端834和一第二端836的色谱介质832。色谱介质有一个用于固定其上的分析物840的一第一特异性结合体的区域以及一个在其上固定一第二特异性结合体的非重叠区域。第一可对折构件822也有一个用作一点样器的、与色谱介质832的第一端有作用性接触的第一传导体842,和一个与色谱介质832的第二端836有作用性接触的第二传导体844。第一可对折构件822也有一条限制线,用于指示要使第一和第二可对折构件822和824相互对折叠合的点。
第二可对折构件824包含一个含有分析物的模拟物的第二点样器850。典型地,将一种含水液体加到第二点样器850上,以溶解第二点样器850上的分析物的模拟物。第二可对折构件824也包含一个与第二点样器850分隔开的第一吸收体848。当第一和第二可对折构件822和824相互对折叠合后,第二点样器850与第一传导体842有作用性接触,而第一吸收体848与第二传导体844有作用性接触,以抽吸液体。一个开孔852设置在色谱介质之后,用以从背后观察一部分色谱介质。第二和第三可对折构件824和826包含接合件849和853。装置820也有一个密封垫858。
第三可对折构件826包含一第二吸收体854,当第三和第一可对折构件826和822相互对折叠合后,第二吸收体854处于能与色谱介质832的相当大的区域有作用性接触。这样将除去色谱介质832、第一传导体842和第二传导体844中的过多的液体。
在使用时,将试样施加到第一传导体或点样器842上,使之在色谱介质832中移动。将第三可对折构件826与第一可对折构件822相互对折叠合,以使第二吸收体854与第一传导体或点样器842和色谱介质832直接接触,而将过多的液体抽吸到第二吸收体854中。然后将第二和第一可对折构件824和822相互对折叠合,以使含有已溶解的加标记的分析物的模拟物的第二点样器850在色谱介质832的第一端834处接触传导体或点样器842。此外也使第一吸收体848在色谱介质832的第二端处与第二传导体844接触。然后将第三可对折构件826作为一盖子闭合在第二可对折构件824上。从位于色谱介质832后面的开孔856可看见一部分色谱介质。
对分析物的检测和/或测定按照前面在II(B)节中对双向流动装置所讨论的同样方式进行。
D.利用生物素(biotin)的特异性的三构件双向流动装置
本发明的色谱装置的又一个实施例是一种利用生物素-抗生物素蛋白键的三构件双向流动装置。
第一可对折构件有一个具有一第一端和一第二端的色谱介质,如上所述。色谱介质上固定有:(1)一种能与生物素特异性结合的物质,它是从由抗生物素蛋白、抗生蛋白链菌素、抗生物素抗体和其衍生物构成的组中选择出来的;(2)一种次特异性结合体。次特异性结合体能够特异性地结合一种三元复合物,该三元复合物包括:(a)分析物,(b)对共价结合到分析物上的分析物缺乏特异性结合亲合力的一种特异性结合体对中的一个组分;和(c)一个结合到特异性结合体的那个组分上的可检测标记物。这种三元复合物设置在一第三可对折构件上,如下面所述。
这些结合组分都固定在色谱介质上的一些单独的分散并且不重叠的区域中,每个区域都大大地小于色谱介质的面积。次特异性结合体固定在第一分散区域并处于比能够结合生物素的物质更靠近色谱介质的第一端的地方,(能结合生物素的物质此处一般地称为“抗生物素蛋白”),该物质固定在第二分散区域中。
第一可对折构件也包含一个与色谱介质的第一端有作用性接触的第一传导体和一个与色谱介质的第二端有作用性接触的第二传导体。
第二可对折构件包含一第一点样器,它有一个针对分析物的、以通过向点样器加入含水液体能够被溶解的形式的第一特异性结合体。如前所述,含水液体可以只是试样较好,或者可以是一种第一重新构成液体,随后加入该试样。第一特异性结合体不能被次特异性结合体结合。第一特异性结合体结合到生物素上。
使生物素键接到球蛋白,包含抗体上的方法在本领域中是公知的,并有描述,例如参见P.Tijssen的“supra”杂志,第25-31页,此处引作参考。生物素可以作为一种反应脂直接地结合到蛋白质上,或者通过引入一种间格隔基(spacer)如ε-氨基己酸(ε-aminoca)而结合到蛋白质上。典型的反应脂是:生物素-P-硝基苯脂(biotinyl-p-nitrophenyl ester),生物素-N-羟基丁二酰胺脂(biotinyl-N-hydroxysuccinimide ester),和已酰基酰氨基生物素-N-羟基丁二酰胺脂(caproylamidobiotinyl-N-hydroxysawinimide ester),其中最后一个反应脂在生物素等分和蛋白质之间提供一个间隔基。生物素也可以用其它组族来激活。
第三可对折构件包含:(1)一个含有三元复合物的第二点样器,如上所述,三元复合物包括分析物,对分析物缺乏亲合力的特异性结合体对中的一个组分,和可检测标记物,(2)一个与第一点样器分隔开的吸收体。
在该装置中,将第一和第二可对折构件相互对折叠合,使第一传导体与第一点样器有作用性接触,从而将第一点样器的内含物施加到第一传导体上并进入色谱介质的第一端。这样,第一点样器的内含物通过至少一部分色谱介质迁移。将第一和第三可对折构件相互对折叠合,则使第二点样器与第二传导体有作用性接触,以使第二点样器的内含物施加到色谱介质的第二端,此外也使吸收体与第一传导体有作用性接触,而从色谱介质第一端抽吸液体,并使流动反向。
在色谱测定装置的这个实施例中应用的一种合适的抗体组合物的例子是(以茶碱作为分析物)在三元复合物中,生物素基化的鼠色(murine)单克隆抗茶碱IgG抗体作为生物素基化的第一特异性结合体,山羊抗家兔IgG抗体作为固定的次特异性结合体,和缺乏抗茶碱活性的家兔IgG作为特异性结合体对的组分。
可以用按照这个实施例的一个装置测定的分析物的另一个例子是青霉素,采用青霉素结合蛋白(PBP)作为特异性结合体,和一种包括共价地键合到家兔IgG上的7-氨基头孢烷酸的三元复合物,家兔IgG上用胶态金标记。其它-内酰胺抗生素可以类似地测定。
在操作时,第一点样器上的生物素基化的第一特异性结合体最好通过只加入试样来溶解,或者通过加入一第一重新构成液体后再加入试样来溶解,如前所讨论的那样。第二点样器上的三元复合物由一第二重新构成液体溶解,如前面II(A)节中所述。在经过一段足以使试样中的任何分析物结合到第一特异性结合体上的培养期之后,将第一和第二可对折构件相互对折叠合,以使试样和正溶解的第一特异性结合体施加到第一传导体上,然后施加到色谱介质的第一端上。试样和第一特异性结合体通过色谱介质迁移,且通过色谱介质中的固定试剂的两个分散的不重叠的区域。第一生物素基化的特异性结合体结合能在第二分散区域中结合生物素的组分。如分析物存在于试样中,那么经过生物素-抗生物素蛋白键而结合到固相载体上的生物素基化的特异性结合体本身结合到分析物上。如果试样中不存在分析物,则分析物不会结合到被结合的生物素基化的特异性结合体上。在试样和溶解的第一特异性结合体通过第二分散区域之后,将第一和第二可对折构件相互分离开,并将第一和第三可对折构件相互对折叠合,以使流动反向,并将三元复合物施加到第二传导体上。然后三元复合物在色谱介质中从第二端处开始向第一端方向迁移。如果分析物存在于试样中,那么结合到第二分散区域中的抗生物素蛋白上的生物素基化的特异性结合体就不能结合三元复合物中的分析物,从而三元复合物到达次特异性结合体。然后次特异性结合体结合三元复合物中的特异性结合体对中的组分,由此对它检测。典型的情况是,装置的第三可对折构件上有一个开孔,使得在将第三可对折构件与第一可对折构件相互对折叠合后,只能看见色谱介质上的次特异性结合体的第一分散区域,而看不见抗生物素蛋白的第二分散区域。但是,当试样中设有分析物时,三元复合物被第一特异性结合体结合,后者被抗生物素蛋白所结合,抗生物素蛋白的抗原结合点未被占据。三元复合物则不会到达含有用于检测的次特异性结合体的第一分散区。
适合实施竞争法免疫测定的这种方案的一种色谱测定装置示于图26中。色谱测定装置860具有一第一、一第二和一第三可对折构件862、864和866。第二可对折构件864由第一铰链868铰接于第一可对折构件862的一侧边上,而第三可对折构件866由第二铰链870铰接于第一可对折构件862的另一侧边上。第一可对折构件862有一个具有一第一端874和一第二端876的色谱介质872,一第一传导体878与色谱介质872的第一端874有作用性接触,而第二传导体880与色谱介质872的第二端876有作用性接触。色谱介质872有一个用于一种次特异性结合体的第一分散区882和一个用于抗生物素蛋白的第二分散区884。第一和第二分散区882和884是不重叠的,第一分散区882更靠近色谱介质872的第一端874设置。第二可对折构件864有一个含有用于分析物的可溶解第一特异性结合体的第一点样器886。第三可对折构件866有一个含有可溶解的三元复合物的第二点样器888和一个与第二点样器888分隔开的吸收体890。第二和第三可对折构件864和866中也有用于观察一部分色谱介质872的开孔892和894,开孔892和894可以观察含有次特异性结合体的第一分散区882,但不能观察含有抗生物素蛋白的第二分散区884。第二和第三可对折构件864和866也包含接合件891和895。装置860也有一个密封垫896。
将第一和第二可对折构件862和864相互对折叠合,则使第一点样器886与第一传导体878有作用性接触,开始通过色谱介质872的流动。之后,再将第一和第三可对折构件862和864相互对折叠合,则第二点样器888与第二传导体880有作用性接触和吸收体890与第一传导体878有作用性接触,从而使通过色谱介质872中的流动反向。
在装置的这个实施例的一个变型中,检测区可以包含两个或多个次特异性结合体谱带,如前面在II(B)节中所述的那样。这样可以滴定可用于结合的加标记的三元复合物的数量,以便利用检测区中可看见的谱带数目指示出试样中存在的分析物的数量。
E.用于竞争法抑制免疫测定的两构件装置
本发明的色谱介质装置的又一个实施例适用于实施竞争法免疫测定。当试样中存在有分析物时,这个装置通过提供一个可检测的信号给出分析物浓度的一个阳性指示。
这个实施例是一种两构件装置,且流动在整个装置中是单向的。第一可对折构件包含一个有一第一端和一第二端的色谱介质。色谱介质上固定有:(1)一种能够结合一种用于分析物的第一特异性结合体的分析物的模拟物;(2)能与第一特异性结合体对中的一个组分结合的一种次特异性结合体,该组分对于分析物没有亲合力,次特异性结合体本身对分析物缺乏亲合力。这些组分都放置在色谱介质上的分开的且不重叠的分散区中。分析物的模拟物比次特异性结合体更靠近色谱介质的第一端。
分析物的模拟物是共价地连接到一个蛋白质分子上的分析物,例如一种非特异性的免疫球蛋白,它能被结合到色谱介质上。该蛋白质分子不应对分析物或对分析物的一种特异性结合体有结合亲合力。
次特异性结合体在一种种类特异性的确定物的基础上与一种用于分析物特异性结合体特异性地结合,如前面所述的那样。次特异性结合体和用于分析物的特异性结合体之间的相互作用不涉及用于分析物的特异性结合体的抗原结合点。
第一可对折构件也包含一个与色谱介质的第一端有作用性接触的传导体,更好的是,第一可对折构件包含一个与色谱介质的第二端有作用性接触的吸收体。
第二可对折构件包含一个点样器,点样器上包含有用于标记有一种可检测的标记物的分析物的特异性结合体。更好的是,可检测标记物是一种肉眼可检测的标记物,如一种金属胶。如果第一可对折构件上没有吸收体的话,另一种方式是,第二可对折构件可以进一步包含一个与点样器分隔开的吸收体。更好的是,第二可对折构件也有一个能够观察一部分色谱介质的开孔。更好的情况是,由该开孔可以观察到次特异性结合体的区域而不是分析物之模拟物的区域。
在使用中,要测试的试样被施加到点样器上,以溶解加标记的特异性结合体。典型的情况是,试样和特异性结合体一起培养大约1~3分钟,尽管如果希望更高的敏感性时可以增加该时间长度。
然后使第一和第二可对折构件相互对折叠合,使点样器的内含物施加到传导体,然后施加到色谱介质的第一端。在一个阳性试样中存在的分析物占据在加标记的特异性结合体上的分析物结合点,从而加标记的特异性结合体不会结合到色谱介质上的分析物的模拟物上面。相反,加标记的特异性结合体继续行进到次特异性结合体的区域,而在此处结合,形成一条可检测的线,该线给出分析物存在的一个阳性指示。
当试样中不存在分析物,所有加标记的用于分析物的特异性结合体都被分析物的模拟物所结合,而不会到达次特异性结合体。所用的试剂的数量可以滴定,从而需要给出一个阳性反应的分析物的浓度可以进行调节,以适应临床分析要求或药理学要求。
适用于竞争法免疫测定的这个实施例的一个装置示于图27中。装置900包括由一个铰链906铰接的第一和第二可对折构件902和904。第一可对折构件902有一个具有一第一端910和一第二端912的色谱介质908。色谱介质908有一个其上固定分析物的模拟物914的区域,和一个其上固定一种次特异性结合体916的非重叠的区域。第一可对折构件902也包含一个与色谱介质908的第一端910有作用性接触的传导体918和一个与色谱介质908的第二端912有作用性接触的吸收体920。
第二可对折构件904有一个点样器922,它含有以通过加入试样能被溶解的形式用于分析物的加标记的特异性结合体。第二可对折构件904也有一个用以观察至少一部分色谱介质908的开孔924,更好的是由该开孔924可以观察到次特异性结合体916的区域,而不是分析物的模拟物914的区域。第一和第二可对折构件也包含如前面对两构件装置所述的接合件923和925,和一个密封垫926。
在装置的这个实施例的另一个方案中,检测区可以包含两个或更多的次特异性结合体的谱带,以给出试样中分析物浓度的一个半定量的指示,如上面在II(B)节中所述的那样。由此滴定可用于结合的加标记的特异性结合体的数量,以便利用检测区可看见的谱带数目,给出试样中分析物存在的数量的一个指示。
III.在测定装置上使用的分析物和抗体
适合于用本发明的测定装置检测的分析物包括抗原,半抗原和抗体。可以用装置检测的抗原包括血红蛋白、链球菌(streptococcus)A和B抗原,对原生动物寄生虫(protozoanparasite)贾第鞭毛虫有特异性的抗原和病毒抗原,包含对人类免疫缺陷病毒(HIV)有特异性的抗体和对肝炎有特异性的澳大利亚抗原。可以测定的抗体包括细菌抗体,如幽门螺杆菌(helicobacter pylori),和病毒抗体,包含人类免疫缺陷病毒抗体。可检测的半抗原包括在前面第III节中同前(supra)所列举的半抗原,以及能够对其制备具有足够特异性的抗体的其它半抗原。
如果分析物是一种抗原或一种半抗原,并采用夹心法,那么第一和第二特异性结合则最好是抗体。在许多应用中,较好的是,第一和第二特异性结合体是分析物上的不同表位的抗体,但这不是所要求的。抗体可以是多克隆或单克隆的,并可以是IgG,IgM或IgA。在许多应用中,优选的是多克隆抗体,因为它们固有的可变性在存在或可能存在抗原多型性的系统中能进行更加精确的检测。
当分析物是一种半抗原并采用夹心测定法时,第一和第二特异性结合体最好是不同表位的抗体,否则可以产生不希望有的竞争反应,而可能干扰加标记的特异性结合体和分析物的复合物结合到固定的第二特异性结合体上。人们认识到,不是所有的半抗原都是大到足以容纳一个以上的表位;但是某些半抗原虽然在由其本身注射后不会大到足以引起抗原的形成,但也大到足够包含一个以上的表位。在不能获得针对一个半抗原的一个以上的表位的抗体时的情况下,一般是优选竞争测定法。
当分析物是一种抗体,并采用夹心测定法时,第一特异性结合体典型地是一种基于种类、等级或次等级(见图表)特异性而结合到分析物上的加标记的抗体。最好是针对一种抗体分析物的第一特异性结合体结合到抗体分析物的恒定区域上,以防止干扰。当分析物是抗体时,较好的是,第二特异性结合体是对抗体分析物特异的一种抗原或半抗原。
在某些应用中,希望采用直接标记。例如,在检测贾第鞭毛虫抗原时,可以采用IgM抗体,这种抗体可能难以直接标记。在这种情况下,可以对针对移动的第一特异性结合体的一种次特异性结合体进行标记。典型地,被标记的次特异性结合体在种类、等级或次等级特异性基础上结合到是第一特异性结合体的抗体上。
作为采用一种次特异性结合体的替换方法,可以使第一特异性结合体结合到生物素上,并可采用一种抗生物素蛋白结合的标记物。
用于夹心法免疫测定的分析物,特异性结合体和标记物之间的这些关系概括在下面的表I中。
表I用于夹心法免疫测定的结合方案
Ag=抗原H=半抗原Ab=抗体Ab1=第一抗体Ab2=第二抗体Abc,Abc1,Abc2=对另一个抗体具有特异性的抗体Bi=生物素Av=抗生物素蛋白L=标记物*表示加标记物的组分
| 分析物 | 第一特异性结合体(移动的) | 第二特异性结合体(固定的) | 次特异性结合体 | 形成的复合物 |
| Ag | Ab1* | Ab2 | --- | Ab2-Ag-Ab1 * |
| H | Ab1 * | Ab2 | --- | Ab2-H-Ab1 *(1) |
| Ab | Abc * | Ag | --- | Ag-Ab-Abc * |
| Ag | Ab1 | Ab2 | Abc * | Ab2-Ag-Ab1-Abc * |
| Ab | Abc1 | Ag | Abc2 * | Ag-Ab-Abc1-Abc2 * |
| Ag | Ab1-Bi | Ab2 | Av-L | Ab2-Ag-Ab1-Bi-Av-L |
(1)Ab2和Ab1*优选结合到不同的表位上;不是所有半抗原都具有这种不同的表位。
在竞争法免疫测定的反应方案中的分析物,特异性结合体,标记物和其它参与物之间的关系示于下面的表II中。
表II用于竞争法测定的结合方案
| 施加到色谱介质上 | 固定到色谱介质上 | 有分析物时的结合 | 没有分析物时的结合 | |||||
| 第一方向 | 第二方向 | 第一点 | 第二点 | 第一点 | 第二点 | 第一点 | 第二点 | |
| I | H-AblorAb1 | Ab2=L | H | --- | H-Ab2=L | --- | H-Ab1 | --- |
| II | Hor--- | H=Ig=L | Abs | Ab1 | Abs|lI=Ig=L | H-Ab1 | Abs | Ab1-H=Ig=L, |
| III | H-Ab1=BiorAb1=Bi | H=Ig=L | Abs | Av | Abs|H=Ig=L | lH-Ab1=Bi-Av | Abs | L=Ig=H-Ab1=Bi=Av |
| IV | H-Ab1=LorAb1=L | --- | Abs | H | Abs|H-Ab1=L | H | Abs | H-Ab1=L |
表II(续)
H:半抗原
Ab1,Ab2:对半抗原特异的第一和第二抗体
Ig:缺乏特异性结合活性的免疫球蛋白
Abs:结合Ab1或Ab2的次抗体
Bi:生物素
Av:抗生物素蛋白
L:标记物
-:非共价键
=:共价键
IV.试验箱(Test Kits)
本发明的另一个方案是能够用于检测特定分析物的试验箱。一种试验箱包括(在单独的容器中):
(1)一个按照本发明的色谱测定装置;
(2)任何为处理或提取试样所必要的试剂;
(3)如果测定装置没有针对分析物的、以能够溶解形式的加标记的特异性结合体,则有选择地包含所要求的特异性结合体。
在(2)和(3)点中所要求的组分是单独包装的,且它们可以是液体或固体形式的(冷冻干燥的,结晶体的,沉淀的或者凝结的)。如果是固体形式的,则使用者要将其溶解,典型的是用含有生理盐水的蒸馏水或纯化水,或一种缓冲液。
在某些情况下,试验箱也可以包含一种重新构成液体,用于存在于装置上的以可溶解形式的一种试剂,它或者是一种特异性结合体,或者是一种分析物的模拟物。上面公开了一些具体的例子,并公开每种类型的装置的操作。
本发明的试验装置的另一些变型也是可能的,例如,所述的任何两构件装置都可以有一个铰接在其中一个可对折构件上的盖子。这个盖子上可以有一个开孔,以便能观察至少一部分色谱介质。
本发明由以下的例子加以说明。这些例子只起说明作用,而不是以任何方式限定本发明的范围。
例1:
用于检测链球菌抗原的装置的结构
构成一种利用针对链球菌A抗原的加标记的抗体检测链球菌A抗原的装置,其结构基本上如图28所示。
图28表示出按照本发明的一种色谱测定装置940,其包括一第一可对折构件942,一个铰接到第一可对折构件942上的第二可对折构件944,和一个铰接到第二可对折构件944上盖子946。第一可对折构件942包含一个色谱介质948。第二可对折构件944包含一个带子952,它张紧在第二可对折构件944的横向上,利用其张力保持住一个滴状接收器950。滴状接收器950在被带子952的张力固定到位后形成一个槽池。第一可对折构件942有一第一窗口942,盖子946有一第二窗口956。
这些可对折构件是用一种硬的不透水的塑料(如聚碳酸脂)制成的。第一和第二可对折构件,以及盖子都大约为3英寸长;第一可对折构件大约2.25英寸宽,而第二可对折构件和盖子都大约为2.375英寸宽。第二可对折构件内衬有一个泡沫橡胶材料的接受件,接受件中开有一个滴状槽池,以便容纳一个签片或其它取样部件。该签片由一个在槽池横向上分别地插入到第二可对折构件中的带子保持在位置上。
色谱介质是一个孔径8微米,长0.5英寸的硝化纤维带条(MSI生产,Westborough,Mass.),用双面胶带(3M公司制造,Minneapolis,Minnesota)固定在塑料背衬上。传导体和吸收体是纤维素条(Ahlstrom Filtration,Holly Springs,Pennsylvania),吸收体的长度为17/32英寸,Ahlstrom等级939,传导体的长度为0.25英寸,Ahlstrom等级1281。检测器点样垫也是Ahlstrom等级1281,并且宽为0.375英寸。检测器点样垫与传导体稍有重叠,传导体又与色谱介质的第一端稍有重叠。色谱介质的第二端则与吸收体稍有重叠。
所要求的试剂被包含在色谱介质和检测器点样垫中,之后用双面胶带组装装置,以将这些组分保持在背衬上。
检测区包括家兔抗链球菌A抗体,它在pH值为7.2的0.001莫尔/升磷酸盐缓冲盐液中的浓度为2毫克/毫升。控制区包括山羊抗家兔IgG,在相同缓冲液中为类似的浓度。抗体溶液被施加到色谱介质的适当区域中并在100°F温度下一个低湿度环境中干燥。色谱介质在过剩阻断溶液(用于ELISA的阻断试剂,德国,曼海姆的Boehringer Mannhein生产,用含有0.2%Tween 20的蒸馏水按1∶10释稀)中渗湿,在100°F下干燥。
检测器点样垫包含家兔抗链球菌抗体,它用40-nm的胶态金颗粒标记。将加标记的抗体施加到检测器点样垫上,用DBN(1.5莫尔/升Tris-HCl,pH7.4,1%(v/v)Tween 20,0.4%(v/v)Brij 35,0.02%(w/v)叠氮化钠(Sodium azide),3毫克/毫升家兔IgG)按1∶1.5释稀加标记的抗体。每次试验将15微升的稀释后的加标记的抗体加入检测的点样垫上。检测器点样垫在100°F下干燥处理30分钟。
例2.
利用例1的装置检测链球菌抗原
例1的装置用于检测链球菌A抗原。将一个其已加有不同数量的链球菌A型细菌的织物涤纶签片插入到试样槽池中。将三滴提取试剂A(0.25%的醋酸,5%的非离子活性剂(Tween)20)和三滴提取试剂B(2莫尔/升的亚硝钠,5%的非离子活性剂)加入到签片中,轻轻地转动签片使之混合,并培养一分钟。然后闭合装置,使第一和第二可对折构件接触,然后将盖子折叠在第一可对折构件上面。在2~5分钟的培养期之后读出结果。在色谱介质的检测区中显示的一条粉红色谱带指示出对链球菌A抗原的检测结果。
例1的装置在一次2分钟的培养期之后可以检测出1×105个链球菌A生物体,而在一次5分钟的培养期之后可以检测出5×104个链球菌A生物体。作为一种比较,Hybritech的Concise的免疫测定(the Coneise immunoassay of Hybritech)(La Jolla,加利福尼亚)在一次5分钟的培养期之后只能检测1×105个链球菌A生物体,但即使其在一次20分钟的培养期之后也不能检测出5×104个链球菌A生物体。类似地,New Horizons的Smart免疫测定在一次7分钟培养期之后只能检测1×105链球菌A生物体,并在一次7分钟的培养期之后给出一个带有5×104链球菌A生物体的不可靠的结果。
例3.
用于检测粪便隐血中的血红蛋白的装置
(预见性的例子)
一种用于检测粪便隐血中的血红蛋白的测定装置按照图1A和1B进行设计制造,并包含在色谱介质的第一端处的任选传导体。一种加标记的特异性结合体以可溶解的形式施加到试样点样垫上。加标记的特异性结合体是用胶态金标记的山羊抗人类抗体。60毫升(μl)的粪便试样被施加到试样点样垫上并使之与结合物混合。将装置闭合,使粪便试样和重新构成的抗体的组合体接触传导体并在色谱介质中移动。让色谱过程进行大约1~5分钟的一段时间。色谱介质包含一个固定抗人类Hb抗体的检测区和一个固定家兔抗山羊IgG抗体的控制区。在检测区和控制区都显现颜色指示出一个阳性结果,亦即粪便试样中存在隐血。在控制区显现颜色而检测区不显现颜色则指示出不存在隐血并且正确实施了该试验。
这种装置能够在约0.2毫升/100克粪便至约17毫升血/100克粪便的浓度范围内检测粪便隐血中的血红蛋白。这种装置不受由过氧化物酶和食物(非人类的)血红蛋白所引起的干扰。
例4.
用三构件测定装置对茶碱进行竞争法免疫测定
设计构造了一种用于检测支气管扩张剂(bronchodilator)茶碱的竞争法免疫测定装置。一个由Schleier和Schuell(Keene,New Hampshire)制造的12微米厚的硝基纤维素膜固定在一块2.5英寸×11/16英寸的双面胶上。一种能够疏水地结合到硝基纤维素上的茶碱模拟物通过将茶碱共价地连接到正常的家兔免疫球蛋白G上面由以下方式制备出来:即一种在2毫升四氢呋喃(tetrahydrofuran)和1毫升N,N-二甲基甲酰胺(dimethylformamide)中加入8-(3-羧基丙基(carboxypropyl)-1,3-二甲基黄嘌呤(dimethylxanthine)(18克,0.068毫克分子)构成的溶液用N-羟基丁二酰胺(hydroxysuccinimide)(17毫克,0.15毫克分子)和二环已基碳二亚胺(dicyclohexylcarbodiimide)(27毫克,0.13毫克分子)进行处理。在将其在室温下放置一昼夜后,将反应混合物冷冻两个小时,然后通过玻璃纤维过滤。反应混合物中的晶体用四氢呋喃冲洗,两种溶液被组合起来。在真空下除去溶剂,用3~4毫升二乙基醚(diethyl ether)冲洗剩余物,除去过量的碳化二亚胺(carbodiimide)。被冲洗的剩余物在1毫升N,N-二甲基甲酰胺中冲洗。正常的家兔IgG(浓度为13.7毫克/毫升的溶液3.75毫升)然后用水稀释到10毫升。将活性N-羟基丁二酰胺酯(hydroxysucciminide ester)慢慢地加入免疫球蛋白G溶液中,接着加入10μl的三乙胺(triethylamine)。这样,反应混合物含有每莫尔蛋白质大约190个活性脂的等同物。
将10μl由茶碱-家兔IgG结合物构成的溶液(在0.05克分子的磷酸盐缓冲剂中,结合物的浓度为1毫克/毫升)经一个Hamilton注射器均匀地施加到2.5英寸长的膜的上部区域中。将该膜在一个烘干机中干燥15分钟,然后浸入一种蛋白质阻断溶液中(0.2%无脂肪干牛奶,0.2%非离子活性剂Tween 20)并再干燥15分钟。茶碱-家兔免疫球蛋白G的线指示剂为膜的顶部。一个1/4英寸长的Ahlstrom cgtosep 799-13(Ahlstrom Filtration)条带被粘到膜的顶部,作为一个传导区域。Ahlstrom 992膜的一第二传导带被固定在膜的下部区域上。然后该膜块被切割成1/4英寸长的条,并储藏起来干燥。
试剂垫是一些切割成Lipore的1/4英寸×1/4英寸的方块(等级9254玻璃纤维过滤器,New Hampshire,Rochester,Lydall技术纸张公司)。第一试剂垫上施加有40μl的浓度为180μg/ml的干燥/稳定缓冲剂(0.5克分子Tris-HCl,pH值7.2,0.1%非离子活性剂Tween 20,0.1%Brij-35,1.0%牛血清清蛋白(bovine serum albumin))的抗茶碱抗体(鼠色单克隆O.E.M.Concepts,Toms River,Now Jersey),并干燥2个小时。第二试剂垫上施加了20μl的利用单克隆茶碱抗体的抗茶碱金结合物(E-Y实验室)的一种工作稀释液,并且第二试剂垫也干燥2个小时。
将膜条固定在一个低板壳中,并且通过壳中的窗口可以看见茶碱-家兔IgG线,如图23所示。含有抗茶碱抗体的第一试剂垫被放置在壳的左三部分上部区域中,以便闭合后,它将接触膜上的上部传导区域,象图23中的点样器764那样。含有抗茶碱-金结合物的第二试剂垫放置在壳的右三部分下部区域中,使之能与膜的下部传导区域接触,如图23中的点样器768那样。一个2厘米×2厘米的Ahlstrom 270方块用作吸收剂垫。并且被放置在壳的右三部分的上部区域,从而当右三部分被闭合在中心上面时,它与上部传导区域接触。
例5.
使用例4的竞争法测定装置实施茶碱测定
(预见性例子)
在一次测定过程中,将40μl的重新构成缓冲液加入第一试剂垫中(重新构成缓冲液的内含物为:1个体积单位的磷酸盐缓冲的盐溶液,0.1M,pH7.2,含有0.8%Tween-20,和1个体积单位的HEPES,2.5mM缓冲剂;pH7.5,含有0.005% Triton x-100,0.003%依地酸四纳(tetrasodim EDEA)和0.05%叠氮化钠)。将相同体积(40μl)的重新构成缓冲液加入第二试剂垫。要测试的试样(10μl)被加入第一试剂垫中并在室温下培养15分钟。将壳的左三部分闭合在中心上面,从而使第一试剂垫上的内含物(包含试样和抗茶碱抗体)施加到色谱介质上。通过窗口很快可以看到一个液体前沿。该前沿在膜上移动到一半路程时(大约在10~20秒钟内),打开壳体,而将测定装置的右三部分(包含第二试剂垫和吸收剂垫)闭合在色谱介质上。装置的右三部分(包含第一试剂垫)也闭合在装置的右三部分和中心上面。如果茶碱存在于浓度为1.25μg/ml血清或更高浓度的试样中,则在1分钟内有一条肉眼可识别的线出现在茶碱-家兔免疫球蛋白G的线处。
例6
阿特拉津(Atrazine)与家兔及山羊免疫球蛋白G的结合物。
为了展示半抗原与免疫球蛋白G结合的可行性,制备有阿特拉津(Atrazine)与家兔及山羊免疫球蛋白G的结合物。对于与家兔免疫球蛋白G的结合物而言,用12毫克的硫羟乙酰基琥珀酸酐(thiolacetylsuccinic anhydride)和20微升的三乙胺(triethylamine)(大约为每莫尔蛋白质有酐(anhydride)的130个克当量)处理家兔IgG(5毫升磷酸盐缓冲的盐溶液中有3.41毫克)。将该溶液置于冰箱中一昼液,然后用2升的水渗析一次,并用2升的磷酸盐缓冲的盐溶液渗析四次。制备出浓度为63毫克/毫升的羟胺氢氯化物(hydroxylamine hydrochloride)溶液。将52微升羟胺(hydroxylamine)溶液(3.3毫克,大约为200克当量)加到8克PBS中的上述制备的家兔IgG中。将溶液在室温下放置45分钟。
一种阿特拉津衍生物(见下面公式I)在浓度为19.7毫克/毫升下溶解到乙腈中,氮分子上的取代基的端甲基(methylgroup)在阿特拉津衍生物中被激活。将这种溶液的一部分(200克当量,16.6毫克,844微升)加入到家兔IgG巯基溶液中,并将其在室温下放置一昼夜。
<I>
采用一种相似的方法将阿特拉津连接到山羊免疫球蛋白G上。用8毫克硫羟乙酰基琥珀酸酐(thiolacetylsuccinic anhydride)和10微升三乙胺(triethylamine)处理山羊IgG(在1.5毫升PBS中有7.8毫克)。将溶液置于冰箱中过一夜,然后象对家兔IgG那样进行渗析处理。渗析后的山羊IgG溶液用10微升羟胺(hydroxylamine)溶液(0.75毫克,约200克当量)处理。该溶液置于室温下保持45分钟。将一第二部分的阿特拉津衍生物(200克当量,3.8毫克,190微升)加入到山羊IgG巯基溶液中并反应一昼夜。在ELISA中,山羊IgG-阿特拉津结合物被固定在聚苯乙烯微型滴定板上,由ELISA表明反应是成功的。
例7
采用加标记的三组分结合体的竞争法免疫测定装置
按照本发明设计构造了一种采用加标记的三构件结合体检测茶碱的竞争法免疫测定装置。该装置是一种类似于图24中所示装置的带有一个盖子的两构件装置,这里所描述的定位是相对于横向定位的装置而言的,如图中所示的那样。
硝基纤维素膜(12微米的孔径)(由Schleicher和Schuell公司制作)固定在2.5英寸×11/16英寸块形双面胶(3M公司制作)上。胶的背侧上已经设置了一块透明塑料。将磷酸盐缓冲盐溶液中的单克隆抗茶碱抗体(10微升)(见例4)用Hamilton注射器均匀地施加到硝基纤维素膜的2.5英寸长度的上部区域横向上,距离指定的顶部5/16英寸处。山羊抗家兔IgG从Pel-FreezBiologicals(Rogers,Arkansas)中获取。纯的IgG从血清中经用辛酸和硫酸铵沉淀而获得。10微升纯化的山羊抗家兔IgG(3.5毫克/毫升,在磷酸盐缓冲盐溶液中)施加到抗茶碱抗体的第一条线之上方,距顶部1/8英寸处。将膜在循环烘干机中干燥10分钟,然后渗入阻断溶液(见例4)中,再干燥15分钟。将一条1/4英寸长的Ahlstrom 1281带(Ahlstrom Filtration)粘到膜的顶部上,作为一个传导区域。一第二传导带,Ahlstrom 992,则固定到下部区域上。然后将膜块切割成1/4英寸的带条。
试剂垫是切割成1/4×1/4英寸的Ahlstrom 1281方块。预先稀释的茶碱-家兔IgG-金(E.Y.实验室)被施加到每一方块上,使这些方块干燥2小时。膜条带固定在壳体中,并且通过窗口只能看见顶部的山羊抗家兔IgG线。将试剂垫放置在壳体的左三部分的下部区域,以便当它闭合在中心板上后,将接触膜上的下部传导区域。一块2厘米×2厘米的Ahlstrom 270方块放置在壳的左三部分的上部区域中,正好在窗口的上方,可以用作一个吸收剂垫。设置的位置使之在闭合时能与膜的上部传导区域接触。
例8
用例7的测定装置检测茶碱(预见性例子)
在用例7的测定装置进行茶碱测定时,将40微升的重新构成缓中液(见例5)加到试剂垫上。将15微升的试样,例如人类血清中的一个茶碱标准量施加到膜条上的上部传导区域中。让液体前沿移动到大约为色谱介质长度的3/4路程的一条标线处,这大约需10秒钟的时间。将壳的左三部分闭合在中心上,接着将右三部分闭合在左三部分上,使液体流动反向。如果茶碱存在于一条界限浓度下,那么2分钟之内就出现一条可见的线。
例9
用于竞争法限制免疫测定的两构件装置
设计构造了一种前述利用硝化纤维膜带、胶粘剂和例4中的试剂垫的两构件装置。该装置类似于前述图27中所示的装置。此处所述的定向相对于横向定向的装置,如图所示。在硝化纤维素色谱介质上固定了两条线。第一条线包含10微升在干燥缓冲液(0.01克分子磷酸盐,3%的蔗糖,0.5%的牛血清清蛋白(bovineserum albumin),0.5%的非离子活性剂Tween 20,0.05%的叠氮化钠(pH7.4)中稀释的亲合力纯化的山羊抗小鼠IgG(O.E.M.Concepts)。第二条线包含10微升处于浓度为1微克/毫升的0.05克分子磷酸盐缓冲液中的例4的茶碱-家兔IgG结合物。将膜置于烘干机中干燥,并渗入蛋白质阻断溶液(0.1克分子Tris-HCl,0.1%BSA,pH7.4)中,然后再干燥。第二可对折构件上的点样器上施加上了20微升在干燥缓冲剂中的一种结合有胶态金(E-Y实验室)的鼠色单克隆抗茶碱抗体(O.E.M.Concepts)的工作稀释液,并被干燥2小时。
为了进行测定,将茶碱(Aldrich Chemical,Milwankee,Wisconsin)溶解在甲醇中,形成一种原料溶液,接着在PBS中或血清中稀释。将试样(30微升)加到第二可对折构件上的点样器上,以溶解抗茶碱-金结合物。培养1分钟之后,将两个可对折构件相互对折叠合,从而点样器与试验条上的下部传导体接触。在2~5分钟之内,一条肉眼可检测的线出现在山羊抗小鼠IgG抗体的区域中,这是通过壳中的窗口能看见的唯一一条线。可以检测到低到1ppb的茶碱浓度。
例10
用于竞争法免疫测定并产生半定量的结果的两构件装置
设计构造了一种按照例9的用于竞争法免疫测定的两构件装置,其不同之处是,除了一条阿特拉津(atrazine)-山羊IgG结合物(例6)线外,检测区含有三条亲合力-纯化的山羊抗小鼠IgG(GAM)(O.E.M.Concepts)线。在色谱介质上最靠近小山羊IgG-阿特拉津结合物的哪条线含有浓度最稀的抗体,浓度为O.5mg/ml;其余两条线会有浓度较大的抗体,其浓度都为1.0mg/ml。鼠色单克隆抗阿特拉津抗体从Agri-Diagnostics公司(位于Cinnaminson,N.J.)购买的。用于抗阿特拉津-金结合物的干燥/稳定作用的缓冲液施加到第二可对折构件上,该缓冲剂是4%的蔗糖,10毫克分子的磷酸盐,0.5%的牛血清清蛋白,0.25%的非离子活性剂Tween 20,0.05%的叠氮化钠,pH7.4。
为了进行测定,将阿特拉当(Supelco公司产,该公司位于Bellefonte Pennsylyania)作为一个标准溶解在甲醇中,并接着在除去离子的水中制备用作工作标准的一些稀释液。将30μl的试样加到第二可对折构件的点样器上。培养1分钟之后,将两个可对折构件相互对折叠合,以便将试样和已溶解的抗阿特拉津-金(结合物)加到色谱介质上。在三分钟之内,试样中的阿特拉当浓度为1~10ppb时在色谱介质上显现出一条线;浓度为11~100ppb显现出两条线,而浓度为101~1000ppb则显现出三条线。
本发明的优点
本发明的色谱测定装置的一个优点在于它由可对折构件的构造。采用可对折构件具有很大的多用性,因为它能够在一些不同的顺序下实施反应。这是因为采用这种可对折构件能够将试剂输送到一个试验条或其它反应组分的精确确定的区域中。另外,采用可对折构件可以将试剂隔离在装置的一些静区(deadvolume)中,保证不浪费试剂,从而以最少的试剂消耗量提供最佳的性能。最后,采用可对折构件时,可以最佳地保持可能被污染的血样,如含有人类免疫缺陷病毒或肝炎病毒的血样。
本发明的测定装置的另一个优点在于,这些装置能够用压力将液体从一个可对折构件传送到另一个可对折构件并使之通过色谱介质,还能够控制施加的压力,使之最佳地适应于要实施的每个测定。这加速了测定过程,并能够在测定装置内实施诸如提取试样的操作。而且它也减少了留在构件中的试剂的静区,从而能够采用较小的试样和较小数量的花费或难以纯化的试剂,如加标记的抗体。
此外,本发明的色谱测定装置能够迅速并且精确地检测在诊断上重要的分析物,如链球菌A和B抗原,用于确定粪便隐血的血红蛋白,和幽门螺杆菌(Helicobacter pylori)抗体,以及诊断上重要的一些半抗原。装置所具有的结构能使试样更加均匀地施加到色谱介质上,并减少了在其它情况会由颗粒试样或带色试样所引起的干扰。采用以可溶解形式的胶态金属标记物使标记过程具有极高的速度,并且能够在试样施加到色谱介质上之前基本上完全形成二元分析物-标记物复合物。这有助于分离污染物,改善测定的实施。此外,装置的外壳的结构和布置保证能抽回过量的含有过量免疫球蛋白的试样,有助于测定的实施,否则会产生干扰。
生物试样如血液、痰或粪便的提取可以直接在装置中进行,减少了必须处理掉的被污染材料的数量,并减少了医生,技术人员或公众被这种污染材料偶然感染的可能性。此外,这种装置能够实施双向色谱分析,进一步提高了精确性,减少了干扰。采用本发明装置的试样方法具有一个很宽的动态范围,并且基本上没有假阴性结果,这种情况在分析物浓度高时可能会在用其它试样方式时产生。
尽管本发明已经针对一些优选方案做了相当详细的描述,但是其它的方案和实施例也是可能的。这些方案包括两构件或三构件装置的其它布置,这些装置是按照这里所描述的基本原理工作的并且采用以下方法中的任何部分:(a)现场提取试样;(b)溶解一种加标记的特异性结合体并迅速结合到分析物上;和(c)布置色谱介质和吸收体,以除去过量的试样,否则可能会产生干扰。这些方案包含适用于夹心法免疫测定也适用于竞争法免疫测定的不同布置的测定装置。特别地,本发明的装置可以利用通过色谱介质的径向流动或周向流动,而不是线性流动。本发明进一步包括一些变型,其中,两构件或三构件装置不是保持在一种永久性固定的布置下,而是可以分离和组合在一起,以进行测定,例如利用电力或磁力,或利用一种可分离的紧固件如一种钩与眼织物,例如Velcro牌商品。因此,本发明的范围由下面的权利要求书来确定。
Claims (91)
1.一种用于检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质;
(ii)一个与色谱介质的第一端有作用性接触的检测器点样垫,检测器点样垫包含有至少一种用于检测分析物的试剂;
(iii)一个传导体,它用于与检测器点样垫有作用性接触并与色谱介质的第一端间接接触而使液体通过;
(iv)一个用于与色谱介质的第二端有作用性接触而吸收液体的吸收体;以及
(b)一第二可对折构件,它包含一个用于接收要测试的试样的试样制备区,第二可对折构件可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,使液体从第二可对折构件传输到第一可对折构件;
其中,第一和第二可对折构件的结构是这样设计的,即当第一和第二可对折构件未对折叠合时,可以将一种试样施加到第二可对折构件上的试样制备区上,而当将第一和第二可对折构件相互对折叠合后,则使试样制备区与传导体接触,而将要测试的试样施加到传导体上,使之流过传导体,然后通过检测器点样垫流到色谱介质的第一端,以将检测分析物的试剂加到试样上,其中通过吸收体吸收液体而帮助液体通过检测器点样垫从传导体流动到色谱介质的第一端。
2.按照权利要求1所述的色谱测定装置,其中,第二可对折构件的试样制备区包含至少一种用于处理试样的试剂。
3.按照权利要求1所述的色谱测定装置,其中,第一可对折构件上的检测器点样垫包含一个针对分析物的、其形式为通过将一种含水液体加到检测器点样垫中而能被溶解的第一特异性结合体,该第一特异性结合体用一种可检测的标记物来标记,而色谱介质进一步包含一个其面积大大小于色谱介质的面积的检测区,该检测区包括其上固定有一种针对分析物的特异性结合体,这样,如果试样中存在分析物,则在检测区中形成一个包括第一特异性结合体、分析物和第二特异性结合体的三元复合物。
4.按照权利要求1所述的色谱测定装置,其中,第一和第二可对折构件由一个不能透过含水液体的铰链连接。
5.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括
(a)权利要求1中所述的色谱测定装置;和
(b)一种针对分析物的、用一种可检测的标记物来标记的、要被施加到检测器点样垫上的特异性结合体。
6.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括
(a)权利要求3中所述的色谱测定装置;和
(b)一种含水液体,用于溶解针对分析物的、用一种可检测的标记物来标记的、要被施加到第一可对折构件上的检测器点样垫上的特异性结合体;
7.一种用于检测和/或测定在一种含水试样中的一种分析物的方法,它包括以下步骤:
(a)在权利要求3中所述的色谱测定装置的第一和第二可对折构件未对折叠合时,将含水试样施加到第二可对折构件的试样制备区上;
(b)在施加试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合,这样,含有含水液体的试样溶解第一可对折构件上的检测器点样垫中的特异性结合体,并且该试样和被溶解的加标记的特异性结合体被施加到第一可对折构件上的传导体上;
(c)然后,使试样和加标记的特异性结合体从检测器点样垫移动并至少通过一部分色谱介质,以使得加标记的特异性结合体通过与色谱介质结合而给出试样中存在分析物和/或分析物的数量的一种可检测的指示,并通过吸收体吸收液体而帮助通过色谱介质的流动;及
(d)然后观测和/或测定已结合到至少一部分色谱介质上的加标记的特异性结合体,以便检测和/或测定分析物。
8.一种用于检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件,它包含:
(i)一个具有一第一端和一第二端的色谱介质;
(ii)一个与色谱介质的第一端有作用性接触的第一检测器点样垫,第一检测器点样垫含有一个针对分析物的、其形式为通过将一种含水液体加到第一检测器点样垫中而能被溶解的第一特异性结合体,该第一特异性结合体用一种可检测的标记物来标记;
(iii)一个传导体,它用于与第一检测器点样垫作用性接触而使液体通过,从而第一检测器点样垫将传导体和色谱介质的第一端进行连接,使液体从传导体通过第一检测器点样垫流动到色谱介质的第一端;和
(iv)一个用于与色谱介质的第二端有作用性接触而吸收液体的吸收体;
(b)一第二可对折构件,其可以连接到第一可对折构件上,从而将第一和第二可对折检测相互对折叠合,而使液体从第二可对折构件传输到第一可对折构件,第二可对折构件包含:
(i)一个用于接收要测定的试样的试样制备区;
(ii)一个与试样制备区有作用性接触的第二检测器点样垫,第二检测器点样垫含有一个针对分析物的、其形式为通过将一种试样加到试样制备区中而能被溶解的第二特异性结合体,该第二特异性结合体用一种可检测的标记物来标记,第二检测器点样垫靠近第二可对折构件上的试样制备区设置,使得将试样施加到试样制备区来溶解第二特异性结合体,从而试样制备区含有一种由试样和第二特异性结合体构成的混合物;以及
其中,第一和第二可对折构件的结构是这样设计的,即当第一和第二可对折构件未对折叠合时,可以将一种试样施加到第二可对折构件的试样制备区上,而当将第一和第二可对折构件相互对折叠合后,则使第二可对折构件上的试样制备区与第一可对折构件上的传导体接触。以将要测试的试样和第二特异性结合体施加到传导体上,使之流过传导体,然后将第一检测器点样垫流到色谱介质的第一端,将第一特异性结合体加到试样和第二特异性结合体上,通过吸收体吸收液体而帮助通过第一检测器点样垫从传导体到色谱介质的第一端的流动。
9.按照权利要求8所述的色谱测定装置,其中,第二可对折构件上的试样制备区包含至少一种用于在将试样施加到试样制备区上之前处理试样的试剂。
10.按照权利要求8所述的色谱测定装置,其中,在第一和第二检测器点样垫中的、针对分析物的第一和第二特异性结合体是相同的,而用于标记第一和第二特异性结合体的可检测的标记物是相同的。
11.按照权利要求10所述的色谱测定装置,其中,相同的可检测的标记物是可以肉眼检测的标记物。
12.按照权利要求8所述的色谱测定装置,其中,第一可对折构件上的色谱介质进一步包含一个其面积大大小于色谱介质的面积的检测区,该检测区包括其上固定有一个针对分析物的第三特异性结合体,这样,如果试样中存在分析物,则在检测区中形成一个包括:(1)第一和第二特异性结合体中的其中一个。(2)分析物,和(3)固定的第三特异性结合体的三元复合物。
13.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括
(a)权利要求8中所述的色谱测定装置;和
(b)一种含水液体,用于溶解至少针对分析物的第一和第二特异性结合体中的其中一个,含水液体将被施加到在第一可对折构件上的第一检测器点样垫和第二可对折构件上的第二检测器点样垫中的至少其中一个上。
14.一种用于检测和/或测定在一种含水试样中的一种分析物的方法,它包括以下步骤:
(a)在权利要求8中所述的色谱测定装置的第一和第二可对折构件未对折叠合时,将含水试样施加到在第二可对折构件的试样制备区上;
(b)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合;这样
(i)第二可对折构件上的试样制备区将试样和第二特异性结合体的混合物施加到第一可对折构件上的传导体上;
(ii)试样和第二特异性结合体的混合物流过传导体,从而到达第一可对折构件上的第一检测器点样垫;
(iii)将试样和第二特异性结合体的混合物施加到第一检测器点样垫,以溶解第一特异性结合体,进而形成一种由试样、第一特异性结合体、和第二特异性结合体构成的混合物;
(c)然后,使试样、加标记的第一特异性结合体和加标记的第二特异性结合体从第一检测器点样垫移动并至少通过一部分色谱介质,使得至少加标记的第一和第二特异性结合体中的其中一个通过与色谱介质结合而给出试样中存在分析物和/或分析物的数量的一种可检测的指示,并通过吸收体吸收液体而帮助通过色谱介质的流动;以及
(d)然后观测和/或测定已结合到至少一部分色谱介质上的至少加标记的第一和第二特异性结合体中的其中一个特异性结合体,以便检测和/或测定分析物。
15.一种用于检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质;
(ii)一个与色谱介质的第一端有作用性接触而能使液体通过的传导体;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,并使液体从第二可对折构件传输到第一可对折构件;第二可对折构件含有:
(i)一个用于接收要测定的试样的试样制备区;和
(ii)一个与在第二可对折构件上的试样制备区隔离开的、用于吸收液体的吸收体;
其中,第一和第二可对折构件的结构是这样设计的,即当第一和第二可对折构件未对折叠合时,可以将一种试样施加到在第二可对折构件上的试样制备区上,而当将第一和第二可对折构件相互对折叠合后,则使在第二可对折构件上的试样制备区与在第一可对折构件上的传导体接触,而将要测试的试样施加到传导体上,使之流过传导体,然后流到色谱介质的第一端,同时使吸收体与色谱介质的第二端有作用性接触,而通过从色谱介质的第二端抽取液体,以帮助液体通过色谱介质从其第一端流动到第二端。
16.一种用于检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个用于接收要测定的试样的试样制备区;
(ii)一个具有一第一端和一第二端的色谱介质;
(iii)一个与试样制备区和色谱介质的第一端有作用性接触而能使液体通过的传导体,从而传导体将试样制备区和色谱介质进行桥接,以使液体从试样制备区流过传导体而流动到色谱介质的第一端;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而使第一和第二可对折构件相互对折叠合,并使液体从第二可对折构件传输到第一可对折构件;第二可对折构件含有:
(i)一个点样器,用于在第一和第二可对折构件相互对折叠合后将液体施加在第一可对折构件上的试样制备区,且它含有一种针对一种分析物的、标记有一种可检测标记物的、其形式为通过向点样器中加入一种含水液体能被溶解的特异性结合体;和
(ii)一个与点样器隔离开的吸收体,用于在第一和第二可对折构件未对折叠合时吸收其中的液体;及
其中,第一和第二可对折构件的结构是这样设计的,即当第一和第二可对折构件未对折叠合时,可以将一种试样施加到第一可对折构件的试样制备区上,而当将第一和第二可对折构件相互对折叠合后,则使在第二可对折构件上的点样器与在第一可对折构件上的试样制备区有作用性接触,从而当已经将一种试样加到试样制备区时,则用于分析物的加标记的特异性结合体就被溶解,并导致在第二可对折构件上的吸收体与第一可对折构件上的色谱介质的第二端有作用性接触,从而从色谱介质中抽取液体,以帮助液体从点样器和试样制备区通过色谱介质的流动。
17.一种用于检测和/或测定试样中一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质;
(ii)一个与色谱介质的第一端有作用性接触的传导体,它能使液体通过;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,使液体从第二可对折构件传输到第一可对折构件;第二可对折构件含有:
(i)一第一点样器,用于在第一和第二可对折构件相互对折叠合后将液体施加到第一可对折构件上的传导体,
(ii)一第二点样器,其在第二可对折构件上与第一点样器分隔开,用于在第一和第二可对折构件相互对折叠合后将液体施加到第一可对折构件上的传导体;和
(iii)一个在第二可对折构件上与第一和第二点样器隔离开的用于吸收其中的液体的吸收体,第一和第二点样器这样地设置在第二可对折构件上,使得当第一和第二可对折构件未对折叠合时,它们相互间不处于有作用性接触,吸收体这样地设置在第二可对折构件上,使得当第一和第二可对折构件相互对折叠合后,它与色谱介质的第二端有作用性接触;
其中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合后,则导致第一可对折构件上的传导体与第二可对折构件上的第二点样器有作用性接触,并导致传导体与第一可对折构件上的第二点样器有作用性接触,由此导致第一和第二点样器相互间间接地有作用性接触,从而第一和第二点样器的内含物流过传导体和色谱介质,通过吸收体抽取液体来帮助液体通过传导体和色谱介质的流动。
18.按照权利要求17所述的色谱测定装置,其中,第二可对折构件上的第一点样器包含一个试样点样垫,用于当第一和第二可对折构件未对折叠合时接收试样,而第二可对折构件上的第二点样器包含一个检测器点样垫,其上至少能施加一种用于检测分析物的检测试剂,由此,当将第一和第二可对折构件相互对折叠合后,试样点样垫和检测器点样垫的内含物则被施加到第一可对折构件上的传导体上。
19.按照权利要求18所述的色谱测定装置,其中,第二可对折构件上的检测器点样垫含有一种针对分析物的、其形式为通过向检测器点样垫中加入一种含水液体能被溶解的第一特异性结合体,第一特异性结合体标记有一种可检测的标记物,而第一可对折构件上的色谱介质进一步包含一个其面积大大小于色谱介质的面积的检测区,该检测区包含其上固定有一个针对分析物的第二特异性结合体,这样,如果试样中存在分析物,则在检测区中形成一个包括第一特异性结合体、分析物和第二特异性结合体的三元复合物。
20.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括:
(a)权利要求17中所述的色谱测定装置;和
(b)一种针对分析物的、标记有一种可检测的标记物的特异性结合体,它将被施加到第二可对折构件上的第二点样器上。
21.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括:
(a)权利要求19中所述的色谱测定装置;和
(b)一种含水液体,用于溶解针对分析物的标记有一种可检测的标记物的特异性结合体,它将被施加到第二可对折构件上的检测器点样垫上。
22.一种用于检测和/或测定在一种含水试样中的一种分析物的方法,它包括以下步骤:
(a)在权利要求19中所述的色谱测定装置的第一和第二可对折构件未对折叠合时,将试样施加到第二可对折构件上的试样点样垫上;
(b)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合;这样,
(i)含有含水液体的试样溶解在第二可对折构件上的检测器点样垫中的特异性结合体;
(ii)由于试样点样垫和在第一可对折构件上的传导体之间的接触以及检测器点样垫和传导体之间的接触,该试样和被溶解的加标记的特异性结合体被施加的色谱介质的第一端上;
(iii)将第二可对折构件上的吸收体置于与在第一可对折构件上的色谱介质的第二端有作用性接触,以帮助液体从试样点样垫和检测器点样垫流过色谱介质,
(c)然后,使试样和加标记的特异性结合体移动并至少通过一部分色谱介质,从而使得加标记的特异性结合体通过与色谱介质结合而给出试样中存在分析物和/或分析物的数量的一种可检测的指示;
(d)然后观测和/或测定已结合到至少一部分色谱介质上的加标记的特异性结合体,以便检测和/或测定分析物。
23.一种用于检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件,它包含:
(i)一个具有一第一端和一第二端的色谱介质;
(ii)一个传导体,它能使与色谱介质的第一端有作用性接触的液体通过;
(iii)一个检测器点样垫,它包含至少一种用于检测分析物的与传导体直接接触的试剂,并这样设置在第一可对折构件上,使之与色谱介质的第一端间接接触;和
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,使液体从第二可对折构件传输到第一可对折构件,第二可对折构件含有:
(i)一个用于在其上施加一种试样的试样点样垫;和
(ii)一个与在第二可对折构件上的试样点样垫隔离开的、用于吸收液体的吸收体;
其中,第一和第二可对折构件的结构是这样设计的,即当第一和第二可对折构件未对折叠合时,可以将一种试样施加到第二可对折构件上的试样点样垫上,而当第一和第二可对折构件相互对折叠合时则导致:
(1)第二可对折构件上的试样点样垫将试样施加到第一可对折构件上的检测器点样垫,由此通过与检测器点样垫直接接触的第一可对折构件上的传导体施加到色谱介质的第一端;及
(2)第二可对折构件上的吸收体与第一可对折构件上的色谱介质的第二端有作用性接触,从而吸收体抽取液体,帮助通过传导体和色谱介质的流动。
24.按照权利要求23所述的色谱测定装置,其中,第一可对折构件上的检测器点样垫含有一种针对分析物的、其形式为通过向检测器点样垫中加入一种含水液体能被溶解的第一特异性结合体,第一特异性结合体标记有一种可检测的标记物,而第一可对折构件上的色谱介质进一步包含一个其面积大大小于色谱介质的面积的检测区,该检测区包括在其上固定有一针对分析物的第二特异性结合体,这样,如果试样中存在分析物,则在检测区中形成一个包括第一特异性结合体、分析物和第二特异性结合体的三元复合物。
25.按照权利要求24所述的色谱测定装置,其中,在将一种试样施加到第二可对折构件上的试样点样垫上之后,该试样点样垫的内含物则包括一种含水液体,而施加到第一可对折构件上的检测器点样垫上的含水液体包括试样点样垫的内含物。
26.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括
(a)权利要求24中所述的色谱测定装置;和
(b)一种针对分析物的、标记有一种可检测的标记物的特异性结合体,它将被施加到第一可对折构件上的检测器点样垫上。
27.一种用于检测和/或测定在一种含水试样中的一种分析物的方法,它包括以下步骤:
(a)在权利要求24中的色谱测定装置的第一和第二可对折构件未对折叠合时,将试样施加到第二可对折构件的试样点样垫上;
(b)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合;这样,
(i)含有含水液体的试样溶解第一可对折构件上的检测器点样垫中的特异性结合体;
(ii)由于试样点样垫和检测器点样垫之间的接触通过在传导体中的流动将该试样和被溶解的加标记的特异性结合体施加到色谱介质的第一端上;
(iii)将第二可对折构件上的吸收体置于与第一可对折构件上的色谱介质的第二端有作用性接触,以帮助液体从试样点样垫和检测器点样垫流过色谱介质;
(c)然后,使试样和加标记的特异性结合体移动并至少通过一部分色谱介质,使得加标记的特异性结合体通过与色谱介质结合而给出试样中存在分析物和/或分析物的数量的一种可检测的指示;及
(d)然后观测和/或测定已结合到至少一部分色谱介质上的加标记的特异性结合体,以便检测和/或测定分析物。
28.一种用于检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质;
(ii)一个检测器点样垫,它包含至少一种用于检测分析物的与色谱介质的第一端直接接触的试剂;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,而使液体从第二可对折构件传输到第一可对折构件;第二可对折构件含有:
(i)一个用于接收一种要测定的试样的试样点样垫;和
(ii)一个与在第二可对折构件上的试样点样垫隔离开的用于吸收液体的吸收体;
其中,第一和第二可对折构件的结构是这样设计的,即当第一和第二可对折构件未对折叠合时,可以将一种试样施加到第二可对折构件上的试样点样垫上,而当第一和第二可对折构件相互对折叠合时则除了检测器点样垫直接与色谱介质的第一端相邻的区域外,将使第一可对折构件上的检测器点样垫与第二可对折构件上的试样点样垫相接触,以使液体从试样点样垫传输到检测器点样垫,同时使从试样点样垫直接传输到色谱介质的液体最少;和
其中,将第一和第二可对折构件相互对折叠合后导致:
(1)要测试的试样被施加到第一可对折构件上的检测器点样垫,然后施加到色谱介质的第一端;及
(2)第二可对折构件上的吸收体和色谱介质的第二端有作用性接触,从而通过吸收体抽取液体而帮助通过检测器点样垫和色谱介质的流动。
29.按照权利要求28所述的色谱测定装置,其中,第一可对折构件上的检测器点样垫含有一种针对分析物的、其形式为通过向检测器点样垫中加入一种含水液体能被溶解的第一特异性结合体,第一特异性结合体标记有一种可检测的标记物,第一可对折构件上的色谱介质进一步包含一个其面积大大小于色谱介质的面积的检测区,该检测包括在其上固定有一个针对分析物的第二特异性结合体,这样,如果试样中存在分析物,则在检测区中形成一个包括第一特异性结合体、分析物和第二特异性结合体的三元复合物。
30.如权利要求28所述的色谱测定装置,其中,在将一种试样施加到第二可对折构件上的试样点样垫上之后,该试样点样挚内含物则包括一种含水液体,而施加到第一可对折构件上的检测器点样垫上的含水液体包括试样点样垫的传输到检测器点样垫上的内含物。
31.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括:
(a)权利要求28中所述的色谱测定装置;和
(b)一种针对分析物的、标记有一种可检测的标记物的特异性结合体,它将被施加到第一可对折构件上的检测器点样垫上。
32.一种用于检测和/或测定在一种含水测试试样中的一种分析物的方法,它包括以下步骤:
(a)在权利要求30中所述的色谱测定装置的第一和第二可对折构件未对折叠合时,将试样施加到第二可对折构件的试样点样垫上;
(b)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合;这样,
(i)含有含水液体的试样溶解在第一可对折构件上的检测器点样垫中的特异性结合体;
(ii)由于第二可对折构件上的试样点样垫和第一可对折构件上的检测器点样垫之间的接触,将该试样和被溶解的加标记的特异性结合体施加到色谱介质的第一端上;
(iii)将第二可对折构件上的吸收体置于与第一可对折构件上的色谱介质的第二端有作用性接触,以帮助液体从试样点样垫和检测器点样垫流过色谱介质,
(c)然后,使试样和加标记的特异性结合体移动并至少通过一部分色谱介质,使得加标记的特异性结合体通过与色谱介质结合而给出试样中存在分析物和/或分析物的数据的一种可检测的指示;以及
(d)然后观测和/或测定已结合到至少一部分色谱介质上的加标记的特异性结合体,以便检测和/或测定分析物。
33.一种检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质;
(ii)一个设在第一可对折构件上的能让液体通过的传导体,当第一和第二可对折构件未对折叠合时,它不与色谱介质的第一端有作用性接触;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而可以将第一和第二可对折构件相互对折叠合,而将液体从第二可对折构件传输到第一可对折构件上;第二可对折构件包含:
(i)一第一点样器,用于在第一和第二可对折构件相互对折叠合时,将液体施加到第一可对折构件上的传导体上;
(ii)一个在第二可对折构件上与第一点样器分隔开的第二点样器,用于在第一和第二可对折构件相互对折叠合时,将液体施加到第一可对折构件上的传导体上;
(iii)一个吸收体,用于吸收与处在第二可对折构件上的第一和第二点样器隔离开的液体,第一和第二点样器则是设置在第二可对折构件上,这样当第一和第二可对折构件未对折叠合时,它们之间不处于有作用性接触,
其中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则:
(1)导致第一可对折构件上的传导体与第二可对折构件上的第一点样器有作用性接触,传导体与第二可对折构件上的第二点样器有作用性接触,以及第二点样器与色谱介质的第一端有作用性接触,由此使第一和第二点样器相互间处于间接的有作用性接触,从而使第一和第二点样器的内含物被施加到色谱介质,进而第一和第二点样器的内含物流过色谱介质,
(2)导致第二可对折构件上的吸收体与色谱介质的第二端有作用性接触,从而通过吸收体抽取液体,来帮助液体从第一和第二点样器流过传导体和色谱介质。
34.按照权利要求33所述的色谱测定装置,其中,第二可对折构件上的第一点样器包含一个试样点样垫,用于当第一和第二可对折构件未对折叠合时在其上施加一个试样,而第二可对折构件上的第二点样器包含一个检测器点样垫,其上至少能施加一种检测试剂,由此在将第一和第二可对折构件相互对折叠合后,试样点样垫和检测器点样垫的内含物通过传导体施加到色谱介质上。
35.按照权利要求34所述的色谱测定装置,其中,第一可对折构件上的检测器点样垫包含一个针对分析物的、其形式为通过将一种含水液体加到检测器点样垫中而能被溶解的第一特异性结合体,该第一特异性结合体用一种可检测的标记物来标记,而第一可对折构件上的色谱介质进一步包含一个其面积大大小于色谱介质的面积的检测区,该检测区包括在其上固定有一种针对分析物的特异性结合体,这样,如果试样中存在分析物,则在检测区中形成一个包括第一特异性结合体、分析物和第二特异性结合体的三元复合物。
36.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括:
(a)权利要求33中所述的色谱测定装置;和
(b)一种针对分析物的、标记有一种可检测的标记物的特异性结合体,它将被施加到第二可对折构件上的第二点样器上。
37.一种用于检测和/或测定在一种含水测试试样中的一种分析物的方法,它包括以下步骤:
(a)在权利要求34中所述的色谱测定装置的第一和第二可对折构件未对折叠合时,将试样施加到第二可对折构件的第一点样器上;
(b)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合;这样
(i)含有含水液体的试样溶解在第二可对折构件上的检测器点样垫中的加标记的特异性结合体;
(ii)通过第一可对折构件上的传导体将该试样和被溶解的加标记的特异性结合体施加到色谱介质的第一端上:
(iii)将第二可对折构件上的吸收体置于与色谱介质的第二端有作用性接触,以帮助液体从试样垫和检测器点样垫流过传导体和色谱介质;
(c)然后,使试样和加标记的特异性结合体移动并至少通过一部分色谱介质,从而使得加标记的特异性结合体通过与色谱介质结合而给出存在分析物和/或分析物的数量的一种可检测的指示;及
(d)然后观测和/或测定已结合到至少一部分色谱介质上的加标记的特异性结合体,以便检测和/或测定分析物。
38.一种检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质;
(ii)一个与色谱介质的第一端有作用性接触的能让液体通过的传导体;
(iii)一个用于吸取与色谱介质的第一端有作用性接触的液体的吸收体;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,并使液体从第二可对折构件传输到第一可对折构件,第二可对折构件含有一个点样器,用于在第一和第二可对折构件相互对折叠合时,将液体施加到第一可对折构件上的传导体上,点样器被分成两个扇区:
(i)一第一扇区,其含有一个针对分析物的、其形式为在第一和第二可对折构件未对折叠合时通过将一种含水液体加到点样器中而能被溶解的第一特异性结合体,该特异性结合体用一种可检测的标记物来标记;和
(ii)一个不合有针对分析物的特异性结合体的第二扇区;及
其中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时则使第二可对折构件上的点样器的第一扇区,而不是第二扇区与第一可对折构件上的传导体直接接触,点样器的第二扇区通过第一扇区与传导体间接接触,将点样器的第一扇区的内含物施加到色谱介质上,接着将点样器的第二扇区的内含物施加到色谱介质上,吸收体从色谱介质抽取液体,以帮助液体从点样器流过传导体和色谱介质。
39.按照权利要求38所述的色谱测定装置,其中,第一可对折构件上的色谱介质进一步包含一个其面积大大小于色谱介质的面积的检测区,该检测区包括在其上固定有一种针对分析物的第二特异性结合体,这样,如果试样中存在分析物,则在检测区中形成一个包括第一特异性结合体、分析物和第二特异性结合体的三元复合物。
40.一种用于检测和/或测定在一种含水测试试样中的一种分析物的方法,它包括以下步骤:
(a)在权利要求38中所述的色谱测定装置的第一和第二可对折构件未对折叠合时,将试样施加到第二可对折构件的点样器上,从而将试样施加到点样器的第一扇区和第二扇区上;
(b)在点样器上施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合,这样,
(i)施加到第二可对折构件的点样器的第一扇区上的试样含有溶解点样器的第一扇区中的加标记的特异性结合体的含水液体;
(ii)通过在第一可对折构件上的传导体存在于点样器的第一扇区中的该试样和被溶解的加标记的特异性结合体施加到色谱介质的第一端上;
(iii)在从点样器的第一扇区将该试样和被溶解的加标记的特异性结合体施加到色谱介质的第一端上之后,通过传导体将存在于点样器的第二扇区中的试样施加到色谱介质的第一端;
(c)然后,使来自点样器的第一扇区的试样和加标记的特异性结合体和后面跟随的来自点样器的第二扇区的试样移动并至少通过一部分色谱介质,使得加标记的特异性结合体的标记物通过与色谱介质结合而给出存在分析物和/或分析物的数量的一种可检测的指示,并使得来自点样器的第二扇区试样从至少一部分色谱介质上冲洗掉至少某种未与分析物结合的加标记特异性结合体,通过吸收体从色谱介质抽取液体以帮助液体流过色谱介质;以及
(d)然后观测和/或测定已结合到至少一部分色谱介质上的标记物,以便检测和/或测定分析物。
41.一种检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质,和它在上面的一个大大小于其面积的分散区域中固定有分析物或它的一个免疫学模拟物;
(ii)一个与色谱介质的第一端有作用性接触的能让液体通过的第一传导体;和
(iii)一个与色谱介质的第二端有作用性接触的能让液体通过的第二传导体;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,而使液体从第二可对折构件传输到第一可对折构件,第二可对折构件含有一第一点样器,用于在第一和第二可对折构件相互对折叠合时,将液体施加到第一可对折构件上的第一传导体上,第一点样器含有一个针对分析物的、其形式为通过将一种第一含水液体加到第一点样器中而能被溶解的第一特异性结合体;
(c)一第三可对折构件,它可以连接到第一可对折构件上,从而将第一和第三可对折构件相互对折叠合,而使液体从第三可对折构件传输到第一可对折构件,第三可对折构件含有
(i)一第二点样器,用于在第一和第三可对折构件相互对折叠合时,将液体施加到第一可对折构件上的第二传导体上,第二点样器含有一个针对分析物的、其形式为通过将一种第二含水液体加到第二点样器中而能被溶解的第二特异性结合体,第二特异性结合体用一种可检测的标记物来标记;
(ii)一个与在第三可对折构件上的第二点样器隔离开用于吸收液体的吸收体;
其中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使第一可对折构件上的第一传导体与第二可对折构件上的第一点样器有作用性接触,从而通过第一传导体使第一点样器的内含物被施加到色谱介质上,并至少流过一部分色谱介质;及
其中,第一和第三可对折构件的结构是这样设计的,即当将第一和第三可对折构件相互对折叠合时则使第三可对折构件上的吸收体与第一可对折构件上的第一传导体有作用性接触,从而通过第一传导体从色谱介质中抽取液体并使第三可对折构件上的第二点样器与第一可对折构件上的第二传导体有作用性接触,从而第二点样器的内含物被施加到色谱介质,并至少流过一部分色谱介质,这部分色谱介质与第一和第二可对折构件接触色谱介质时抽吸施加到色谱介质上的第一点样器的内含物所通过的部分是重叠的。
42.按照权利要求41所述的色谱测定装置,其中,第一和第二特异性结合体每一个都是对分析物具有特异性的抗体。
43.按照权利要求41所述的色谱测定装置,其中,固定的分析物或它的模拟物包括共价地连接到一种缺乏对分析物的特异性结合活性的蛋白质上的分析物。
44.一种用于检测和/或测定试样中的一种分析物的试验箱,它在分开的容器中包括:
(a)权利要求41中所述的色谱测定装置;和
(b)一第二含水液体,用于溶解在第三可对折构件上的第二点样器中所含的针对分析物的第二特异性结合体。
45.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在权利要求41中所述的色谱测定装置的第一可对折构件与第二可对折构件或第三可对折构件未对折叠合时,将试样施加到第二可对折构件的第一点样器上,该试样包含第一含水液体;
(b)当第一和第三可对折构件未对折叠合时,将一种重新构成液体施加到第三可对折构件上的第二点样器上,重新构成液体包含第二含水液体;
(c)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合,由于第一点样器和第一传导体之间接触从而该试样和针对分析物的被溶解特异性结合体被施加到第一传导体上,然后被施加到色谱介质的第一端上。
(d)然后,使试样和被溶解的第一特异性结合体移动并至少通过一部分色谱介质;
(e)然后,将第一和第二可对折构件分离开,使之不再叠合到一起;
(f)然后,将第一和第三可对折构件相互对折叠合,通过第二点样器和第二吸收体之间接触,从而被溶解的加标记的第二特异性结合体被施加到第一可对折构件上的第二传导体上,然后被施加到色谱介质的第二端上,同时使第三可对折构件上的吸收体与第一传导体有作用性接触,以帮助液体从第二点样器流过色谱介质;
(g)然后让被溶解的加标记的第二特异性结合体移动并至少流过一部分色谱介质,这部分色谱介质与试样和被溶解的第一特异性结合体被抽吸所通过的色谱介质部分是重叠的,从而当测试试样中存在分析物时,加标记的第二特异性结合体就结合到固定在分散区域中的分析物或它的免疫学模拟物上;和
(h)然后观测和/或测定已结合到分散区域上的第二特异性结合体,以便检测和/或测定分析物。
46.按照权利要求45所述的方法,进一步包括以下步骤:在将试样施加到第二可对折构件上的第一点样器上后,对色谱测定装置进行培养,以便促进分析物和第一特异性结合体之间的反应。
47.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在权利要求41中所述的色谱测定装置的第一可对折构件与第二可对折构件或第三可对折构件未对折叠合时,将一第一重新构成液体施加到第二可对折构件上的第一点样器上;
(b)当第一可对折构件与第二可对折构件或第三可对折构件未对折叠合时,将试样施加到在权利要求41中所述的色谱测定装置的第一点样器上,第一重新构成液体和试样的组合物包括第一含水液体,
(c)当第一可对折构件与第三可对折构件未对折叠合时,将一第二重新构成液体施加到第三可对折构件上的第二点样器上,第二重新构成液体包含第二含水液体;
(d)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合,由于第一点样器和第一传导体之间接触从而该试样和针对分析物的被溶解的第一特异性结合体被施加到第一传导体上,然后被施加到色谱介质的第一端上;
(e)然后,使试样和被溶解的第一特异性结合体移动并至少通过一部分色谱介质;
(f)然后,将第一和第二可对折构件分离开,使之不再叠合到一起;
(g)然后,将第一和第三可对折构件相互对折叠合,通过第二点样器和第二吸收体之间接触,使被溶解的加标记的第二特异性结合体被施加到第一可对折构件上的第二传导体,然后被施加到色谱介质的第二端上,同时使第三可对折构件上的吸收体与第一传导体有作用性接触,以帮助液体从第二点样器流过色谱介质;及
(h)然后让被溶解的加标记的第二特异性结合体移动并至少流过一部分色谱介质,这部分色谱介质与试样和被溶解的第一特异性结合体被抽吸所通过的色谱介质部分是重叠的,从而当试样中存在在分析物时,加标记的第二特异性结合体就结合到固定在分散区域中的分析物或它的免疫学模拟物上;和
(i)然后观测和/或测定已结合到分散区域上的第二特异性结合体,以便检测和/测定分析物。
48.按照权利要求47所述的方法,其进一步包括以下步骤:在将试样施加到第二可对折构件上的第一点样器上后,对色谱测定装置进行培养,以便促进分析物和第一特异性结合体之间的反应。
49.一种由一种竞争免疫测定法检测和/或测定试样中的一种免疫学上单价的分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质,且在它上面的一些其面积都大大小于色谱介质的分散区域和非重叠区域中固定有:
(A)用于分析物的一种特异性结合体;和
(B)一种次特异性结合体,该次特异性结合体能够与一个对分析物缺乏亲合力的特异性结合体对中的一个组分相结合,该次特异性结合体设置得比第一特异性结合体更靠近色谱介质的第一端;
(ii)一个能让与色谱介质的第一端有作用性接触的液体通过的第一传导体;和
(iii)一个能让色谱介质的第二端有作用性接触的液体通过的第二传导体;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,而使液体从第二可对折构件传输到第一可对折构件,第二可对折构件含有:
(i)一个点样器,用于在第一和第二可对折构件相互对折叠合时,将液体施加到第二传导体上,并含有一种分析物的模拟物,该分析物的模拟物包括与一个对分析物缺乏亲合力的特异性结合体对中的一个组分共价地相结合的、并能被次特异性结合体结合的分析物,特异性结合体对中的那个组分标记有一种可检测的标记物,分析物的模拟物的形式为通过将一种含水液体加到点样器中而能被溶解;
(ii)一个在与第二可对折构件上的点样器隔离开的用于吸收液体的吸收体;
其中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件对折叠合时则使第二传导体与点样器有作用性接触,从而将点样的内含物施加到色谱介质,并至少流过一部分色谱介质,同时使吸收体与第一传导体有作用性接触,以从色谱介质中抽取液体。
50.按照权利要求49所述的色谱测定装置,其进一步包括一个铰接在第一可对折构件上的盖子,从而当将第一和第二可对折构件相互对折叠合时,盖子可以折叠在第一和第二可对折构件上面,盖子上开有孔口,用以在将第一和第二可对折构件相互对折叠合并且将盖子折叠在第一和第二可对折构件上面后观察至少一部分色谱介质。
51.按照权利要求49所述的色谱测定装置,其中,第一特异性结合体是一个对分析物具有特异性的抗体,而次特异性结合体是一个能够结合对分析物缺乏特异性的一种抗体的第二抗体。
52.按照权利要求49所述的色谱测定装置,其中,分析物的模拟物包括共价地连接到一种免疫球蛋白上的分析物。
53.按照权利要求49所述的色谱测定装置,其中,固定在色谱介质上的次特异性结合体的面积被分成至少两个分散的且不重叠的带区,每个带区中的次特异性结合体的数量是确定的,从而由分析物的模拟物所结合的带区数目指示出结合到检测区中的分析物的模拟物的数量,因而指示出试样中的分析物的浓度。
54.一种用于检测和/或测定试样中的一种免疫学上单价的分析物的试验箱,它在分开的容器中包括:
(a)权利要求49中所述的色谱测定装置;和
(b)一种含水液体,用于溶解将被施加到第二可对折构件的点样器上的分析物的模拟物。
55.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在权利要求49中所述的色谱测定装置的第一可对折构件与第二可对折构件未对折叠合时,将一种重新构成液体施加到第二可对折构件上的点样器上,重新构成液体包括用于重新构成第二特异性结合体的含水液体;
(b)当第一可对折构件和第二可对折构件未对折叠合时,将试样施加到色谱测定装置的第一可对折构件的第一传导体上;
(c)然后,使试样移动而至少通过一部分色谱介质,包括固定在色谱介质的一个分散区域中的针对分析物的第一特异性结合体;
(d)然后,将第一和第二可对折构件相互对折叠合,由于点样器和第二传导体之间接触,使被溶解的加标记的第二特异性结合体施加到第二传导体上,然后被施加到色谱介质的第二端上;
(e)然后让被溶解的加标记的分析物的模拟物移动并至少通过一部分色谱介质,这部分色谱介质与试样被抽吸所通过的色谱介质部分是重叠的,包括固定有试剂的两个分散区域,从而当试样中存在分析物时,加标记的分析物的模拟物就结合到次特异性结合体上;和
(f)然后观测和/或测定已结合到含有固定的次特异性结合体的分散区域上的加标记的分析物的模拟物,以便检测和/或测定分析物。
56.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在权利要求53中所述的色谱测定装置的第一可对折构件与第二可对折构件未对折叠合时,将一种重新构成液体施加到第二可对折构件上的点样器上,重新构成液体包括用于重新构成第二特异性结合体的含水液体;
(b)当第一可对折构件与第二可对折构件未对折叠合时,将试样施加到色谱测定装置的第一可对折构件的第一传导体上;
(c)然后,使试样移动而至少通过一部分色谱介质,包括固定在色谱介质的一个分散区域中的针对分析物的第一特异性结合体,
(d)然后,将第一和第二可对折构件相互对折叠合,由于点样器和第二传导体之间接触,使被溶解的加标记的第二特异性结合体施加到第二传导体上,然后被施加到色谱介质的第二端上;
(e)然后让被溶解的加标记的分析物的模拟物移动并至少通过一部分色谱介质,这部分色谱介质与试样被抽吸所通过的色谱介质部分是重叠的,包括固定有试剂的两个分散区域,从而当试样中存在分析物时,加标记的分析物的模拟物就结合到次特异性结合体上;和
(f)然后观测和/或测定在含有固定的次特异性结合体的分析区域内的两个或多个带区中的加标记的分析物的模拟物,以便检测和/或测定分析物,加标记的分析物的模拟物所结合的带区的数目随着分析物的浓度的增加而增加。
57.一种由一种竞争免疫测定法检测和/或测定试样中的一种免疫学上单价的分析物的色谱测定装置,其包括
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质,且在它上面的一些其面积都大大小于色谱介质的分散区域和非重叠区域中固定有:
(A)对于分析物的一种特异性结合体;和
(B)一种次特异性结合体,该次特异性结合体能够与一个对分析物缺乏亲合力的特异性结合体对中的一个组分相结合,该次特异性结合体设置得比第一特异性结合体更靠近色谱介质的第一端;
(ii)一个与色谱介质的第一端有作用性接触的能让液体通过的第一传导体,第一传导体能起着一第一点样器的功能;和
(iii)一个与色谱介质的第二端有作用性接触的能让液体通过的第二传导体;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,而使液体从第二可对折构件传输到第一可对折构件,第二可对折构件含有:
(i)一第二点样器,用于在第一和第二可对折构件相互对折叠合时,将液体施加到第二传导体上,并含有一种分析物的模拟物,该分析物的模拟物包括与一个对分析物缺乏亲合力的特异性结合体对中的一个组分相结合的、并能被次特异性结合体结合的分析物,特异性结合体对中的那个组分上标记有一种可检测的标记物,分析物的模拟物的形式为通过将一种含水液体加到第二点样器中而能被溶解;和
(ii)一个与第二可对折构件上的第二点样器隔离开的、用于吸收液体的第一吸收体;
(c)一个有吸收液体的第二吸收体的第三可对折构件;
其中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时则使第二点样器与第一传导体有作用性接触,以及使第一吸收体与第二传导体有作用性接触,从而通过第二传导体从色谱介质中抽取液体;以及
其中,第一和第三可对折构件的结构是这样设计的,即当将第一和第三可对折构件相互对折叠合时则使第二吸收体与第一传导体和色谱介质有作用性接触,从而通过第一传导体从色谱介质中柚取液体。
58.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在权利要求57中所述的色谱测定装置的第一可对折构件与第二可对折构件未对折叠合时,将试样施加到第一可对折构件的第一传导体上;
(b)将一种重新构成液体施加到色谱测定装置的第二可对折构件上的第二点样器上,以溶解第二点样器中的加标记的分析物的模拟物;
(c)使试样移动而至少通过一部分色谱介质,包括固定在色谱介质上的针对分析物的特异性结合体和次特异性结合体,
(d)然后,将第三和第一可对折构件相互对折叠合,由于点样器和第一传导体之间以及点样器和色谱介质之间的接触使第三可对折构件上的第二吸收体与第一可对折构件上的第一传导体和色谱介质直接接触,而从色谱介质中抽取液体;
(e)然后,将第二和第一可对折构件相互对折叠合,使第二可对折构件上的第二点样器与第一可对折构件上的第一传导体有作用性接触,和使第二可对折构件上的第一吸收体与第一可对折构件上的第二传导体有作用性接触,由于第二点样器和第一传导体之间以及第一吸收体和第二传导体之间的接触,从而将被溶解的加标记的分析物的模拟物施加到第一传导体上,然后施加到色谱介质的第一端上;
(f)然后让溶解的加标记的分析物的模拟物移动至少通过含有对分析物的特异性结合体和次特异性结合体的那部分色谱介质;和
(g)然后观测和/或测定结合到次特异性结合体上的加标记的分析物的模拟物,以便检测和/或测定分析物。
59.一种由一种竞争免疫测定法检测和/或测定试样中的一种免疫学上单价的分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质,且在它上面的一些其面积都大大小于色谱介质的分散区域和非重叠区域中固定有:
(A)一种能够与生物素特异性结合的物质,该生物素选自由抗生物素蛋白(avidin)、抗生物蛋白链菌素(streptavidin),抗-生物素(anti-biotin)抗体,和它们的衍生物组成的组;和
(B)一种次特异性结合体,该次特异性结合体能够与一个三元的复合物特异性的相结合,该三元的复合物包括:(1)分析物,(2)一个对分析物缺乏亲合力的特异性结合体对中的一个组分,该组分共价地结合到分析物上,和(3)一个结合到特异性结合体对中的这个组分上的可检测的标记物;
(ii)一个与色谱介质的第一端有作用性接触的能让液体通过的第一传导体;和
(iii)一个与色谱介质的第二端有作用性接触的能让液体通过的第二传导体;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,而使液体从第二可对折构件传输到第一可对折构件,第二可对折构件含有:一第一点样器,用于将液体施加到第一传导体上,第一点样器含有一种针对分析物的、形成为通过一种含水试样加到第一点样器中而能被溶解的第一特异性结合体,第一特异性结合体共价地结合到生物素上,第一特异性结合体不能被次特异性结合体结合;
(c)一第三可对折构件,它可以连接到第一可对折构件上,从而将第一和第三可对折构件相互对折叠合,而使液体从第三可对折构什传输到第一可对折构件,第三可对折构件含有:
(i)一个含有三元复合物的用于将液体加到第二传导体上的第二点样器,三元复合物的形式为通过将一种第二含水液体加到第二点样器中而能被溶解;
(ii)一个与在第三可对折构件上的第二点样器隔离开的、用于吸收液体的吸收体;及
其中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使第一传导体与第一点样器有作用性接触,从而将第一点样器的内含物施加到色谱介质,并至少被抽吸通过一部分色谱介质,其中,第一和第三可对折构件的结构是这样设计的,即当将第一和第三可对折构件相互对折叠合时,则使吸收体与第一传导体接触,从而从色谱介质中抽取液体,并使第二点样器与第二传导体有作用性接触,从而将第二传导体的内含物施加到色谱介质上,并至少被抽吸通过与第一点样器的内含物被抽吸通过的那部分色谱介质相重叠的一部分色谱介质。
60.按照权利要求59所述的色谱测定装置,其中,第一特异性结合体是一种抗分析物的抗体。
61.按照权利要求60所述的色谱测定装置,其中,在三元复合物中的特异性结合体对的那个组分是家兔免疫球蛋白G,而第二特异性结合体是山羊抗家兔IgG。
62.按照权利要求59所述的色谱测定装置,其中,能够特异性地结合生物素的基底是抗生物蛋白链菌素。
63.按照权利要求59所述的色谱测定装置,其中,固定在色谱介质上的次特异性结合体的区域分成至少两个分散的且不重叠的带区,每个带区中的次特异性结合体的数量是确定的,从而由三元复合物结合的带区的数目指示出结合到检测区上的三元复合物的数量,由此指示出试样中原始分析物的浓度。
64.一种用于检测和/或测定试样中的一种免疫学上单价的分析物的试验箱,它在分开的容器中包括:
(a)权利要求59中所述的色谱测定装置,和
(b)一种用于溶解三元复合物的第二含水液体,它将被施加到第三可对折构件上的第二点样器上。
65.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在权利要求59中所述的色谱测定装置的第一可对折构件与第二可对折构件未对折叠合时,将包含一种第一含水液体的试样施加到色谱测定装置的第一点样器上;
(b)在第一可对折构件与第三可对折构件未对折叠合时,将一种包含一种第二含水液体的重新构成液体施加到第二点样器上;
(c)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合,从而通过第一传导体将试样和被溶解的针对分析物的第一特异性结合体施加到色谱介质的第一端;
(d)然后,使试样和被溶解的第一特异性结合体移动而至少通过一部分色谱介质;
(e)然后,将第一和第二可对折构件分离开,使之不再叠合到一起;
(f)然后,将第一和第三可对折构件相互对折叠合,使被溶解的三元复合物通过第二传导体施加到色谱介质的第二端;
(g)然后让被溶解的三元复合物移动并至少通过一部分色谱介质,这部分色谱介质与试样和被溶解的第一特异性结合体被抽吸所通过的色谱介质部分是重叠的,从而当测试试样与分析物存在时,三元复合物就结合到固定在第二分散区域中的第二特异性结合体上;和
(h)然后观测和/或测定结合到第二分散区域中的加标记特异性结合体,以便检测和/或测定分析物。
66.按照权利要求65所述的方法,其进一步包括以下步骤:在试样施加到第一点样器上后,对色谱测定装置进行培养,以便促进分析物和第一特异性结合体之间的反应。
67.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在权利要求59中所述的色谱测定装置的第一可对折构件和第二可对折构件未对折叠合时,将一种第一重新构成液体施加到色谱测定装置的第一点样器上;
(b)在第一可对折构件和第二可对折构件未对折叠合时,将试样施加到权利要求66中所述的色谱测定装置的第一点样器上,试样和第一重新构成液体的组合物包括第一含水液体,
(c)在第一可对折构件和第三可对折构件未对折叠合时,将一种第二重新构成液体施加到第二点样器上,第二重新构成液体包括第二含水液体;
(d)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合,从而通过第一传导体将试样和被溶解的针对分析物的第一特异性结合体施加到色谱介质的第一端;
(e)然后,使试样和被溶解的第一特异性结合体移动而至少通过一部分色谱介质;
(f)然后,将第一和第二可对折构件分离开,使之不再叠合在一起;
(g)然后,将第一和第三可对折构件相互对折叠合,使被溶解的三元复合物通过第二传导体施加到色谱介质的第二端;
(h)然后让被溶解的三元复合物移动并至少通过一部分色谱介质,这部分色谱介质与试样和被溶解的第一特异性结合体被抽吸所通过的色谱介质部分是重叠的,从而当测试试样与分析物存在时,三元复合物就结合到固定在第二分散区域中的第二特异性结合体上;和
(i)然后观测和/或测定结合到第二分散区域中的加标记的特异性结合体,以便检测和/或测定分析物。
68.按照权利要求67所述的方法,其进一步包括以下步骤:在将试样施加到第一点样器上后,对色谱测定装置进行培养,以便促进分析物和第一特异性结合体之间的反应。
69.一种用于检测和/或测定在一种测试试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在第一可对折构件与第二可对折构件未对折叠合时,将包括一种第一含水液体的试样施加到权利要求63中所述的色谱测定装置的第一点样器上;
(b)在第一可对折构件与第三可对折构件未对折叠合时,将一种包括一种第二含水液体的重新构成液体施加到第二点样器上;
(c)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合,从而通过第一传导体将试样和被溶解的针对分析物的第一特异性结合体施加到色谱介质的第一端;
(d)然后,使试样和被溶解的第一特异性结合体移动而至少通过一部分色谱介质;
(e)然后,将第一和第二可对折构件分离开,使之不再叠合到一起;
(f)然后,将第一和第三可对折构件相互对折叠合,使被溶解的三元复合物通过第二传导体施加到色谱介质的第二端;
(g)然后让被溶解的三元复合物移动并至少通过一部分色谱介质,这部分色谱介质与试样和被溶解的第一特异性结合体被抽吸所通过的色谱介质部分是重叠的,从而当测试试样与分析物存在时,三元复合物就结合到固定在第二分散区域中的第二特异性结合体上;和
(h)然后观测和/或测定结合到含有固定的次特异性结合体的分散区域内的两个或多个带区上的加标记的分析物的模拟物,以便检测和/或测定分析物,加标记的分析物的模拟物所结合的带区的数目随着分析物的浓度的增加而增加。
70.一种由一种竞争免疫测定法检测和/或测定试样中的一种免疫学上单价的分析物的色谱测定装置,其包括:
(a)一第一可对折构件;它包含:
(i)一个具有一第一端和一第二端的色谱介质,且在它上面的一些其面积都大大小于色谱介质的分散区域和非重叠区域中固定有:
(A)一种能够结合针对分析物的特异性结合体分析物的模拟物;和
(B)一种次特异性结合体,该次特异性结合体能够与一个对分析物具有亲合力的特异性结合体对中的一个组分相结合,次特异性结合体本身缺乏对分析物的亲合力;
(ii)一个能让与色谱介质的第一端有作用性接触的液体通过的传导体;
(b)一第二可对折构件,它可以连接到第一可对折构件上,从而将第一和第二可对折构件相互对折叠合,而使液体从第二可对折构件传输到第一可对折构件,第二可对折构件有一个点样器,点样器含有一种针对分析物的、形式为通过将一种含水液体加到点样器中而能被溶解的特异性结合体;和
其中,第一和第二可对折构件的结构是这样设计的,即当将第一和第二可对折构件相互对折叠合时,则使传导体与点样器有作用性接触,从而将点样器的内含物施加到色谱介质上并使之至少通过一部分色谱介质。
71.按照权利要求70所述的色谱测定装置,其中,第一特异性结合体是对分析物有特异性的抗体。
72.按照权利要求70所述的色谱测定装置,其中,分析物的模拟物包括共价地连接到一种蛋白上的分析物,该蛋白对分析物或分析物的特异性结合体缺乏特异性结合活性。
73.按照权利要求71所述的色谱测定装置,其中,在不涉及分析物的抗体的抗原结合点是品种-特异性相互作用的基础上,次特异性结合体与对分析物有特异性的抗体相结合。
74.按照权利要求70所述的色谱测定装置,其中,第一可对折构件进一步包含一个用于吸收与色谱介质的第二端有作用性接触的液体的吸收体,以帮助液体通过色谱介质的流动。
75.按照权利要求70所述的色谱测定装置,其中,第二可对折构件进一步包含一个用于吸收从点样器分离出的液体的吸收体,该吸收体是这样设置在第二可对折构件上,使得当第一和第二可对折构件相互对折叠合后,吸收体则与色谱介质的第二端有作用性接触,以帮助液体通过色谱介质的流动。
76.按照权利要求70所述的色谱测定装置,其中,固定在色谱介质上的次特异性结合体的区域分成至少两个分散的且不重叠的带区,每个带区的次特异性结合体的数量是确定的,从而由针对分析物的加标记的特异性结合体结合的带区的数目指示出结合到检测区上的针对分析物的加标记的特异性结合体的数量,由此指示出试样中分析物的数量。
77.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在第一可对折构件与第二可对折构件未对折叠合时,将包括含水液体的试样施加到权利要求70所述的色谱测定装置的点样器上;
(b)在施加了试样之后,将色谱测定装置的第一和第二可对折构相互对折叠合,从而通过传导体将试样和被溶解的针对分析物的加标记的特异性结合体施加到色谱介质的第一端;
(c)然后,使试样和被溶解的加标记的特异性结合体移动而至少通过一部分色谱介质,该部分至少包含分析物的模拟物和次特异性结合体的那些分散的和不重叠的区域;和
(d)然后观测和/或测定结合到特异性结合体的分散区域中的加标记的特异性结合体,以便检测和/或测定分析物。
78.一种用于检测和/或测定在一种含水试样中的一种免疫学上单价的分析物的方法,它包括以下步骤:
(a)在第一可对折构件与第二可对折构件未对折叠合时,将包含含水液体的试样施加到权利要求76中所述的色谱测定装置的点样器上;
(b)在施加了试样之后,将色谱测定装置的第一和第二可对折构件相互对折叠合,从而通过传导体将试样和被溶解的针对分析物的加标记的特异性结合体施加到色谱介质的第一端;
(c)然后,使试样和被溶解的加标记的特异性结合体移动而至少通过一部分色谱介质,该部分至少包含分析物的模拟物和次特异性结合体的那些分散的和不重叠的区域;和
(d)观测和/或测定结合到含有固定的次特异性结合体的分散区域内的两个或多个带区上的加标记的特异性结合体,以便检测和/或测定分析物,加标记的分析物的模拟物所结合的带区的数目随着分析物的浓度的增加而增加。
79.按照权利要求4,19,35,39,41,49,57,59或70所述的色谱测定装置,其中,可检测的标记物是一种可肉眼检测的标记物。
80.一种检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)至少两个基本上平面的可对折构件,其中的一个基本上平面的可对折构件在其表面上有一个色谱介质;和
(b)用于将可对折构件相互对折叠合并在其上施加压力的部件,该压力大到足以能沿着一个大致垂直于可对折构件的方向将液体从一个可对折构件传输到另一个可对折构件,从而将一种试样施加到色谱介质上,以检测和/或测定其上的分析物,用于将可对折构件相互对折叠合的部件使可对折构件有作用性接触用以传输液体,从而可以在可对折构件未对折叠合时将一种试样施加到其中的一个可对折构件上,然后在可对折构件相互对折叠合后使试样从其中的一个可对折构件传输到另一个可对折构件。
81.按照权利要求80所述的色谱测定装置,其中,至少基本上平面的可对折构件中的一个可对折构件上面有一个试样制备区,用于在可对折构件未对折叠合时接收要测试的一种试样。
82.按照权利要求80所述的色谱测定装置,其中,
(i)至少其中的一个构件的上面含有一种针对分析物的、加标记的、其形式为通过加入一种含水液体能被溶解的第一特异性结合体,含水液体可以是一种试样,第一加标记的特异性结合体设置在构件上能与试样中的分析物起反应的地方;和
(ii)色谱介质上面含有一个其上固定一种针对分析物的、未加标记的、第二特异性结合体的检测区,检测区的面积大大小于色谱介质的面积,从而如果在试样中存在分析物时,则在检测区中形成一个包括:(1)第一加标记的特异性结合体;(2)分析物;和(3)固定在第二特异性结合体的三元复合物,由此实施一种夹心法免疫测定。
83.按照权利要求80所述的色谱测定装置,其中,在色谱介质上面的一个大大小于色谱介质面积的区域中含有一个特异性结合体对的一个组分,该特异性结合体对选自由一种分析物或其模拟物和一种针对分析物的特异性结合体构成的组,从而测定装置能够对试样中的分析物实施一种竞争法免疫测定。
84.按照权利要求80所述的色谱测定装置,其中,基本上平面的可对折构件中的一个可对折构件上面具有至少两个分开的且不接触的色谱介质,从而能够在其上面对分析物至少同时实施两个检测和/或测定。
85.按照权利要求80所述的色谱测定装置,其中,在将试样施加到色谱介质上后,利用一种可肉眼检测的加标记的组分检测和/或测定分析物,该可肉眼检测的加标记的组分选自于由一种连接到一种可肉眼检测的标记物上的分析物或其模拟物和一种连接到一种可肉眼检测的标记物上的针对分析物的特异性结合体构成的组。
86.一种检测和/或测定试样中的一种分析物的色谱测定装置,其包括:
(a)至少三个基本上平面的可对折构件,其中的一个基本上平面的可对折构件在其表面上有一个色谱介质,该色谱介质具有一第一端和一第二端;和
(b)用于以至少两种不同的组合中成对地将可对折构件相互对折叠合并在其上施加压力的部件,该压力大到足以能沿着一个大致垂直于可对折构件的方向将液体从一个可对折构件传输到另一个可对折构件上,从而将一种试样施加到色谱介质上并通过色谱介质从第一端流动到第二端,以检测和/或测定色谱介质上的分析物,用于将可对折构件相互对折叠合的部件使可对折构件以成对的组合方式有作用性接触而传输液体,从而可以在可对折构件未对折叠合时将一种试样施加到其中的一个可对折构件上,然后在将可对折构件相互对折叠合后使试样从其中的一个可对折构件传输到另一个可对折构件;和
(c)至少一个用于将液体施加到色谱介质上的点样器和一个用于吸收液体的吸收体,它们位于其中的一个可对折构件上并这样地设置,即当由使可对折构件相互对折叠合的部件将其上设有点样器和吸收体的可对折构件与其上设有色谱介质的可对折构件相互对折叠合后,则将一第二液体施加到色谱介质上并通过色谱介质从第二端流动到第一端,这种从第二端到第一端的流动由吸收体吸收液体来帮助完成,由此使通过色谱介质的流动反向,在接着通过色谱介质的流动的反向后对分析物作出检测和/或测定。
87.按照权利要求86所述的色谱测定装置,其中,至少其中的一个基本上平面的可对折构件的上面有一个试样制备区。
88.按照权利要求86所述的色谱测定装置,其中:
(i)至少其中的一个构件的上面含有一种针对分析物的、加标记的、其形式为通过加入一种含水液体能被溶解的第一特异性结合体,含水液体可以是一种试样,第一加标记的特异性结合体设置在构件上能与试样中的分析物有反应的位置;和
(ii)色谱介质上面含有一个检测区,其上固定一种针对分析物的、未加标记的、第二特异性结合体,检测区的面积大大小于色谱介质的面积,从而如果在试样中存在分析物时,则在检测区中形成一个包括:(1)第一加标记的特异性结合体;(2)分析物;和(3)固定的第二特异性结合体的三元复合物,由此实施一种夹心法免疫测定。
89.按照权利要求86所述的色谱测定装置,其中,在色谱介质上面的一个大大小于色谱介质面积的区域中含有一个特异性结合体对的一个组分,该特异性结合体对选自于由一种分析物或其模拟物和一种针对分析物的特异性结合体构成的组,从而测定装置能够对试样中的分析物实施一种竞争法免疫测定。
90.按照权利要求86所述的色谱测定装置,其中,基本上平面的可对折构件中的一个可对折构件上面具有至少两个分开的不接触的色谱介质,每个色谱介质都有一第一端和一第二端,从而能够在其上面对分析物至少同时实施两次检测和/或测定。
91.按照权利要求86所述的色谱测定装置,其中,在将试样施加色谱介质上后,利用一种可肉眼检测的加标记的组分检测和/或测定分析物,该可肉眼检测的加标记的组分选自于由一种连接到一种可肉眼检测的标记物上的分析物或其模拟物和一种连接到一种可肉眼检测的标记物上的针对分析物的特异性结合体构成的组。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US08/040,430 | 1993-03-31 | ||
| US08/040,430 US5877028A (en) | 1991-05-29 | 1993-03-31 | Immunochromatographic assay device |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1124524A true CN1124524A (zh) | 1996-06-12 |
Family
ID=21910947
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN94192256A Pending CN1124524A (zh) | 1993-03-31 | 1994-03-31 | 由可相互对折叠合的构件构成的色谱测定装置 |
Country Status (21)
| Country | Link |
|---|---|
| US (1) | US5877028A (zh) |
| EP (1) | EP0692097B1 (zh) |
| JP (1) | JP3506178B2 (zh) |
| KR (1) | KR960702109A (zh) |
| CN (1) | CN1124524A (zh) |
| AT (1) | ATE177206T1 (zh) |
| AU (1) | AU678461B2 (zh) |
| BG (1) | BG100104A (zh) |
| BR (1) | BR9406755A (zh) |
| DE (1) | DE69416828T2 (zh) |
| DK (1) | DK0692097T3 (zh) |
| ES (1) | ES2131191T3 (zh) |
| FI (1) | FI954591A (zh) |
| HU (1) | HUT73379A (zh) |
| NO (1) | NO953872L (zh) |
| NZ (1) | NZ263754A (zh) |
| OA (1) | OA10233A (zh) |
| PL (1) | PL310953A1 (zh) |
| RU (1) | RU2124729C1 (zh) |
| SK (1) | SK122795A3 (zh) |
| WO (1) | WO1994023300A1 (zh) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7270995B2 (en) | 2000-05-25 | 2007-09-18 | Nichirei Biosciences | Analyzing device |
| CN100427950C (zh) * | 2001-08-03 | 2008-10-22 | 麦美华股份有限公司 | 快速诊断装置,分析方法及多功能缓冲液 |
| CN100430726C (zh) * | 1999-10-25 | 2008-11-05 | 松下电器产业株式会社 | 免疫色谱试验片及色谱分析方法 |
| CN101426898B (zh) * | 2006-03-31 | 2013-03-06 | 拉敏纳股权公司 | 一体式筛选和确认设备 |
| CN104865340A (zh) * | 2015-05-12 | 2015-08-26 | 华南理工大学 | 一种用于进行薄层板手动浸渍操作的装置 |
| CN105319278A (zh) * | 2014-07-08 | 2016-02-10 | 哈尔滨飞机工业集团有限责任公司 | 一种超声对比试块嵌入件放置方法 |
| CN109187962A (zh) * | 2017-10-07 | 2019-01-11 | 贾晓轻 | 血液样本免疫层析诊断试纸条、试剂盒和检测方法 |
| CN114384190A (zh) * | 2016-06-29 | 2022-04-22 | 安捷伦科技有限公司 | 用于降低柱流失携带效应的方法和系统 |
Families Citing this family (102)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5607863A (en) * | 1991-05-29 | 1997-03-04 | Smithkline Diagnostics, Inc. | Barrier-controlled assay device |
| US5468648A (en) * | 1991-05-29 | 1995-11-21 | Smithkline Diagnostics, Inc. | Interrupted-flow assay device |
| US5648274A (en) * | 1991-05-29 | 1997-07-15 | Smithkline Diagnostics, Inc. | Competitive immunoassay device |
| EP0832430B1 (en) * | 1995-05-09 | 2006-07-26 | Beckman Coulter, Inc. | Devices and methods for separating cellular components of blood from liquid portion of blood |
| US5747351A (en) * | 1995-06-07 | 1998-05-05 | Smithkline Diagnostics, Inc. | Immunochemical-based test device with lift and twist specimen full tab |
| AUPO071396A0 (en) * | 1996-06-28 | 1996-07-25 | Chandler, Howard Milne | Chromatographic assay or test device |
| ATE286252T1 (de) * | 1996-10-25 | 2005-01-15 | Idexx Lab Inc | Immunoassay-vorrichtung mit teilbarem gehäuse |
| US6156272A (en) * | 1997-06-06 | 2000-12-05 | All Technologies Corporation | Method and apparatus for urine self-test intended for use in a toilet |
| CA2713206C (en) * | 1997-10-06 | 2012-06-19 | Enterix Inc. | Apparatus and method for analyte detection |
| US6602719B1 (en) | 1999-03-26 | 2003-08-05 | Idexx Laboratories, Inc. | Method and device for detecting analytes in fluids |
| US6511814B1 (en) * | 1999-03-26 | 2003-01-28 | Idexx Laboratories, Inc. | Method and device for detecting analytes in fluids |
| US6551842B1 (en) * | 1999-03-26 | 2003-04-22 | Idexx Laboratories, Inc. | Method and device for detecting analytes in fluids |
| ES2269171T3 (es) * | 1999-07-26 | 2007-04-01 | The Government Of The United States Of America, As Represented By The Secretary, Department Of Heal | Dispositivo en capas con regiones de captura para analisis celular. |
| US6727073B1 (en) * | 1999-11-19 | 2004-04-27 | Binax, Inc. | Method for detecting enteric disease |
| US6316205B1 (en) | 2000-01-28 | 2001-11-13 | Genelabs Diagnostics Pte Ltd. | Assay devices and methods of analyte detection |
| US20020004246A1 (en) * | 2000-02-07 | 2002-01-10 | Daniels Robert H. | Immunochromatographic methods for detecting an analyte in a sample which employ semiconductor nanocrystals as detectable labels |
| US6699722B2 (en) | 2000-04-14 | 2004-03-02 | A-Fem Medical Corporation | Positive detection lateral-flow apparatus and method for small and large analytes |
| US20020102717A1 (en) * | 2000-12-09 | 2002-08-01 | Hadeed Erika Lynn | Refillable, reusable pregnancy test |
| US6890484B2 (en) | 2001-05-18 | 2005-05-10 | Acon Laboratories, Inc. | In line test device and methods of use |
| US6565808B2 (en) | 2001-05-18 | 2003-05-20 | Acon Laboratories | Line test device and methods of use |
| US20040191889A1 (en) * | 2001-06-15 | 2004-09-30 | Lalit Mahajan | See through testing device |
| US6818456B2 (en) * | 2001-07-20 | 2004-11-16 | Varian, Inc. | Color contrast system for lateral flow immunoassay tests |
| US7300633B2 (en) * | 2001-07-25 | 2007-11-27 | Oakville Hong Kong Company Limited | Specimen collection container |
| SE0103072D0 (sv) * | 2001-09-17 | 2001-09-17 | Pharmacia Diagnostics Ab | Multi-analyte assay device with multi-spot detection zone |
| US8481334B1 (en) | 2001-11-06 | 2013-07-09 | Charm Sciences, Inc. | Method of attaching a ligand to a solid support |
| AU2003274629B2 (en) * | 2002-10-11 | 2009-03-12 | Zbx Corporation | Diagnostic devices |
| US7560272B2 (en) * | 2003-01-04 | 2009-07-14 | Inverness Medical Switzerland Gmbh | Specimen collection and assay container |
| DE10330982A1 (de) | 2003-07-09 | 2005-02-17 | Prisma Diagnostika Gmbh | Vorrichtung und Verfahren zur simultanen Bestimmung von Blutgruppenantigenen |
| DE10330981B4 (de) | 2003-07-09 | 2010-04-01 | Medion Diagnostics Ag | Vorrichtung und Verfahren zur simultanen Durchführung von Blutgruppenbestimmung, Serumgegenprobe und Antikörpersuch-Test |
| US7517495B2 (en) * | 2003-08-25 | 2009-04-14 | Inverness Medical Switzerland Gmbh | Biological specimen collection and analysis system |
| US7238538B2 (en) * | 2003-09-19 | 2007-07-03 | Freitag Helmut E | Chromatographic assay device and methods |
| EP1692501B1 (en) * | 2003-11-14 | 2016-01-06 | Alere Switzerland GmbH | Rapid sample analysis and storage devices and methods of use |
| US7588733B2 (en) * | 2003-12-04 | 2009-09-15 | Idexx Laboratories, Inc. | Retaining clip for reagent test slides |
| US7410808B1 (en) | 2003-12-08 | 2008-08-12 | Charm Sciences, Inc. | Method and assay for detection of residues |
| US20050136531A1 (en) * | 2003-12-17 | 2005-06-23 | Kimberly-Clark Worldwide, Inc. | Folded substrate with applied chemistry |
| US20050163658A1 (en) * | 2004-01-28 | 2005-07-28 | Naishu Wang | Interrupted, vertical flow testing device |
| US7488450B2 (en) * | 2004-03-04 | 2009-02-10 | Beckman Coulter, Inc. | Analyte collection and detection devices |
| JP2007530946A (ja) * | 2004-03-23 | 2007-11-01 | クイデル コーポレイション | ハイブリッド相ラテラルフロー・アッセイ |
| FI20040825A0 (fi) * | 2004-06-15 | 2004-06-15 | Ani Biotech Oy | Suodatinväline, sen käyttö, menetelmä ja kitti |
| US20060019406A1 (en) * | 2004-07-23 | 2006-01-26 | Ning Wei | Lateral flow device for the detection of large pathogens |
| US20060068500A1 (en) * | 2004-09-28 | 2006-03-30 | Kimberly-Clark Worldwide, Inc. | Detecting yeast infections using a lateral flow assay |
| WO2006042004A2 (en) * | 2004-10-06 | 2006-04-20 | Binax, Inc. | Sample receiving device and methods of use thereof |
| US7442557B1 (en) | 2004-10-22 | 2008-10-28 | Idexx Laboratories, Inc. | Bi-directional flow assay device with reagent bridge |
| EP1657550A1 (en) * | 2004-11-10 | 2006-05-17 | Coris Bioconcept SPRL | Double-sided device for multiplex dipstick immunodiagnostic |
| US7387890B2 (en) * | 2004-12-16 | 2008-06-17 | Chembio Diagnostic Systems, Inc. | Immunoassay devices and use thereof |
| US7396689B2 (en) * | 2005-02-04 | 2008-07-08 | Decision Biomarkers Incorporated | Method of adjusting the working range of a multi-analyte assay |
| US8669052B2 (en) * | 2008-06-10 | 2014-03-11 | Rapid Pathogen Screening, Inc. | Lateral flow nucleic acid detector |
| WO2006088904A2 (en) * | 2005-02-16 | 2006-08-24 | Ping Gao | Fecal sample test device and methods of use |
| US7189522B2 (en) | 2005-03-11 | 2007-03-13 | Chembio Diagnostic Systems, Inc. | Dual path immunoassay device |
| WO2006098804A2 (en) | 2005-03-11 | 2006-09-21 | Chembio Diagnostic Systems, Inc. | Dual path immunoassay device |
| CA2612450C (en) * | 2005-06-28 | 2014-04-29 | Zbx Corporation | Membrane array and analytical device |
| WO2007054714A2 (en) * | 2005-11-12 | 2007-05-18 | Platform Diagnostics Limited | Agglutination assay |
| JP2009524799A (ja) * | 2005-11-30 | 2009-07-02 | インバーネス・メデイカル・スウイツツアーランド・ゲゼルシヤフト・ミツト・ベシユレンクテル・ハフツング | 流体試料中の分析物の存在または量を検出するための装置およびその方法 |
| US7794656B2 (en) | 2006-01-23 | 2010-09-14 | Quidel Corporation | Device for handling and analysis of a biological sample |
| US7871568B2 (en) | 2006-01-23 | 2011-01-18 | Quidel Corporation | Rapid test apparatus |
| US20090215159A1 (en) * | 2006-01-23 | 2009-08-27 | Quidel Corporation | Device for handling and analysis of a biological sample |
| GB2435512A (en) * | 2006-02-23 | 2007-08-29 | Mologic Ltd | A binding assay and assay device |
| US20080014657A1 (en) * | 2006-07-12 | 2008-01-17 | Beckton Dickinson And Company | Use of Albumin, Bovine, P-Aminophenyl N-Acetyl B-D Glucosaminide as a Control Line for an Immunoassay Device |
| CA2658795A1 (en) * | 2006-07-26 | 2008-02-07 | Abon Biopharm (Hangzhou) Co., Ltd. | A test device for detecting an analyte in a liquid sample |
| AU2007302626B2 (en) | 2006-09-28 | 2013-09-26 | The Macfarlane Burnet Institute For Medical Research And Public Health Limited | A method of diagnosis and kit therefor |
| WO2008061130A2 (en) * | 2006-11-15 | 2008-05-22 | Ucp Biosciences, Inc. | An improved collecting and testing device and method of use |
| GB2452076A (en) * | 2007-08-23 | 2009-02-25 | Mologic Ltd | Detection of enzymes by detecting binding of substrate recognition molecules to modified substrates |
| US9274056B2 (en) * | 2007-12-03 | 2016-03-01 | Robert Hudak | Use of non-chelated fluorochromes in rapid test systems |
| US8058073B2 (en) * | 2008-01-30 | 2011-11-15 | Ortho-Clinical Diagnostics, Inc. | Immunodiagnostic test cards having indicating indicia |
| US8247220B2 (en) * | 2008-02-01 | 2012-08-21 | Kimberly-Clark Worldwide, Inc. | Optical indicator for detecting bacterial pathogens |
| US9068981B2 (en) | 2009-12-04 | 2015-06-30 | Rapid Pathogen Screening, Inc. | Lateral flow assays with time delayed components |
| US20130196310A1 (en) | 2008-05-20 | 2013-08-01 | Rapid Pathogen Screening, Inc. | Method and Device for Combined Detection of Viral and Bacterial Infections |
| US8815609B2 (en) | 2008-05-20 | 2014-08-26 | Rapid Pathogen Screening, Inc. | Multiplanar lateral flow assay with diverting zone |
| US8962260B2 (en) | 2008-05-20 | 2015-02-24 | Rapid Pathogen Screening, Inc. | Method and device for combined detection of viral and bacterial infections |
| US8609433B2 (en) * | 2009-12-04 | 2013-12-17 | Rapid Pathogen Screening, Inc. | Multiplanar lateral flow assay with sample compressor |
| JP5117928B2 (ja) * | 2008-05-27 | 2013-01-16 | 富士フイルム株式会社 | イムノクロマトグラフデバイス |
| US20110086359A1 (en) * | 2008-06-10 | 2011-04-14 | Rapid Pathogen Screening, Inc. | Lateral flow assays |
| US20100022916A1 (en) | 2008-07-24 | 2010-01-28 | Javanbakhsh Esfandiari | Method and Apparatus for Collecting and Preparing Biological Samples for Testing |
| US9234889B1 (en) | 2008-12-18 | 2016-01-12 | Charm Sciences, Inc. | Method and test strip for detecting residues |
| US8453525B2 (en) * | 2009-02-09 | 2013-06-04 | Healthpoint Diagnostix, Inc. | Plasma sample collection device |
| EP2269737B1 (en) * | 2009-07-02 | 2017-09-13 | Amic AB | Assay device comprising serial reaction zones |
| ES2523768T3 (es) * | 2009-12-04 | 2014-12-01 | Rapid Pathogen Screening Inc. | Ensayo de flujo lateral multiplanar con compresor de muestras |
| CN105044320B (zh) | 2010-03-25 | 2017-02-22 | 艾博生物医药(杭州)有限公司 | 测试液体样本中被分析物的检测装置 |
| ES2945032T3 (es) | 2010-05-06 | 2023-06-28 | Charm Sciences Inc | Dispositivo de incubadora con lector |
| US8956859B1 (en) | 2010-08-13 | 2015-02-17 | Aviex Technologies Llc | Compositions and methods for determining successful immunization by one or more vaccines |
| US8603835B2 (en) | 2011-02-10 | 2013-12-10 | Chembio Diagnostic Systems, Inc. | Reduced step dual path immunoassay device and method |
| JP6043718B2 (ja) | 2011-07-01 | 2016-12-14 | 株式会社ダイセル | スポット検出用セット、スポット検出方法、及び被転写シート |
| WO2013058767A1 (en) * | 2011-10-21 | 2013-04-25 | Empire Technology Development Llc | Materials and methods to detect pyrimidine-pyrimidine dimer formation |
| US20150293131A1 (en) * | 2012-04-02 | 2015-10-15 | Astute Medical, Inc. | Methods and compositions for diagnosis and prognosis of sepsis |
| US20130309656A1 (en) * | 2012-05-17 | 2013-11-21 | David C. Davis | Antibody detection method and device for a saliva sample from a non-human animal |
| CA3153763A1 (en) | 2013-03-11 | 2014-10-09 | Meso Scale Technologies, Llc. | Improved methods for conducting multiplexed assays |
| US9068968B2 (en) | 2013-07-02 | 2015-06-30 | Daniel Gordon DRURY | Urine analysis device, method and system |
| US9352313B2 (en) | 2013-12-31 | 2016-05-31 | Hangzhou Ditu Technology Co., Ltd. | Device for collecting and testing analyte in a liquid sample |
| US10416158B2 (en) | 2014-03-11 | 2019-09-17 | Wisconsin Alumni Research Foundation | Peptide MHCII tetramers to detect endogenous calnexin specific CD4 T cells |
| CA2944488C (en) | 2014-04-02 | 2023-03-21 | Chembio Diagnostic Systems, Inc. | Immunoassay utilizing trapping conjugate |
| EP3132265A4 (en) * | 2014-04-14 | 2018-02-14 | Abreos Biosciences, Inc. | Lateral flow immunoassay |
| WO2016025726A1 (en) * | 2014-08-13 | 2016-02-18 | Vivebio, Llc | An analytic membrane array, and plasma separation device incorporating the same |
| US20160116466A1 (en) | 2014-10-27 | 2016-04-28 | Chembio Diagnostic Systems, Inc. | Rapid Screening Assay for Qualitative Detection of Multiple Febrile Illnesses |
| US10808287B2 (en) | 2015-10-23 | 2020-10-20 | Rapid Pathogen Screening, Inc. | Methods and devices for accurate diagnosis of infections |
| WO2018031887A1 (en) | 2016-08-12 | 2018-02-15 | Abreos Biosciences, Inc. | Detection and quantification of natalizumab |
| US10458974B2 (en) | 2017-06-09 | 2019-10-29 | Optimum Imaging Diagnostics LLC | Universal testing system for quantitative analysis |
| RU178938U1 (ru) * | 2017-06-20 | 2018-04-23 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Амурская государственная медицинская академия" Министерства здравоохранения Российской Федерации | Устройство для подготовки цитологического мазка биологических жидкостей к проведению экспресс-анализа клеточного состава |
| US11293839B2 (en) | 2018-08-16 | 2022-04-05 | Epitope Biotechnology Co., Ltd. | Device for fecal sample collection and extraction |
| US11918936B2 (en) | 2020-01-17 | 2024-03-05 | Waters Technologies Corporation | Performance and dynamic range for oligonucleotide bioanalysis through reduction of non specific binding |
| EP4127721A1 (en) * | 2020-03-31 | 2023-02-08 | 3M Innovative Properties Company | Diagnostic device |
| EP3904876A1 (en) * | 2020-04-28 | 2021-11-03 | Universitat Politècnica De Catalunya | A foldable fluidic device and method for biomarker detection in body fluids |
| EP4260065A1 (en) * | 2020-12-11 | 2023-10-18 | Huvepharma Inc. | Lateral flow assay for detection of monensin |
Family Cites Families (395)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1926299A (en) * | 1932-11-04 | 1933-09-12 | Nelson Knitting Company | Carton |
| US3078031A (en) * | 1961-07-18 | 1963-02-19 | Foils Packaging Corp | Reclosure lock |
| US3186623A (en) * | 1961-09-05 | 1965-06-01 | Waldorf Paper Prod Co | Carton tear strip opener |
| NL125235C (zh) * | 1965-04-15 | |||
| US3307770A (en) * | 1965-07-26 | 1967-03-07 | Waldorf Paper Prod Co | Butter cartons and the like |
| US3420205A (en) * | 1966-03-23 | 1969-01-07 | Miles Lab | Indicating device |
| US3437449A (en) * | 1966-06-08 | 1969-04-08 | Manley J Luckey | Breath alcohol determination |
| GB979193A (en) * | 1966-10-19 | 1965-01-01 | Konstantin Sergeevich Evstropi | Optical glasses |
| US3720760A (en) * | 1968-09-06 | 1973-03-13 | Pharmacia Ab | Method for determining the presence of reagin-immunoglobulins(reagin-ig)directed against certain allergens,in aqueous samples |
| USRE31006E (en) * | 1968-09-24 | 1982-08-03 | Akzona Incorporated | Process for the demonstration and determination of reaction components having specific binding affinity for each other |
| US3811840A (en) * | 1969-04-01 | 1974-05-21 | Miles Lab | Test device for detecting low concentrations of substances in fluids |
| US3993451A (en) * | 1970-07-28 | 1976-11-23 | Miles Laboratories, Inc. | Test for a given constituent in a liquid |
| US3932220A (en) * | 1970-08-11 | 1976-01-13 | Liotta Lance A | Method for isolating bacterial colonies |
| US4067774A (en) * | 1971-05-14 | 1978-01-10 | Syva Company | Compounds for enzyme amplification assay |
| US3723064A (en) * | 1971-07-26 | 1973-03-27 | L Liotta | Method and device for determining the concentration of a material in a liquid |
| IT1006557B (it) * | 1971-09-08 | 1976-10-20 | Bagshawe Kenneth Dawson | Cella di reazione particolarmente utile in prove di radioimmunita |
| US3902964A (en) * | 1971-12-13 | 1975-09-02 | U S Medical Research And Dev I | Method of and apparatus for chemically separating plasma or serum from formed elements of blood |
| US3867517A (en) * | 1971-12-21 | 1975-02-18 | Abbott Lab | Direct radioimmunoassay for antigens and their antibodies |
| US3798004A (en) * | 1972-04-18 | 1974-03-19 | Ames Yissum Ltd | Test device |
| US4054646A (en) * | 1973-07-30 | 1977-10-18 | General Electric | Method and apparatus for detection of antibodies and antigens |
| US4012198A (en) * | 1972-07-25 | 1977-03-15 | Burroughs Wellcome Co. | Immunodiffusion device |
| US3989591A (en) * | 1973-01-15 | 1976-11-02 | Liotta Lance A | Test method for separating and/or isolating bacteria and tissue cells |
| FI49086C (fi) * | 1973-01-25 | 1975-03-10 | Matti Antero Reunanen | Radioimmunologinen määritysmenetelmä. |
| US3966897A (en) * | 1973-04-02 | 1976-06-29 | Marine Colloids, Inc. | Medium for use in bioassay and method of using same |
| IL42105A (en) * | 1973-04-25 | 1976-08-31 | Yissum Res Dev Co | Process for determination of triiodothyronine |
| CA1023251A (en) * | 1973-06-22 | 1977-12-27 | The Standard Oil Company | Method and paper test strip for determining low levels of lead in hydrocarbon fuels |
| US3992158A (en) * | 1973-08-16 | 1976-11-16 | Eastman Kodak Company | Integral analytical element |
| US4039652A (en) * | 1973-10-11 | 1977-08-02 | Miles Laboratories, Inc. | Column method of immunoassay employing an immobilized binding partner |
| US3949064A (en) * | 1973-10-26 | 1976-04-06 | Baxter Laboratories, Inc. | Method of detecting antigens or antibodies |
| US3935074A (en) * | 1973-12-17 | 1976-01-27 | Syva Company | Antibody steric hindrance immunoassay with two antibodies |
| GB1451669A (en) * | 1974-01-02 | 1976-10-06 | Radiochemical Centre Ltd | Protein staining |
| US3926564A (en) * | 1974-02-25 | 1975-12-16 | Gen Electric | Substrate for immunological tests and method of fabrication thereof |
| US3933997A (en) * | 1974-03-01 | 1976-01-20 | Corning Glass Works | Solid phase radioimmunoassay of digoxin |
| US3975162A (en) * | 1974-03-13 | 1976-08-17 | Marine Colloids, Inc. | Applying reagent to medium and device therefor |
| US4108972A (en) * | 1974-03-15 | 1978-08-22 | Dreyer William J | Immunological reagent employing radioactive and other tracers |
| US3901657A (en) * | 1974-04-29 | 1975-08-26 | Sun Scient Inc | Device for testing solutions and body fluids |
| US4169138A (en) * | 1974-05-29 | 1979-09-25 | Pharmacia Diagnostics Ab | Method for the detection of antibodies |
| US3951332A (en) * | 1974-07-22 | 1976-04-20 | Torbeck Frank W | Container closure with tuck-under tab |
| US3915647A (en) * | 1974-08-16 | 1975-10-28 | Polaroid Corp | Device for determining the concentration of a substance in a fluid |
| US3933594A (en) * | 1974-08-16 | 1976-01-20 | Polaroid Corporation | Method and device for determining the concentration of a substance in a fluid |
| US3979509A (en) * | 1974-09-03 | 1976-09-07 | General Electric Company | Opaque layer method for detecting biological particles |
| US3996158A (en) * | 1974-09-23 | 1976-12-07 | Cohen Marvin D | Pumicite filter aid |
| US4017597A (en) * | 1974-10-30 | 1977-04-12 | Monsanto Company | Unitized solid phase immunoassay kit and method |
| US4123509A (en) * | 1974-12-19 | 1978-10-31 | American Home Products Corporation | Pregnancy test |
| US4018662A (en) * | 1975-01-03 | 1977-04-19 | Max-Planck-Gesellschaft Zur Forderung Der Wissenschaften E.V. | Method and apparatus for simultaneous quantitative analysis of several constituents in a sample |
| SE388694B (sv) * | 1975-01-27 | 1976-10-11 | Kabi Ab | Sett att pavisa ett antigen exv i prov av kroppvetskor, med utnyttjande av till porost berarmaterial bundna eller adsorberande antikroppar |
| US3960499A (en) * | 1975-02-18 | 1976-06-01 | Miles Laboratories, Inc. | Biological test apparatus |
| US3992631A (en) * | 1975-02-27 | 1976-11-16 | International Diagnostic Technology, Inc. | Fluorometric system, method and test article |
| US4166102A (en) * | 1975-04-07 | 1979-08-28 | Becton, Dickinson And Company | Immobilized immunoadsorbent |
| NO136062C (no) * | 1975-04-14 | 1977-07-13 | Henry Hirschberg | Fremgangsm}te og anordning for oppsamling av v{ske med innhold av radioaktive sporstoffer. |
| USRE30267E (en) * | 1975-06-20 | 1980-05-06 | Eastman Kodak Company | Multilayer analytical element |
| CA1054034A (en) * | 1975-06-20 | 1979-05-08 | Barbara J. Bruschi | Multilayer analytical element |
| US4042335A (en) * | 1975-07-23 | 1977-08-16 | Eastman Kodak Company | Integral element for analysis of liquids |
| US4016043A (en) * | 1975-09-04 | 1977-04-05 | Akzona Incorporated | Enzymatic immunological method for the determination of antigens and antibodies |
| US4474878A (en) | 1975-09-29 | 1984-10-02 | Cordis Laboratories, Inc. | Sandwich EIA for antigen associated with hepatitis |
| US4642285A (en) | 1975-09-29 | 1987-02-10 | Diamedix Corporation | Sandwich EIA for antigen |
| US3984533A (en) * | 1975-11-13 | 1976-10-05 | General Electric Company | Electrophoretic method of detecting antigen-antibody reaction |
| US4123224A (en) * | 1975-12-17 | 1978-10-31 | American Home Products Corporation | Diagnostic test device |
| US3990850A (en) * | 1976-01-06 | 1976-11-09 | Akzona Incorporated | Diagnostic test card |
| US4020151A (en) * | 1976-02-17 | 1977-04-26 | International Diagnostic Technology, Inc. | Method for quantitation of antigens or antibodies on a solid surface |
| US4053284A (en) * | 1976-03-10 | 1977-10-11 | Akzona Incorporated | Continuous flow apparatus for biological testing |
| US4128399A (en) * | 1976-03-15 | 1978-12-05 | Liotta Lance A | Device and method for detecting phenothiazine-type drugs in urine |
| US4038485A (en) * | 1976-03-18 | 1977-07-26 | Miles Laboratories, Inc. | Test composition, device, and method |
| US4059407A (en) * | 1976-04-14 | 1977-11-22 | Becton, Dickinson And Company | Disposable chemical indicators |
| US4087326A (en) * | 1976-05-03 | 1978-05-02 | Ethicon, Inc. | Microbiological scaled sterility test strips and method |
| US4087332A (en) * | 1976-05-07 | 1978-05-02 | Kai Aage Hansen | Indicator for use in selection of bactericidal and bacteristatic drugs and method for producing same |
| US4067959A (en) * | 1976-05-10 | 1978-01-10 | International Diagnostic Technology, Inc. | Indirect solid surface test for antigens or antibodies |
| IL49685A (en) * | 1976-05-31 | 1978-10-31 | Technion Res & Dev Foundation | Specific binding assay method for determining the concentration of materials and reagent means therefor |
| US4157323A (en) * | 1976-06-09 | 1979-06-05 | California Institute Of Technology | Metal containing polymeric functional microspheres |
| US4094647A (en) * | 1976-07-02 | 1978-06-13 | Thyroid Diagnostics, Inc. | Test device |
| GB1582956A (en) * | 1976-07-30 | 1981-01-21 | Ici Ltd | Composite magnetic particles |
| US4210418A (en) * | 1976-08-30 | 1980-07-01 | Mallinckrodt, Inc. | Container for immunochemical and enzymatical determinations or procedures |
| US4145186A (en) * | 1976-10-04 | 1979-03-20 | H. W. Andersen Products Inc. | Sterilization detection device and method |
| US4046514A (en) * | 1976-11-24 | 1977-09-06 | Miles Laboratories, Inc. | Test device and method for determining a component in a sample |
| US4134792A (en) * | 1976-12-06 | 1979-01-16 | Miles Laboratories, Inc. | Specific binding assay with an enzyme modulator as a labeling substance |
| US4130462A (en) * | 1976-12-16 | 1978-12-19 | Syva Company | Receptor steric hindrance immunoassay for receptor determination |
| US4200690A (en) * | 1976-12-16 | 1980-04-29 | Millipore Corporation | Immunoassay with membrane immobilized antibody |
| US4407943A (en) | 1976-12-16 | 1983-10-04 | Millipore Corporation | Immobilized antibody or antigen for immunoassay |
| CA1095819A (en) * | 1977-01-14 | 1981-02-17 | Eastman Kodak Company | Element for analysis of liquids |
| IL51354A (en) * | 1977-01-28 | 1979-07-25 | Ames Yissum Ltd | Assay method for the quantitative determination of a hapten in aqueous solution |
| US4116638A (en) * | 1977-03-03 | 1978-09-26 | Warner-Lambert Company | Immunoassay device |
| US4108976A (en) * | 1977-03-04 | 1978-08-22 | Becton, Dickinson And Company | Automated direct serum radioimmunoassay |
| IL51667A (en) * | 1977-03-16 | 1979-10-31 | Miles Yeda Ltd | Immunoassay for the determination of a hapten |
| US4145406A (en) * | 1977-04-11 | 1979-03-20 | Miles Laboratories, Inc. | Specific binding - adsorbent assay method and test means |
| US4108729A (en) * | 1977-05-16 | 1978-08-22 | U.S. Packaging Corp. | Paper booklet for presumptive diagnosis of Neisseria Gonorrhoeae in the male |
| US4110079A (en) * | 1977-06-09 | 1978-08-29 | Eastman Kodak Company | Analytical element for clinical analysis |
| US4129417A (en) * | 1977-10-28 | 1978-12-12 | Miles Laboratories, Inc. | Multisystem test means |
| US4219335A (en) * | 1978-09-18 | 1980-08-26 | E. I. Du Pont De Nemours And Company | Immunochemical testing using tagged reagents |
| US4298345A (en) | 1977-11-21 | 1981-11-03 | Damon Corporation | Method and apparatus for chemical spot test analysis |
| US4153668A (en) * | 1978-01-03 | 1979-05-08 | Eastman Kodak Company | Multi-zone analytical element and method using same |
| US4160008A (en) * | 1978-01-26 | 1979-07-03 | Miles Laboratories, Inc. | Multilayered test device for determining the presence of a liquid sample component, and method of use |
| AU527489B2 (en) | 1978-03-20 | 1983-03-10 | Abbott Laboratories | Sugar coated reagents for solid phase immunoassay |
| US4244694A (en) * | 1978-03-31 | 1981-01-13 | Union Carbide Corporation | Reactor/separator device for use in automated solid phase immunoassay |
| US4233402A (en) * | 1978-04-05 | 1980-11-11 | Syva Company | Reagents and method employing channeling |
| US4275149A (en) | 1978-11-24 | 1981-06-23 | Syva Company | Macromolecular environment control in specific receptor assays |
| US4631174A (en) | 1978-05-02 | 1986-12-23 | Fuji Photo Film Co., Ltd. | Multilayer chemical analysis member having an outer waterproof layer |
| JPS5510590A (en) | 1978-05-04 | 1980-01-25 | Wellcome Found | Enzyme immunity quantity analysis |
| DE2821469A1 (de) * | 1978-05-17 | 1979-11-22 | Boehringer Mannheim Gmbh | Diagnostisches mittel zur bestimmung von harnstoff |
| JPS587332Y2 (ja) | 1978-06-06 | 1983-02-08 | 富士写真フイルム株式会社 | 多層血液化学分析材料 |
| US4254082A (en) * | 1978-06-12 | 1981-03-03 | Miles Laboratories, Inc. | Specific binding-adsorbent assay test means |
| US4238565A (en) * | 1978-06-22 | 1980-12-09 | Miles Laboratories, Inc. | Specific binding assay with a prosthetic group as a label component |
| US4175923A (en) * | 1978-06-26 | 1979-11-27 | Friend William G | Method and apparatus for occult blood testing in the home |
| NL7807532A (nl) | 1978-07-13 | 1980-01-15 | Akzo Nv | Metaal-immunotest. |
| DE2932973A1 (de) | 1978-08-14 | 1980-02-28 | Fuji Photo Film Co Ltd | Integrales mehrschichtiges material fuer die chemische analyse des blutes |
| DE2836046A1 (de) | 1978-08-17 | 1980-02-28 | Behringwerke Ag | Immunologisches bestimmungsverfahren |
| US4228237A (en) * | 1978-09-21 | 1980-10-14 | Calbiochem-Behring Corp. | Methods for the detection and determination of ligands |
| US4254083A (en) | 1979-07-23 | 1981-03-03 | Eastman Kodak Company | Structural configuration for transport of a liquid drop through an ingress aperture |
| US4233029A (en) * | 1978-10-25 | 1980-11-11 | Eastman Kodak Company | Liquid transport device and method |
| US4189304A (en) * | 1978-10-27 | 1980-02-19 | Miles Laboratories, Inc. | Device and method for detecting myoglobin |
| US4237234A (en) * | 1978-10-30 | 1980-12-02 | Meunier Henry E | Device for use in the study of biochemical or enzymatic reactions produced by living organisms |
| IL55816A (en) | 1978-10-30 | 1982-04-30 | Ames Yissum Ltd | Method for simultaneous immunoassay of several different antibodies and a kit therefor |
| US4246339A (en) * | 1978-11-01 | 1981-01-20 | Millipore Corporation | Test device |
| US4374925A (en) | 1978-11-24 | 1983-02-22 | Syva Company | Macromolecular environment control in specific receptor assays |
| US4318707A (en) | 1978-11-24 | 1982-03-09 | Syva Company | Macromolecular fluorescent quencher particle in specific receptor assays |
| JPH0142041Y2 (zh) * | 1978-12-11 | 1989-12-11 | ||
| US4258001A (en) | 1978-12-27 | 1981-03-24 | Eastman Kodak Company | Element, structure and method for the analysis or transport of liquids |
| US4235601A (en) * | 1979-01-12 | 1980-11-25 | Thyroid Diagnostics, Inc. | Test device and method for its use |
| US4361537A (en) | 1979-01-12 | 1982-11-30 | Thyroid Diagnostics, Inc. | Test device and method for its use |
| US4288228A (en) | 1979-01-31 | 1981-09-08 | Technicon Instruments Corporation | Whole blood analyses and diffusion apparatus therefor |
| US4274832A (en) | 1979-02-12 | 1981-06-23 | Eastman Kodak Company | Analytical element and method for analysis of multiple analytes |
| GB2045431B (en) | 1979-02-26 | 1983-04-20 | Technicon Instr | Immunoassay utilising two particulate reagents |
| US4268270A (en) | 1979-04-30 | 1981-05-19 | Children's Hospital Medical Center | Glycosylated hemoglobin measurement |
| US4301139A (en) | 1979-06-21 | 1981-11-17 | Ames-Yissum Ltd. | Multilayer column chromatography specific binding assay method, test device and test kit |
| US4271119A (en) | 1979-07-23 | 1981-06-02 | Eastman Kodak Company | Capillary transport device having connected transport zones |
| US4281061A (en) | 1979-07-27 | 1981-07-28 | Syva Company | Double antibody for enhanced sensitivity in immunoassay |
| US4305924A (en) | 1979-08-08 | 1981-12-15 | Ventrex Laboratories, Inc. | Method and apparatus for performing in vitro clinical diagnostic tests using a solid phase assay system |
| US4305721A (en) | 1979-08-20 | 1981-12-15 | Becton Dickinson & Company | Agglutination assay |
| US4305720A (en) | 1979-08-20 | 1981-12-15 | Becton Dickinson & Company | Gentamicin assay and products therefor |
| US4270921A (en) | 1979-09-24 | 1981-06-02 | Graas Joseph E | Microchromatographic device and method for rapid determination of a desired substance |
| JPS5647761A (en) | 1979-09-27 | 1981-04-30 | Fuji Photo Film Co Ltd | Laminated analyzing piece and immunity analyzing method using the same |
| US4280816A (en) | 1979-10-25 | 1981-07-28 | Nasik Elahi | Macroencapsulated immunosorbent assay technique and element therefor |
| US4338094A (en) | 1979-10-25 | 1982-07-06 | Nasik Elahi | Macroencapsulated immunosorbent assay technique |
| US4540659A (en) | 1981-04-17 | 1985-09-10 | Syva Company | Simultaneous calibration heterogeneous immunoassay |
| US4299916A (en) | 1979-12-26 | 1981-11-10 | Syva Company | Preferential signal production on a surface in immunoassays |
| US4849338A (en) | 1982-07-16 | 1989-07-18 | Syntex (U.S.A.) Inc. | Simultaneous calibration heterogeneous immunoassay |
| US4533629A (en) | 1981-04-17 | 1985-08-06 | Syva Company | Simultaneous calibration heterogeneous immunoassay |
| US4391904A (en) | 1979-12-26 | 1983-07-05 | Syva Company | Test strip kits in immunoassays and compositions therein |
| US4843000A (en) | 1979-12-26 | 1989-06-27 | Syntex (U.S.A.) Inc. | Simultaneous calibration heterogeneous immunoassay |
| NL8000173A (nl) | 1980-01-11 | 1981-08-03 | Akzo Nv | Toepassing van in water dispergeerbare, hydrofobe kleurstoffen als label in immunochemische testen. |
| FI61965C (fi) | 1980-01-17 | 1982-10-11 | Suovaniemi Finnpipette | Foerfarande foer detektering av hemoglobin i avfoering |
| US4323536A (en) | 1980-02-06 | 1982-04-06 | Eastman Kodak Company | Multi-analyte test device |
| US4452901A (en) | 1980-03-20 | 1984-06-05 | Ciba-Geigy Corporation | Electrophoretically transferring electropherograms to nitrocellulose sheets for immuno-assays |
| US4347312A (en) | 1980-03-20 | 1982-08-31 | Research Triangle Institute | Detection of antibiotics in milk |
| EP0111762B1 (en) | 1980-06-20 | 1987-11-19 | Unilever Plc | Processes and apparatus for carrying out specific binding assays |
| US5009997A (en) | 1980-06-30 | 1991-04-23 | Shah Vipin D | Two site cross-reaction immunometric sandwich assay method |
| US5009996A (en) | 1980-06-30 | 1991-04-23 | International Immunoassay Laboratories, Inc. | Two site cross-reaction immunometric sandwich assay method |
| US4333733A (en) | 1980-07-17 | 1982-06-08 | Eastman Kodak Company | Continuous release of reagent in an analytical element to reduce assay interference |
| US4376110A (en) | 1980-08-04 | 1983-03-08 | Hybritech, Incorporated | Immunometric assays using monoclonal antibodies |
| US4486530A (en) | 1980-08-04 | 1984-12-04 | Hybritech Incorporated | Immunometric assays using monoclonal antibodies |
| US4816224A (en) | 1980-08-05 | 1989-03-28 | Boehringer Mannheim Gmbh | Device for separating plasma or serum from whole blood and analyzing the same |
| DE3029579C2 (de) | 1980-08-05 | 1985-12-12 | Boehringer Mannheim Gmbh, 6800 Mannheim | Verfahren und Mittel zur Abtrennung von Plasma oder Serum aus Vollblut |
| US4366241A (en) | 1980-08-07 | 1982-12-28 | Syva Company | Concentrating zone method in heterogeneous immunoassays |
| US4357311A (en) | 1980-10-03 | 1982-11-02 | Warner-Lambert Company | Substrate for immunoassay and means of preparing same |
| JPS5767860A (en) | 1980-10-15 | 1982-04-24 | Fuji Photo Film Co Ltd | Material for multilayer analysis |
| US4668619A (en) | 1980-10-30 | 1987-05-26 | Miles Laboratories, Inc. | Multilayer homogeneous specific binding assay device |
| EP0064063B1 (en) | 1980-11-07 | 1985-09-11 | Celltech Limited | Assay for interferon |
| JPS5782766A (en) | 1980-11-11 | 1982-05-24 | Konishiroku Photo Ind Co Ltd | Amynological measuring element |
| US4517288A (en) | 1981-01-23 | 1985-05-14 | American Hospital Supply Corp. | Solid phase system for ligand assay |
| US4752562A (en) | 1981-01-23 | 1988-06-21 | Baxter Travenol Laboratories, Inc. | Detection of serum antibody and surface antigen by radial partition immunoassay |
| US4774174A (en) | 1981-01-23 | 1988-09-27 | Baxter Travenol Laboratories, Inc. | Solid phase system for ligand assay |
| US4426451A (en) | 1981-01-28 | 1984-01-17 | Eastman Kodak Company | Multi-zoned reaction vessel having pressure-actuatable control means between zones |
| US4425438A (en) | 1981-03-13 | 1984-01-10 | Bauman David S | Assay method and device |
| US4442204A (en) | 1981-04-10 | 1984-04-10 | Miles Laboratories, Inc. | Homogeneous specific binding assay device and preformed complex method |
| US4711955A (en) | 1981-04-17 | 1987-12-08 | Yale University | Modified nucleotides and methods of preparing and using same |
| US4447526A (en) | 1981-04-20 | 1984-05-08 | Miles Laboratories, Inc. | Homogeneous specific binding assay with carrier matrix incorporating specific binding partner |
| US4362697A (en) | 1981-04-20 | 1982-12-07 | Miles Laboratories, Inc. | Homogeneous specific binding assay test device having copolymer enhancing substance |
| EP0063810B1 (en) | 1981-04-29 | 1986-03-05 | Ciba-Geigy Ag | New devices and kits for immunological analysis |
| US4365970A (en) | 1981-05-01 | 1982-12-28 | Smithkline Instruments, Inc. | Specimen test slide and method for testing occult blood |
| US4604365A (en) | 1981-06-02 | 1986-08-05 | Electro-Nucleonics, Inc. | Immunoprecipitation assay |
| US4390343A (en) | 1981-07-06 | 1983-06-28 | Miles Laboratories, Inc. | Multilayer analytical element having an impermeable radiation diffusing and blocking layer |
| US4447529A (en) | 1981-07-06 | 1984-05-08 | Miles Laboratories, Inc. | Preparing homogeneous specific binding assay element to avoid premature reaction |
| US4440301A (en) | 1981-07-16 | 1984-04-03 | American Hospital Supply Corporation | Self-stacking reagent slide |
| ATE15229T1 (de) | 1981-07-16 | 1985-09-15 | Hoffmann La Roche | Verfahren zum nachweisen von okkultem humanblut in humanstuhlproben. |
| JPS5818167A (ja) | 1981-07-24 | 1983-02-02 | Fuji Photo Film Co Ltd | 分析フイルム及びこれを用いる分析方法 |
| US4363874A (en) | 1981-08-07 | 1982-12-14 | Miles Laboratories, Inc. | Multilayer analytical element having an impermeable radiation nondiffusing reflecting layer |
| US4608336A (en) | 1981-08-27 | 1986-08-26 | Miles Laboratories, Inc. | #3B theophylline immunoassay employing 9-theophylline reagents |
| DE3134611A1 (de) | 1981-09-01 | 1983-03-10 | Boehringer Mannheim Gmbh, 6800 Mannheim | Verfahren zur durchfuehrung analytischer bestimmungen und hierfuer geeignetes mittel |
| US4461829A (en) | 1981-09-14 | 1984-07-24 | Miles Laboratories, Inc. | Homogeneous specific binding assay element and lyophilization production method |
| US4629690A (en) | 1981-09-18 | 1986-12-16 | Syntex (U.S.A.) Inc. | Homogeneous enzyme specific binding assay on non-porous surface |
| US4446232A (en) | 1981-10-13 | 1984-05-01 | Liotta Lance A | Enzyme immunoassay with two-zoned device having bound antigens |
| US4639419A (en) | 1981-10-22 | 1987-01-27 | Meloy Laboratories, Inc. | Immunological color change test involving two differently colored reagent spots |
| US4446234A (en) | 1981-10-23 | 1984-05-01 | The United States Of America As Represented By The Department Of Health And Human Services | Vitro cellular interaction with amnion membrane substrate |
| US4464552A (en) | 1981-10-29 | 1984-08-07 | James River-Dixie/Northern, Inc. | Packaging |
| US4562148A (en) | 1981-11-06 | 1985-12-31 | Miles Laboratories, Inc. | Analytical element and method for preventing reagent migration |
| US4938927A (en) | 1982-01-08 | 1990-07-03 | Environmental Diagnostics, Inc. | Rotary fluid manipulator |
| US5141875A (en) | 1982-01-08 | 1992-08-25 | Environmental Diagnostics, Inc. | Rotary fluid manipulator |
| US4444193A (en) | 1982-01-11 | 1984-04-24 | Medtronic, Inc. | Fluid absorbent quantitative test device |
| US5073484A (en) | 1982-03-09 | 1991-12-17 | Bio-Metric Systems, Inc. | Quantitative analysis apparatus and method |
| US4506009A (en) | 1982-03-30 | 1985-03-19 | University Of California | Heterogeneous immunoassay method |
| US4450231A (en) | 1982-03-31 | 1984-05-22 | Biostar Medical Products, Inc. | Immunoassay for determination of immune complexes with polymer-coated plastic base |
| US4504585A (en) | 1982-04-05 | 1985-03-12 | Aalto Scientific, Ltd. | Affinity immunoassay system |
| US4663278A (en) | 1982-04-30 | 1987-05-05 | Syva Company | Agglutination dependent enzyme channeling immunoassay |
| US4435504A (en) | 1982-07-15 | 1984-03-06 | Syva Company | Immunochromatographic assay with support having bound "MIP" and second enzyme |
| JPS5934154A (ja) | 1982-08-19 | 1984-02-24 | Konishiroku Photo Ind Co Ltd | 免疫分析素子測定法 |
| US4447546A (en) | 1982-08-23 | 1984-05-08 | Myron J. Block | Fluorescent immunoassay employing optical fiber in capillary tube |
| DE3332144A1 (de) | 1982-09-06 | 1984-03-08 | Konishiroku Photo Industry Co., Ltd., Tokyo | Analytisches element |
| US4722906A (en) | 1982-09-29 | 1988-02-02 | Bio-Metric Systems, Inc. | Binding reagents and methods |
| US4459358A (en) | 1982-12-29 | 1984-07-10 | Polaroid Corporation | Multilayer element for analysis |
| AU529210B3 (en) | 1983-02-02 | 1983-04-14 | Australian Monoclonal Development Pty. Ltd. | Monoclonal antibody in occult blood diagnosis |
| US4687735A (en) | 1983-03-14 | 1987-08-18 | Syntex (U.S.A.) Inc. | Enzymatic poly-reactant channeling binding assay |
| AU2706384A (en) | 1983-05-06 | 1984-11-08 | Monoclonal Antibodies Inc. | Colorimetric immunoassay on solid surface |
| US4687732A (en) | 1983-06-10 | 1987-08-18 | Yale University | Visualization polymers and their application to diagnostic medicine |
| US4550075A (en) | 1983-06-22 | 1985-10-29 | Kallestad Laboratories, Inc. | Method for ligand determination utilizing an immunoassay monitorable by biotin-containing enzymes, and compositions therefor |
| US4552839A (en) | 1983-08-01 | 1985-11-12 | Syntex (U.S.A.) Inc. | Determination of analytes in particle-containing medium |
| DE3335839A1 (de) | 1983-10-03 | 1985-04-18 | Kernforschungsanlage Jülich GmbH, 5170 Jülich | Verfahren zur absenkung der reaktivitaet und zum abschalten eines gasgekuehlten, graphitmoderierten kernreaktors und graphitelement mit abschaltsubstanz |
| US4594327A (en) | 1983-11-02 | 1986-06-10 | Syntex (U.S.A.) Inc. | Assay method for whole blood samples |
| GB8331514D0 (en) | 1983-11-25 | 1984-01-04 | Janssen Pharmaceutica Nv | Visualization method |
| AU579123B2 (en) | 1983-12-02 | 1988-11-17 | Vertrik Bioteknik A.B. | Multisegment test strip that folds |
| EP0149168B1 (en) | 1983-12-19 | 1991-04-24 | Daiichi Pure Chemicals Co. Ltd. | Immunoassay |
| US4703017C1 (en) | 1984-02-14 | 2001-12-04 | Becton Dickinson Co | Solid phase assay with visual readout |
| GB8406752D0 (en) | 1984-03-15 | 1984-04-18 | Unilever Plc | Chemical and clinical tests |
| US4743560A (en) | 1984-03-26 | 1988-05-10 | Becton Dickinson And Company | Solid phase assay |
| US4632901A (en) | 1984-05-11 | 1986-12-30 | Hybritech Incorporated | Method and apparatus for immunoassays |
| EP0170746A1 (en) | 1984-08-07 | 1986-02-12 | Covalent Technology Corporation | Biologically active material test |
| US4826759A (en) | 1984-10-04 | 1989-05-02 | Bio-Metric Systems, Inc. | Field assay for ligands |
| US4999285A (en) | 1984-11-15 | 1991-03-12 | Syntex (U.S.A.) Inc. | Chromatographic cassette |
| US4760142A (en) | 1984-11-27 | 1988-07-26 | Hoechst Celanese Corporation | Divalent hapten derivatives |
| DE3445816C1 (de) | 1984-12-15 | 1986-06-12 | Behringwerke Ag, 3550 Marburg | Flaechenfoermiges diagnostisches Mittel |
| US4782016A (en) | 1985-01-18 | 1988-11-01 | Eastman Kodak Company | Analytical element and method for determination of theophylline by enzyme inhibition |
| US4740468A (en) | 1985-02-14 | 1988-04-26 | Syntex (U.S.A.) Inc. | Concentrating immunochemical test device and method |
| US4678757A (en) | 1985-04-11 | 1987-07-07 | Smithkline Diagnostics, Inc. | Device and method for whole blood separation and analysis |
| JPS61247965A (ja) | 1985-04-25 | 1986-11-05 | Susumu Kogyo Kk | 酵素免疫測定法 |
| US4803170A (en) | 1985-05-09 | 1989-02-07 | Ultra Diagnostics Corporation | Competitive immunoassay method, device and test kit |
| US4837395A (en) | 1985-05-10 | 1989-06-06 | Syntex (U.S.A.) Inc. | Single step heterogeneous assay |
| US4693834A (en) | 1986-05-05 | 1987-09-15 | Murex Corporation | Transverse flow diagnostic kit |
| US4623461A (en) | 1985-05-31 | 1986-11-18 | Murex Corporation | Transverse flow diagnostic device |
| US4757024A (en) | 1985-05-31 | 1988-07-12 | Biostar Medical Products, Inc. | Immune complex detection method and article using immunologically non-specific immunoglobulins |
| JPH076984B2 (ja) | 1985-05-31 | 1995-01-30 | 株式会社日立製作所 | 複数項目分析方法 |
| US4753893A (en) | 1985-05-31 | 1988-06-28 | Biostar Medical Products, Inc. | Method and article for detection of immune complexes |
| US4931385A (en) | 1985-06-24 | 1990-06-05 | Hygeia Sciences, Incorporated | Enzyme immunoassays and immunologic reagents |
| DE3523439A1 (de) | 1985-06-29 | 1987-01-08 | Boehringer Mannheim Gmbh | Testtraeger |
| US4806312A (en) | 1985-08-28 | 1989-02-21 | Miles Inc. | Multizone analytical element having detectable signal concentrating zone |
| US4806311A (en) | 1985-08-28 | 1989-02-21 | Miles Inc. | Multizone analytical element having labeled reagent concentration zone |
| DE3530993A1 (de) | 1985-08-30 | 1987-03-05 | Miles Lab | Teststreifen mit festlegbarer probenaufnahmekapazitaet |
| US4900663A (en) | 1985-09-13 | 1990-02-13 | Environmental Diagnostics, Inc. | Test kit for determining the presence of organic materials and method of utilizing same |
| US4761381A (en) | 1985-09-18 | 1988-08-02 | Miles Inc. | Volume metering capillary gap device for applying a liquid sample onto a reactive surface |
| TW203120B (zh) | 1985-10-04 | 1993-04-01 | Abbott Lab | |
| US4868106A (en) | 1985-10-17 | 1989-09-19 | Konishiroku Photo Industry Co., Ltd. | Analytical element and method for determining a component in a test sample |
| GB8526741D0 (en) | 1985-10-30 | 1985-12-04 | Boots Celltech Diagnostics | Binding assay device |
| US5236826A (en) | 1985-12-10 | 1993-08-17 | Murex Corporation | Immunoassay for the detection or quantitation of an analyte |
| US4868108A (en) | 1985-12-12 | 1989-09-19 | Hygeia Sciences, Incorporated | Multiple-antibody detection of antigen |
| CA1291031C (en) | 1985-12-23 | 1991-10-22 | Nikolaas C.J. De Jaeger | Method for the detection of specific binding agents and their correspondingbindable substances |
| US4916056A (en) | 1986-02-18 | 1990-04-10 | Abbott Laboratories | Solid-phase analytical device and method for using same |
| JPH0750114B2 (ja) | 1986-03-17 | 1995-05-31 | 富士写真フイルム株式会社 | 免疫分析器具を用いる分析方法 |
| US4960692A (en) | 1986-03-18 | 1990-10-02 | Fisher Scientific Company | Assay employing binding pair members on particles and on a filter or membrane |
| GB8608157D0 (en) | 1986-04-03 | 1986-05-08 | Unilever Plc | Ovulation test chart |
| DE3616105A1 (de) | 1986-05-13 | 1987-11-19 | Merck Patent Gmbh | Teststreifen |
| US4786594A (en) | 1986-05-14 | 1988-11-22 | Syntex (U.S.A.) Inc. | Enzyme immunoassay |
| US4851210A (en) | 1986-05-22 | 1989-07-25 | Genelabs Incorporated | Blood typing device |
| US4837145A (en) | 1986-06-09 | 1989-06-06 | Liotta Lance A | Layered immunoassay using antibodies bound to transport particles to determine the presence of an antigen |
| AU602694B2 (en) | 1986-06-09 | 1990-10-25 | Ortho Diagnostic Systems Inc. | Improved colloidal gold membrane assay |
| US4959305A (en) | 1986-06-18 | 1990-09-25 | Miles Inc. | Reversible immobilization of assay reagents in a multizone test device |
| US4812293A (en) | 1986-06-30 | 1989-03-14 | Becton, Dickinson And Company | Vacuum actuated assay device and method of using same |
| US4790979A (en) | 1986-08-29 | 1988-12-13 | Technimed Corporation | Test strip and fixture |
| US4959307A (en) | 1986-09-05 | 1990-09-25 | Syntex (U.S.A.) Inc. | Immunoseparating strip |
| US5260194A (en) | 1986-09-05 | 1993-11-09 | Syntex (U.S.A.) Inc. | Immunoseparating strip |
| US4963468A (en) | 1986-09-05 | 1990-10-16 | Syntex (U.S.A.) Inc. | Immunoseparating strip |
| US5260193A (en) | 1986-09-05 | 1993-11-09 | Syntex (U.S.A.) Inc. | Immunoseparating strip |
| US5085988A (en) | 1986-09-05 | 1992-02-04 | Syntex (U.S.A.) Inc. | Immunoseparating strip |
| US5085987A (en) | 1986-09-05 | 1992-02-04 | Syntex (U.S.A.) Inc. | Immunoseparating strip |
| DE3630999A1 (de) | 1986-09-12 | 1988-03-17 | Boehringer Mannheim Gmbh | Mehrschichtiger testtraeger |
| EP0260965B2 (en) | 1986-09-18 | 2002-01-16 | Pacific Biotech Inc. | Immunodiagnostic device |
| US4960691A (en) | 1986-09-29 | 1990-10-02 | Abbott Laboratories | Chromatographic test strip for determining ligands or receptors |
| US4880751A (en) | 1986-10-31 | 1989-11-14 | Board Of Regents, The University Of Texas System | Immunoglobulin adsorption |
| GB8626081D0 (en) | 1986-10-31 | 1986-12-03 | Unilever Plc | Printing processes |
| US5232835A (en) | 1986-11-07 | 1993-08-03 | Syntex (U.S.A.) Inc. | Qualitative immunochromatographic method and device |
| US5156952A (en) | 1986-11-07 | 1992-10-20 | Syntex (U.S.A.) Inc. | Qualitative immunochromatographic method and device |
| EP0271204A3 (en) | 1986-11-07 | 1989-10-25 | Syntex (U.S.A.) Inc. | Immunochromatographic method and device |
| US5030558A (en) | 1986-11-07 | 1991-07-09 | Syntex (U.S.A.) Inc. | Qualitative immunochromatographic method and device |
| US4789629A (en) | 1986-11-24 | 1988-12-06 | Smithkline Beckman Corporation | Method and device for collecting and testing for fecal occult blood |
| DE3787078T2 (de) | 1986-11-24 | 1993-12-09 | Abbott Lab | Proberichtwirkung für analytisches Festphasengerät. |
| US4770853A (en) | 1986-12-03 | 1988-09-13 | New Horizons Diagnostics Corporation | Device for self contained solid phase immunodiffusion assay |
| US4976926A (en) | 1986-12-15 | 1990-12-11 | Pall Corporation | Vacuum diagnostic device |
| US4789526A (en) | 1986-12-15 | 1988-12-06 | Pall Corporation | Vacuum diagnostic device |
| DE3643516A1 (de) | 1986-12-19 | 1988-06-30 | Boehringer Mannheim Gmbh | Testtraeger fuer die analytische bestimmung von bestandteilen von koerperfluessigkeiten |
| US4859603A (en) | 1987-01-05 | 1989-08-22 | Dole Associates, Inc. | Personal diagnostic kit |
| GB8701432D0 (en) | 1987-01-22 | 1987-02-25 | Unilever Plc | Assays |
| US5079142A (en) | 1987-01-23 | 1992-01-07 | Synbiotics Corporation | Orthogonal flow immunoassays and devices |
| US4797260A (en) | 1987-01-27 | 1989-01-10 | V-Tech, Inc. | Antibody testing system |
| AU592174B2 (en) | 1987-02-17 | 1990-01-04 | Genesis Labs, Inc. | Immunoassay test strip |
| US4920046A (en) | 1987-02-20 | 1990-04-24 | Becton, Dickinson And Company | Process, test device, and test kit for a rapid assay having a visible readout |
| US4847199A (en) | 1987-02-27 | 1989-07-11 | Eastman Kodak Company | Agglutination immunoassay and kit for determination of a multivalent immune species using a buffered salt wash solution |
| US4918025A (en) | 1987-03-03 | 1990-04-17 | Pb Diagnostic Systems, Inc. | Self contained immunoassay element |
| CA1303983C (en) | 1987-03-27 | 1992-06-23 | Robert W. Rosenstein | Solid phase assay |
| JPH0684970B2 (ja) | 1987-03-31 | 1994-10-26 | 株式会社京都医科学研究所 | 糞便中の潜血検出方法 |
| US4803048A (en) | 1987-04-02 | 1989-02-07 | Nason Frederic L | Laboratory kit |
| US4849340A (en) | 1987-04-03 | 1989-07-18 | Cardiovascular Diagnostics, Inc. | Reaction system element and method for performing prothrombin time assay |
| IT1206777B (it) | 1987-04-06 | 1989-05-03 | Chemetron Del Dr Del Campo Gio | Procedimento di analisi immunologica o chimica per la determinazione di proteine in fluidi biologici e relativo completo (kit) di mezzi analitici. |
| US4857453A (en) | 1987-04-07 | 1989-08-15 | Syntex (U.S.A.) Inc. | Immunoassay device |
| US4788136A (en) | 1987-04-07 | 1988-11-29 | Abbott Laboratories | Diagnostic immunoassay by solid phase separation for digoxin |
| US5137808A (en) | 1987-04-07 | 1992-08-11 | Syntex (U.S.A.) Inc. | Immunoassay device |
| US4956275A (en) | 1987-04-14 | 1990-09-11 | Molecular Devices Corporation | Migratory detection immunoassay |
| DE3887771C5 (de) | 1987-04-27 | 2009-06-04 | Inverness Medical Switzerland Gmbh | Immunoassays und Vorrichtungen dafür. |
| DE3715485A1 (de) | 1987-05-09 | 1988-11-17 | Boehringer Mannheim Gmbh | Stabilisierung von ss-galactosidase |
| US4855240A (en) | 1987-05-13 | 1989-08-08 | Becton Dickinson And Company | Solid phase assay employing capillary flow |
| US4814142A (en) | 1987-05-22 | 1989-03-21 | Polymer Technology International Corp. | Test strip having a non-particulate dialyzed polymer layer |
| US4943522A (en) | 1987-06-01 | 1990-07-24 | Quidel | Lateral flow, non-bibulous membrane assay protocols |
| CA1313616C (en) | 1987-06-01 | 1993-02-16 | Robert B. Sargeant | Lateral flow, non-bibulous membrane protocols |
| JPS63305251A (ja) | 1987-06-05 | 1988-12-13 | Dai Ichi Pure Chem Co Ltd | ラテツクス凝集反応を利用する免疫学的測定方法 |
| IL85899A0 (en) | 1987-06-10 | 1988-09-30 | Miles Inc | Method,test device and test kit for separating labeled reagent in an immunometric binding assay |
| US4810470A (en) | 1987-06-19 | 1989-03-07 | Miles Inc. | Volume independent diagnostic device |
| US5215886A (en) | 1987-06-22 | 1993-06-01 | Patel P Jivan | HDL determination in whole blood |
| US4999287A (en) | 1988-05-19 | 1991-03-12 | Chemtrak Corporation | Direct measuring assay strip and method of use thereof |
| US5120643A (en) | 1987-07-13 | 1992-06-09 | Abbott Laboratories | Process for immunochromatography with colloidal particles |
| US4874692A (en) | 1987-07-20 | 1989-10-17 | Eastman Kodak Company | Binder composition and analytical element having stabilized peroxidase in layer containing the composition |
| US4883764A (en) | 1987-07-20 | 1989-11-28 | Kloepfer Mary A | Blood test strip |
| US4981786A (en) | 1987-09-04 | 1991-01-01 | Syntex (U.S.A.) Inc. | Multiple port assay device |
| US4956302A (en) | 1987-09-11 | 1990-09-11 | Abbott Laboratories | Lateral flow chromatographic binding assay device |
| EP0306772B1 (en) | 1987-09-11 | 1993-03-10 | Abbott Laboratories | Lateral flow chromatographic binding assay device |
| US4923680A (en) | 1987-09-18 | 1990-05-08 | Eastman Kodak Company | Test device containing an immunoassay filter with a flow-delaying polymer |
| US4912034A (en) | 1987-09-21 | 1990-03-27 | Biogenex Laboratories | Immunoassay test device and method |
| US4853335A (en) | 1987-09-28 | 1989-08-01 | Olsen Duane A | Colloidal gold particle concentration immunoassay |
| DE3733084A1 (de) | 1987-09-30 | 1989-04-13 | Boehringer Mannheim Gmbh | Testtraeger zur analytischen bestimmung eines bestandteils einer koerperfluessigkeit |
| US5006464A (en) | 1987-10-01 | 1991-04-09 | E-Y Laboratories, Inc. | Directed flow diagnostic device and method |
| US4902629A (en) | 1987-10-06 | 1990-02-20 | Personal Diagnostics, Inc. | Apparatus and processes for facilitating reaction between analyte and test reagent system |
| US4859612A (en) | 1987-10-07 | 1989-08-22 | Hygeia Sciences, Inc. | Metal sol capture immunoassay procedure, kit for use therewith and captured metal containing composite |
| US4891321A (en) | 1987-10-21 | 1990-01-02 | Hubscher Thomas T | Apparatus for performing determinations of immune reactants in biological fluids |
| US5275785A (en) | 1987-10-30 | 1994-01-04 | Unilever Patent Holdings B.V. | Test device for detecting an analyte in a liquid sample |
| US5256372A (en) | 1987-11-06 | 1993-10-26 | Idexx Corporation | Dipstick test device including a removable filter assembly |
| DE3878167T2 (de) | 1987-11-16 | 1993-05-27 | Janssen Pharmaceutica Nv | Auf ultrakleine kolloidale metallteilchen gegruendetes, allgemein anwendbares nachweissystem. |
| US4818677A (en) | 1987-12-03 | 1989-04-04 | Monoclonal Antibodies, Inc. | Membrane assay using focused sample application |
| US5006474A (en) | 1987-12-16 | 1991-04-09 | Disease Detection International Inc. | Bi-directional lateral chromatographic test device |
| US4988627A (en) | 1987-12-18 | 1991-01-29 | Eastman Kodak Company | Test device with dried reagent drops on inclined wall |
| EP0323605B1 (en) | 1987-12-21 | 1994-01-26 | Abbott Laboratories | Chromatographic binding assay devices and methods |
| US4977078A (en) | 1987-12-22 | 1990-12-11 | Olympus Optical Co., Ltd. | Plate substrate immunoassay device and method for performing a multi-test immunoassay on a specimen |
| US5209904A (en) | 1987-12-23 | 1993-05-11 | Abbott Laboratories | Agglutination reaction device utilizing selectively impregnated porous material |
| US5114673A (en) | 1988-01-21 | 1992-05-19 | Boehringer Mannheim Corporaton | Apparatus for determination of a component in a sample |
| US5206177A (en) | 1988-01-21 | 1993-04-27 | Boehringer Mannheim Corporation | Apparatus for determining an analyte and method therefor |
| US4952517A (en) | 1988-02-08 | 1990-08-28 | Hygeia Sciences, Inc. | Positive step immunoassay |
| US5104793A (en) | 1988-02-16 | 1992-04-14 | Boehringer Mannheim Corporation | Method for determining an analyte in a liquid sample using a zoned test device and an inhibitor for a label used in said method |
| NL8800796A (nl) | 1988-03-29 | 1989-10-16 | X Flow Bv | Werkwijze voor de chemische analyse van bestanddelen van een lichaamsvloeistof, alsmede een testinrichting en testpakket voor een dergelijke analyse. |
| US5202267A (en) | 1988-04-04 | 1993-04-13 | Hygeia Sciences, Inc. | Sol capture immunoassay kit and procedure |
| US5162237A (en) | 1988-04-11 | 1992-11-10 | Miles Inc. | Reaction cassette for preforming sequential analytical assays by noncentrifugal and noncapillary manipulations |
| DE3814370A1 (de) | 1988-04-28 | 1989-11-09 | Boehringer Mannheim Gmbh | Testtraeger fuer die analyse einer probenfluessigkeit, verfahren zur durchfuehrung einer solchen analyse und herstellungsverfahren |
| US5145784A (en) | 1988-05-04 | 1992-09-08 | Cambridge Biotech Corporation | Double capture assay method employing a capillary flow device |
| US4963325A (en) | 1988-05-06 | 1990-10-16 | Hygeia Sciences, Inc. | Swab expressor immunoassay device |
| US5137804A (en) | 1988-05-10 | 1992-08-11 | E. I. Du Pont De Nemours And Company | Assay device and immunoassay |
| US5164294A (en) | 1988-05-17 | 1992-11-17 | Syntex (U.S.A.) Inc. | Method for immunochromatographic analysis |
| US5039607A (en) | 1988-05-17 | 1991-08-13 | Syntex (U.S.A.) Inc. | Method for immunochromatographic analysis |
| US5094962A (en) | 1988-06-13 | 1992-03-10 | Eastman Kodak Company | Microporous article having a stabilized specific binding reagent, a method for its use and a diagnostic test kit |
| US5051237A (en) | 1988-06-23 | 1991-09-24 | P B Diagnostic Systems, Inc. | Liquid transport system |
| US5096809A (en) | 1988-07-25 | 1992-03-17 | Pacific Biotech, Inc. | Whole blood assays using porous membrane support devices |
| US4877586A (en) | 1988-07-27 | 1989-10-31 | Eastman Kodak Company | Sliding test device for assays |
| DE3826057A1 (de) | 1988-07-30 | 1990-02-01 | Boehringer Mannheim Gmbh | Testtraeger zur analytischen bestimmung eines bestandteils einer fluessigen probe |
| US4959197A (en) | 1988-09-07 | 1990-09-25 | Bio-Rad Laboratories, Inc. | Filter canister for immunoassays |
| US5030555A (en) | 1988-09-12 | 1991-07-09 | University Of Florida | Membrane-strip reagent serodiagnostic apparatus and method |
| US5182191A (en) | 1988-10-14 | 1993-01-26 | Pacific Biotech, Inc. | Occult blood sampling device and assay |
| US5079172A (en) | 1988-11-04 | 1992-01-07 | Board Of Trustees Operating Michigan State University | Method for detecting the presence of antibodies using gold-labeled antibodies and test kit |
| US5079174A (en) | 1988-12-08 | 1992-01-07 | Boehringer Mannheim Corporation | Apparatus for sequential determination of an analyte in a fluid sample |
| US5106758A (en) | 1988-12-12 | 1992-04-21 | Technicon Instruments Corporation | Analytical test device and the use thereof |
| DE3842702A1 (de) | 1988-12-19 | 1990-06-21 | Boehringer Mannheim Gmbh | Testtraeger zur analytischen untersuchung einer probenfluessigkeit mit hilfe einer spezifischen bindungsreaktion zweier bioaffiner bindungspartner und entsprechendes testverfahren |
| US5202268A (en) | 1988-12-30 | 1993-04-13 | Environmental Diagnostics, Inc. | Multi-layered test card for the determination of substances in liquids |
| US5028535A (en) | 1989-01-10 | 1991-07-02 | Biosite Diagnostics, Inc. | Threshold ligand-receptor assay |
| GB8903627D0 (en) | 1989-02-17 | 1989-04-05 | Unilever Plc | Assays |
| US4960565A (en) | 1989-03-14 | 1990-10-02 | Ecostix Environmental Inc. | Acid monitoring kit |
| US5132086A (en) | 1990-02-06 | 1992-07-21 | Chemtrak Corporation | Non-instrumented cholesterol assay |
| US5264180A (en) | 1989-03-16 | 1993-11-23 | Chemtrak, Inc. | Mobile reagents in an analyte assay in a self-contained apparatus |
| US4933092A (en) | 1989-04-07 | 1990-06-12 | Abbott Laboratories | Methods and devices for the separation of plasma or serum from whole blood |
| US5064541A (en) | 1989-04-07 | 1991-11-12 | Abbott Laboratories | Devices and methods for the collection of a predetermined volume of plasma or serum |
| US5135872A (en) | 1989-04-28 | 1992-08-04 | Sangstat Medical Corporation | Matrix controlled method of delayed fluid delivery for assays |
| US5100619A (en) | 1989-05-09 | 1992-03-31 | Beckman Instruments, Inc. | Device and method for collecting fecal occult blood specimens |
| US5120662A (en) | 1989-05-09 | 1992-06-09 | Abbott Laboratories | Multilayer solid phase immunoassay support and method of use |
| US5100620A (en) | 1989-05-15 | 1992-03-31 | Miles, Inc. | Capillary tube/gap reagent format |
| US5087556A (en) | 1989-05-17 | 1992-02-11 | Actimed Laboratories, Inc. | Method for quantitative analysis of body fluid constituents |
| US5234813A (en) | 1989-05-17 | 1993-08-10 | Actimed Laboratories, Inc. | Method and device for metering of fluid samples and detection of analytes therein |
| DE3922960A1 (de) | 1989-07-12 | 1991-01-17 | Boehringer Mannheim Gmbh | Verfahren zur bestimmung eines analyten |
| US5135716A (en) | 1989-07-12 | 1992-08-04 | Kingston Diagnostics, L.P. | Direct measurement of HDL cholesterol via dry chemistry strips |
| AU640162B2 (en) | 1989-08-28 | 1993-08-19 | Lifescan, Inc. | Blood separation and analyte detection techniques |
| US5185127A (en) | 1989-09-21 | 1993-02-09 | Becton, Dickinson And Company | Test device including flow control means |
| US5024323A (en) | 1989-09-25 | 1991-06-18 | Bernard Bolton | Suture extender and needle guard |
| US5075078A (en) | 1989-10-05 | 1991-12-24 | Abbott Laboratories | Self-performing immunochromatographic device |
| US5135873A (en) | 1989-11-27 | 1992-08-04 | Syntex (U.S.A.) Inc. | Device and method for completing a fluidic circuit which employs a liquid expandable piece of bibulous material |
| US5104812A (en) | 1989-11-27 | 1992-04-14 | Syntex (U.S.A.) Inc. | Device and method for interrupting capillary flow |
| US5260222A (en) | 1989-11-27 | 1993-11-09 | Syntex (U.S.A.) Inc. | Device and method for completing a fluidic circuit which employs a liquid expandable piece of bibulous material |
| US5141850A (en) | 1990-02-07 | 1992-08-25 | Hygeia Sciences, Inc. | Porous strip form assay device method |
| US5096837A (en) | 1990-02-08 | 1992-03-17 | Pacific Biotech, Inc. | Immunochromatographic assay and method of using same |
| DE4005021A1 (de) | 1990-02-19 | 1991-08-22 | Boehringer Mannheim Gmbh | Testtraeger zur analyse einer probenfluessigkeit |
| EP0443231B1 (en) | 1990-02-22 | 1995-11-08 | Editek, Inc. | Multi-layered diagnostic test device for the determination of substances in liquids |
| TW199858B (zh) | 1990-03-30 | 1993-02-11 | Fujirebio Kk | |
| US5258163A (en) | 1990-04-14 | 1993-11-02 | Boehringer Mannheim Gmbh | Test carrier for analysis of fluids |
| US5212060A (en) | 1990-04-27 | 1993-05-18 | Genesis Labs, Inc. | Dry test strip comprising a dextran barrier for excluding erythrocytes |
| DE4015590A1 (de) | 1990-05-15 | 1991-11-21 | Boehringer Mannheim Gmbh | Testtraeger zur bestimmung von ionen |
| US5238652A (en) | 1990-06-20 | 1993-08-24 | Drug Screening Systems, Inc. | Analytical test devices for competition assay for drugs of non-protein antigens using immunochromatographic techniques |
| US5158869A (en) | 1990-07-06 | 1992-10-27 | Sangstat Medical Corporation | Analyte determination using comparison of juxtaposed competitive and non-competitive elisa results and device therefore |
| US5119941A (en) | 1990-11-23 | 1992-06-09 | Lepie Eric J | Matchbook-like personal dental and nail hygiene apparatus and method |
| US5294369A (en) | 1990-12-05 | 1994-03-15 | Akzo N.V. | Ligand gold bonding |
| US5106582A (en) | 1990-12-18 | 1992-04-21 | Smithkline Diagnostics, Inc. | Specimen test slide and method of testing for fecal occult blood |
| US5143210A (en) | 1991-01-31 | 1992-09-01 | Warwick S John | Foldable protective package for storing, dispensing, and displaying diagnostic kit components |
| US5252492A (en) | 1991-03-12 | 1993-10-12 | University Of Utah Research Foundation | Fluorescence assay for ligand or receptor utilizing size exclusion |
| JPH04351962A (ja) | 1991-05-29 | 1992-12-07 | Mochida Pharmaceut Co Ltd | 特異結合分析方法および特異結合分析装置 |
| US6168956B1 (en) * | 1991-05-29 | 2001-01-02 | Beckman Coulter, Inc. | Multiple component chromatographic assay device |
| US5314804A (en) | 1992-03-24 | 1994-05-24 | Serim Research Corporation | Test for Helicobacter pylori |
| US5308580A (en) | 1992-05-19 | 1994-05-03 | Millipore Corporation | Sample collection and analytical device |
| US5278079A (en) | 1992-09-02 | 1994-01-11 | Enzymatics, Inc. | Sealing device and method for inhibition of flow in capillary measuring devices |
| US5426191A (en) * | 1993-12-03 | 1995-06-20 | Warner-Lambert Company | Process for the synthesis of 3-chlorobenzo[b]thiophene-2-carbonyl chlorides |
-
1993
- 1993-03-31 US US08/040,430 patent/US5877028A/en not_active Expired - Lifetime
-
1994
- 1994-03-31 ES ES94912379T patent/ES2131191T3/es not_active Expired - Lifetime
- 1994-03-31 BR BR9406755A patent/BR9406755A/pt active Search and Examination
- 1994-03-31 AU AU64970/94A patent/AU678461B2/en not_active Ceased
- 1994-03-31 JP JP52239294A patent/JP3506178B2/ja not_active Expired - Fee Related
- 1994-03-31 PL PL94310953A patent/PL310953A1/xx unknown
- 1994-03-31 EP EP94912379A patent/EP0692097B1/en not_active Expired - Lifetime
- 1994-03-31 SK SK1227-95A patent/SK122795A3/sk unknown
- 1994-03-31 CN CN94192256A patent/CN1124524A/zh active Pending
- 1994-03-31 WO PCT/US1994/003568 patent/WO1994023300A1/en active IP Right Grant
- 1994-03-31 AT AT94912379T patent/ATE177206T1/de not_active IP Right Cessation
- 1994-03-31 DK DK94912379T patent/DK0692097T3/da active
- 1994-03-31 RU RU95118163A patent/RU2124729C1/ru active
- 1994-03-31 DE DE69416828T patent/DE69416828T2/de not_active Expired - Fee Related
- 1994-03-31 NZ NZ263754A patent/NZ263754A/en unknown
- 1994-03-31 HU HU9502835A patent/HUT73379A/hu unknown
-
1995
- 1995-09-27 FI FI954591A patent/FI954591A/fi unknown
- 1995-09-29 OA OA60717A patent/OA10233A/en unknown
- 1995-09-29 NO NO953872A patent/NO953872L/no not_active Application Discontinuation
- 1995-09-30 KR KR1019950704262A patent/KR960702109A/ko not_active Application Discontinuation
- 1995-10-30 BG BG100104A patent/BG100104A/xx active Pending
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN100430726C (zh) * | 1999-10-25 | 2008-11-05 | 松下电器产业株式会社 | 免疫色谱试验片及色谱分析方法 |
| US7270995B2 (en) | 2000-05-25 | 2007-09-18 | Nichirei Biosciences | Analyzing device |
| CN100427950C (zh) * | 2001-08-03 | 2008-10-22 | 麦美华股份有限公司 | 快速诊断装置,分析方法及多功能缓冲液 |
| CN101426898B (zh) * | 2006-03-31 | 2013-03-06 | 拉敏纳股权公司 | 一体式筛选和确认设备 |
| CN105319278A (zh) * | 2014-07-08 | 2016-02-10 | 哈尔滨飞机工业集团有限责任公司 | 一种超声对比试块嵌入件放置方法 |
| CN104865340A (zh) * | 2015-05-12 | 2015-08-26 | 华南理工大学 | 一种用于进行薄层板手动浸渍操作的装置 |
| CN114384190A (zh) * | 2016-06-29 | 2022-04-22 | 安捷伦科技有限公司 | 用于降低柱流失携带效应的方法和系统 |
| CN109187962A (zh) * | 2017-10-07 | 2019-01-11 | 贾晓轻 | 血液样本免疫层析诊断试纸条、试剂盒和检测方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US5877028A (en) | 1999-03-02 |
| ATE177206T1 (de) | 1999-03-15 |
| FI954591A (fi) | 1995-11-27 |
| DE69416828T2 (de) | 1999-07-08 |
| AU6497094A (en) | 1994-10-24 |
| EP0692097B1 (en) | 1999-03-03 |
| EP0692097A1 (en) | 1996-01-17 |
| NO953872D0 (no) | 1995-09-29 |
| BR9406755A (pt) | 1996-04-02 |
| KR960702109A (ko) | 1996-03-28 |
| JPH08508569A (ja) | 1996-09-10 |
| NZ263754A (en) | 1997-03-24 |
| JP3506178B2 (ja) | 2004-03-15 |
| WO1994023300A1 (en) | 1994-10-13 |
| HUT73379A (en) | 1996-07-29 |
| DK0692097T3 (da) | 1999-10-04 |
| NO953872L (no) | 1995-11-06 |
| HU9502835D0 (en) | 1995-12-28 |
| SK122795A3 (en) | 1996-06-05 |
| OA10233A (en) | 1997-10-07 |
| AU678461B2 (en) | 1997-05-29 |
| ES2131191T3 (es) | 1999-07-16 |
| BG100104A (en) | 1996-05-31 |
| PL310953A1 (en) | 1996-01-08 |
| RU2124729C1 (ru) | 1999-01-10 |
| FI954591A0 (fi) | 1995-09-27 |
| DE69416828D1 (de) | 1999-04-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1124524A (zh) | 由可相互对折叠合的构件构成的色谱测定装置 | |
| CN1142868A (zh) | 具有用于调节施加试剂的屏障的测定装置 | |
| CN1250970C (zh) | 分析化验装置和方法 | |
| CN101031798A (zh) | 侧向流系统和测定 | |
| CN1201527A (zh) | 具有传导阻片的对置部件分析装置 | |
| CN1137316A (zh) | 阻断流分析装置 | |
| CN1191603A (zh) | 竞争性免疫测定装置 | |
| CN101035429A (zh) | 定量侧向流系统和测定 | |
| AU2002331408B2 (en) | Diagnostic testing process and apparatus | |
| US7875435B2 (en) | Diagnostic testing process | |
| CN1217189C (zh) | 测定全血样品中白细胞个数的方法 | |
| CN100351990C (zh) | 滞留层析和蛋白质芯片排列在生物学和医药上的应用 | |
| CN1798976A (zh) | 口蹄疫的诊断方法及诊断试剂盒 | |
| AU730243B2 (en) | Detachable-element assay device | |
| CN1564945A (zh) | 快速诊断装置,分析方法及多功能缓冲液 | |
| CN101065497A (zh) | 用于亲和分离的微泡 | |
| CN1627070A (zh) | 制备水溶性交联轭合物的方法 | |
| US20150251177A1 (en) | Strip for lateral flow assay, comprising subpad, and cartridge for lateral flow assay used for the same | |
| CN1784600A (zh) | 层析分析系统 | |
| CN1636138A (zh) | 包括相关方法的磁性光学生物盘和系统 | |
| CN1659439A (zh) | 利用光学生物盘系统基于细胞核形态学的白血细胞类型的识别和定量 | |
| CN1764839A (zh) | 固相免疫层析试验方法 | |
| CN109425733A (zh) | 微流控芯片检测装置、其使用方法及应用设备 | |
| CN1833169A (zh) | 测量对象物测量器具、测量装置和测量方法 | |
| CN207472894U (zh) | 微流控芯片检测装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |