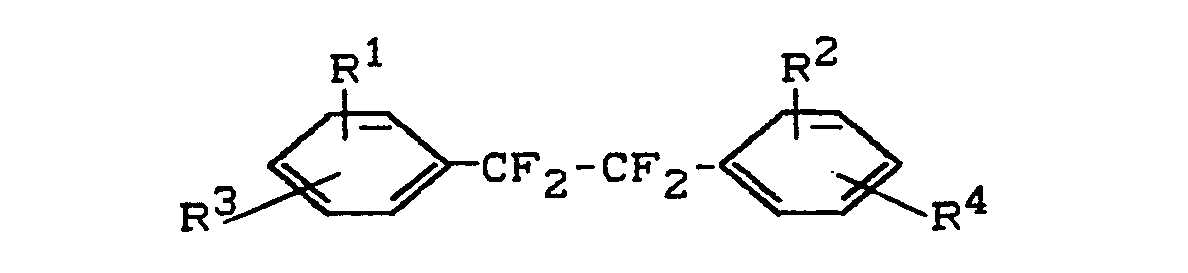EP0201031A2 - (Meth)-Acrylsäureester und ihre Verwendung - Google Patents
(Meth)-Acrylsäureester und ihre Verwendung Download PDFInfo
- Publication number
- EP0201031A2 EP0201031A2 EP86105902A EP86105902A EP0201031A2 EP 0201031 A2 EP0201031 A2 EP 0201031A2 EP 86105902 A EP86105902 A EP 86105902A EP 86105902 A EP86105902 A EP 86105902A EP 0201031 A2 EP0201031 A2 EP 0201031A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- meth
- acrylic acid
- different
- hydrogen
- acid esters
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 *C=CC(NN)=CC=N* Chemical compound *C=CC(NN)=CC=N* 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F20/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride, ester, amide, imide or nitrile thereof
- C08F20/02—Monocarboxylic acids having less than ten carbon atoms, Derivatives thereof
- C08F20/10—Esters
- C08F20/26—Esters containing oxygen in addition to the carboxy oxygen
- C08F20/30—Esters containing oxygen in addition to the carboxy oxygen containing aromatic rings in the alcohol moiety
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K6/00—Preparations for dentistry
- A61K6/20—Protective coatings for natural or artificial teeth, e.g. sealings, dye coatings or varnish
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K6/00—Preparations for dentistry
- A61K6/30—Compositions for temporarily or permanently fixing teeth or palates, e.g. primers for dental adhesives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K6/00—Preparations for dentistry
- A61K6/80—Preparations for artificial teeth, for filling teeth or for capping teeth
- A61K6/884—Preparations for artificial teeth, for filling teeth or for capping teeth comprising natural or synthetic resins
- A61K6/887—Compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K6/00—Preparations for dentistry
- A61K6/80—Preparations for artificial teeth, for filling teeth or for capping teeth
- A61K6/884—Preparations for artificial teeth, for filling teeth or for capping teeth comprising natural or synthetic resins
- A61K6/891—Compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
- A61K6/893—Polyurethanes
Definitions
- the invention relates to new fluorine-containing acrylic acid and methacrylic acid esters, hereinafter referred to as (meth) acrylic acid esters, and their preparation.
- the new compounds can be used as monomers for use in the dental field.
- Fluorine-containing phenylcarbinol acrylates such as 1,1,1,3,3,3-hexafluoro-2-phenyl-2-acryloxypropane are from Org. Coat. Plastic. Chem. 42, 204-207, (1980).
- Similar (meth) acrylic esters such as 1,3-bis (2- (meth) acrylic-oxy-1,1,1,3,3,3-hexafluoropropyl-2) -5-perfluoroalkyl-benzene and their use the dental field are described in US 4,356,296.
- the carbinols are acidified by the trifluoromethyl groups and the carbinol esters produced therefrom are distinguished by a reduced resistance to hydrolysis. This limits their usability as dental monomers.
- Monomers of this type provide dental materials with insufficient mechanical properties.
- the new (meth) -acrylic acid esters are colorless, non-volatile and, after polymerisation, result in transparent plastics.
- the materials obtained in this way are characterized by great resistance to physical and chemical stress. Of particular note are the favorable surface properties and low water absorption of the polymers obtained with the new (meth) acrylic acid esters.
- a C 1 to C 4 alkyl radical generally means a straight-chain or branched hydrocarbon radical. Examples include methyl, ethyl, propyl, isopropyl, butyl and isobutyl. The methyl radical is preferred.
- AC 2 to C 8 alkylene chain generally means a straight-chain or branched double-bonded hydrocarbon chain. Examples include ethylene, propylene, iso-propylene, butylene, iso-butylene, pentylene, iso-pentylene, hexylene, iso-hexylene, heptylene, iso-heptylene, octylene and iso-octylene.
- the substituents R 3 and R 4 can preferably be in the 3,3'- or 3,4'- or 4,4'-position in the 1,2-diphenyl-tetrafluoroethane. Compounds with R 3 and R 4 in the 4,4'-position are particularly preferred.
- ⁇ , ⁇ -dihydroxy compounds can be, for example, ethylene glycol, propylene glycol, diethylene glycol or triethylene glycol.
- Reactive derivatives of (meth) acrylic acid are, for example, the acid halides, preferably the chlorides and esters, preferably esters of lower alcohols.
- the oxyalkylation of the compounds III with the ⁇ , ⁇ -dihydroxy compounds described above is carried out in the presence of strong bases in the temperature range from 50 to 180 ° C., preferably 100 to 160 ° C.
- strong bases can have a PK B value of less than 3, preferably less than 2, particularly preferably less than 0.
- Examples include potassium tert-butoxide, sodium and potassium isopropoxide.
- the products are isolated, for example, by pouring the reaction mixture onto ice water and filtering off the precipitated crystals or, in the case of liquid products, extracting them with a water-insoluble solvent.
- the number of attached oxyalkylene units (n) is variable within wide limits.
- N can preferably assume the values 1 or 2.
- the (meth) acrylic acid esters (I) according to the invention are obtained from the hydroxyl compounds of the formula (V) by esterification or by reaction with isocyanatoalkyl (meth) acrylates.
- esterification For the esterification, (meth) acrylic acid, (meth) acrylic acid chloride, (meth) acrylic acid anhydride or (meth) acrylic acid esters of lower alcohols can be used.
- the esterification is preferably carried out with (meth) acrylic acid in the presence of an acid catalyst, for example p-toluenesulfonic acid, sulfuric acid or ion exchangers in the H e form in a solvent which is immiscible with water, for example toluene, chloroform, xylene, etc.
- an acid catalyst for example p-toluenesulfonic acid, sulfuric acid or ion exchangers in the H e form in a solvent which is immiscible with water, for example toluene, chloroform, xylene, etc.
- Suitable polymerization inhibitors are, for example, 2,6-di-tert-butyl-4-methylphenol, methylene blue and hydroquinone in an amount of 0.01 to 1% by weight.
- unreacted (meth) acrylic acid is removed by extraction with a basic aqueous solution.
- the inhibitor is separated off, for example, by adding adsorbents.
- the reaction products according to the invention are isolated by distilling off the solvents.
- the conversion to urethane is preferably carried out with the exclusion of water in an inert solvent.
- suitable solvents are: chloroform, tetrahydrofuran, dioxane, methylene chloride, toluene and acetonitrile.
- Preferred solvents are chloroform, tetrahydrofuran and acetonitrile.
- the reaction is generally carried out in the temperature range from 20 to 100 ° C., preferably 30 to 70 ° C.
- Catalysts containing tin, such as dibutyltin dilaurate or tin (II) octoate, are preferably used to accelerate the reaction.
- Other suitable catalysts are compounds with tert. Amino groups and titanium compounds. In general, the catalyst is used in an amount of 0.01 to 2.5% by weight, preferably 0.1 to 1.5% by weight, based on the total amount of the reactants.
- the conversion to urethane is generally carried out in the presence of 0.01 to 0.2% by weight of a polymerization inhibitor, for example 2,6-di-tert-butyl-4-methylphenol Normal pressure carried out.
- a polymerization inhibitor for example 2,6-di-tert-butyl-4-methylphenol Normal pressure carried out.
- reaction solution After the addition of the polymerization inhibitor, the reaction solution is heated to a temperature between 20 and 100 ° C.
- the time course of the implementation can be followed, for example, by measuring the IR spectra. After the isocyanate groups have reacted completely, the reaction products are isolated by removing the solvent. Prior cleaning with the aid of adsorbents, for example activated carbon, bleaching earth, silica gel or aluminum oxide, is possible.
- adsorbents for example activated carbon, bleaching earth, silica gel or aluminum oxide
- the (meth) acrylic acid esters of the formula 1 according to the invention can be mixed with monomers known per se, for example in order to adapt the viscosity to the intended use. Viscosities in the range from 60 to 10,000 mPas are preferred. This can be achieved by using the Monomers according to the invention optionally admixed a comonomer of lower viscosity as a reactive diluent.
- the compounds according to the invention are used in a mixture with comonomers in a proportion of approximately 30 to approximately 90% by weight, a proportion of 50 to 90% by weight being particularly preferred.
- the (meth) -acrylic acid esters according to the invention can be cured, if appropriate in a mixture with the monomer mentioned, using methods known per se (GM Brauer, H. Argentar, Am. Chem. Soc., Symp. Ser. 212, S 359-371 ( 1983)).
- redox polymerization is a system of a peroxidic compound and one Reducing agents, for example based on tertiary aromatic amines, are suitable, the peroxide-containing and amine-containing monomer mixture having to be stored separately until use in order to prevent premature polymerization.
- tertiary aromatic amines are N, N-dimethyl-p-toluidine, bis- (2-hydroxyethyl) -p-toluidine, bis (2-hydroxyethyl) -3,5-dimethylaniline and that in German Pat. No. 2,759,239 N-methyl-N- (2-methylcarbamoyl-oxypropyl) -3,5-dimethylaniline described.
- the concentration of the peroxide or of the amine is advantageously chosen so that it is 0.1 to 5% by weight, preferably 0.5 to 3% by weight, based on the monomer mixture.
- the monomers according to the invention can also be brought to polymerization by irradiation with UV light or visible light (for example in the wavelength range from 230 to 650 nm).
- Suitable initiators for the photo-initiated polymerization are, for example, benzil, benzil dimethyl ketal, benzoin monoalkyl ether, benzophenone, p-methoxybenzophenone, fluorenone, thioxanthone, phenanthrenequinone and 2,3-bornandione (camphorquinone), optionally in the presence of synergistic photoactivators such as N, N-methacrylate , Triethanolamine, 4-N, N-dimethylaminobenzenesulfonic acid bisallylamide.
- synergistic photoactivators such as N, N-methacrylate , Triethanolamine, 4-N, N-dimethylaminobenzenesulfonic acid bisallylamide.
- light stabilizers and polymerization inhibitors known per se for this purpose can be added to the (meth) acrylic acid esters according to the invention.
- the light stabilizer and the polymerization inhibitor are generally used in an amount of 0.01 to 0.50 parts by weight, based on 100 parts by weight of the monomer mixture.
- the monomer mixtures can be used as coating agents (tooth varnishes) without the addition of fillers.
- fillers When used as tooth filling compounds, fillers are generally added to the monomer mixtures obtained. Around To be able to achieve a high degree of filling, monomer mixtures which have a viscosity in the range from 60 to 10,000 mPas are particularly advantageous.
- the monomer mixtures containing the compounds of the formula I according to the invention can preferably be admixed with inorganic fillers. For example, rock crystal, quartzite, crystallobalite, quartz glass, highly disperse silica, aluminum oxide and glass ceramics, for example glass ceramics containing lanthanum and zircon (DE-OS 23 47 591) may be mentioned.
- the inorganic fillers are preferably pretreated with an adhesion promoter.
- the adhesion can be achieved, for example, by treatment with organosilicon compounds (Plueddemann, Progress in Organic coatings, 11, 297 to 308 (1983)).
- 3-Methacryloyloxypropyltrimethoxysilane is preferably used.
- the fillers for the dental filling compositions according to the invention generally have an average particle diameter of 0.01 to 100 ⁇ m, preferably 0.05 to 50 ⁇ m, particularly preferably 0.05 to 5 ⁇ m. It can also be advantageous to use several fillers next to one another which have a different particle diameter.
- the proportion of the (meth) -acrylic acid esters according to the invention in the filling materials is generally 5 to 85% by weight, based on the filling material.
- the filler content in the tooth filling materials is generally 5 to 85% by weight, preferably 50 to 80% by weight.
- the components are processed using kneading machines known per se.
- the liquid hardens when exposed with a dental lamp (exposure time 40 seconds).
- Example 6 was repeated using the monomer from Example 4.
- the cured coating solutions from Examples 6 and 7 are transparent and have a high hardness.
- Amine paste In a monomer mixture of 80 parts by weight of the compound according to the invention from Example 5 and 20 parts by weight of triethylene glycol dimethacrylate, 2.2% by weight of N-methyl-N- (2-methylcarbamoyloxypropyl) -3,5-dimethylaniline and 0.04% by weight .-% of the polymerization inhibitor from Example 6 dissolved. 5 g of this solution are processed into a paste with 15 g of a commercially available glass ceramic with an average particle diameter of 4 ⁇ m, which was silanized with 3-methacryloyloxypropyltrimethoxysilane.
- Peroxide paste 2.0 parts by weight of dibenzoyl peroxide are dissolved in a mixture of 80 parts by weight of the compound according to the invention from Example 5 and 20 parts by weight of triethylene glycol dimethacrylate. 5 g of this solution are processed into a paste with 15 g of a commercially available glass ceramic with an average particle diameter of 4 ⁇ m, which was silanized with 3-methacryloyloxypropyltrimethoxysilane.
- a mixture of equal parts of amine paste and peroxide paste hardens within 2 to 3 minutes.
- the curing takes place by exposure with a dental lamp. With an exposure time of 40 seconds, the curing depth is 6.1 mm.
- Example 9 was repeated using the compound from Example 4.
Abstract
Description
- Die Erfindung betrifft neue fluorhaltige Acrylsäure- und Methacrylsäureester, im folgenden (Meth)-Acrylsäureester genannt, und ihre Herstellung. Die neuen Verbindungen können als Monomere für die Anwendung im Dentalbereich eingesetzt werden.
- Fluorhaltige Phenylcarbinol-acrylate wie 1,1,1,3,3,3-Hexafluor-2-Phenyl-2-acryloxy-propan sind aus Org. Coat. Plast. Chem. 42, 204-207, (1980) bekannt. Ähnlich aufgebaute(Meth)acrylsäureester, wie l,3-Bis-(2-(meth)acryl- oxy-1,1,1,3,3,3-hexafluoropropyl-2)-5-perfluoralkyl-benzol und ihre Verwendung auf dem Dentalgebiet werden in der US 4 356 296 beschrieben. Durch die Trifluormethylgruppen werden die Carbinole acidifiziert und die daraus hergestellten Carbinolester zeichnen sich durch eine verminderte Hydrolysenbeständigkeit aus. Dadurch ist ihre Verwendbarkeit als Dentalmonomere eingeschränkt.
- Weiterhin ist die Verwendung von 1,1,5-Trihydro-octafluoro-pentyl-methacrylat in Zahnfüllmassen in J. Dent. Res. 58, 1181 - 1186 (1979) beschrieben.
- Monomere dieses Typs liefern Dentalmaterialien mit unzureichenden mechanischen Eigenschaften.
-
- R1 und R2 gleich oder verschieden sind und Wasserstoff, Chlor, Fluor oder einen C1- bis C4-Alkylrest bedeuten und
- R3 und R4 gleich oder verschieden sind und für die Gruppe
- R5 und R6 gleich oder verschieden sind und ein Wasserstoffatom oder eine Methylgruppe bedeuten,
- Z eine geradkettige oder verzweigte C2- bis C8-Alkylenkette bedeutet und
- n Werte von 1 bis 4 bedeutet,
- Die neuen (Meth)-Acrylsäureester sind farblos, schwerflüchtig und ergeben nach Polymerisation transparente Kunststoffe.
- Sie lassen sich besonders gut in Abdichtungsmitteln, Klebstoffen und Dentalmaterialien, wie Zahnfüllmassen und Beschichtungsmitteln, verwenden. Die so erhaltenen Materialien zeichnen sich durch eine große Widerstandfähigkeit gegenüber physikalischer und chemischer Beanspruchung aus. Besonders hervorzuheben sind die günstigen Oberflächeneigenschaften und geringe Wasseraufnahme der mit den neuen (Meth)-Acrylsäureestern erhaltenen Polymerisate.
- Im Rahmen der vorliegenden Erfindung können die Substituenten im allgemeinen folgende Bedeutung haben.
- Ein C1- bis C4-Alkylrest bedeutet im allgemeinen ein geradkettiger oder verzweigter Kohlenwasserstoffrest. Beispielsweise seien Methyl, Ethyl, Propyl, iso- Propyl, Butyl und iso-Butyl genannt. Bevorzugt wird der Methylrest.
- Ein C2- bis C8-Alkylenkette bedeutet im allgemeinen eine geradkettige oder verzweigte zweibindige Kohlenwasserstoffkette. Beispielsweise seien Ethylen, Propylen, isoPropylen, Butylen, iso-Butylen, Pentylen, iso-Pentylen, Hexylen, iso-Hexylen, Heptylen, iso-Heptylen, Octylen und iso-Octylen genannt.
-
- R 3 und R4 gleich oder verschieden sind und für die Gruppen
- R5 und R6 gleich oder verschieden sind und ein Wasserstoffatom oder eine Methylgruppe bedeuten,
- Z eine geradkettige oder verzweigte C2- bis C8-Alkylenkette bedeutet und
- n Werte von 1 bis 4 bedeutet.
- Die Substituenten R3 und R4 können bevorzugt in 3,3'- oder 3,4'- oder 4,4'-Stellung im 1,2-Diphenyl-tetrafluorethan stehen. Insbesondere bevorzugt werden Verbindungen mit R3 und R4 in 4,4'-Stellung.
-
-
- R1 und R2 gleich oder verschieden sind und Wasserstoff, Chlor, Fluor oder einen C1- bis C4-Alkylrest bedeuten,
- mit α,ω-Dihydroxy-Verbindungen der Formel
- n Werte von 1 bis 4 und
- R5 Wasserstoff oder Methyl bedeutet,
- Verbindungen der Formel III sind beispielsweise gemäß L.M. Yagupolskii, V.I. Troitskaya, Zh. Obshch. Khim. 35. (9), 1620 (1965) bzw. J. Gen. Chem.. U.S.S.R. 35, 1616 bis 1623 (1965) zugänglich.
- α,ω-Dihydroxyverbindungen können beispielsweise Ethylenglykol, Propylenglykol, Diethylenglykol oder Triethylenglykol sein.
- Reaktive Derivate der (Meth)-acrylsäure sind beispielsweise die Säurehalogenide, bevorzugt die Chloride und Ester, bevorzugt Ester niederer Alkohole.
- Die Oxyalkylierung der Verbindungen III mit den oben beschriebenen α,ω-Dihydroxyverbindungen wird in Gegenwart starker Basen im Temperaturbereich von 50 bis 180°C, bevorzugt 100 bis 160°C, durchgeführt.
- Starke Basen können erfindungsgemäß einen PKB-Wert von kleiner als 3, bevorzugt kleiner als 2, insbesondere bevorzugt kleiner als 0, haben. Beispielsweise seien Kalium-tert.-butylat, Natrium- und Kaliumisopropylat genannt.
- Die Produkte werden beispielsweise isoliert, indem man die Reaktionsmischung auf Eiswasser gibt und die ausgefallenen Kristalle absaugt oder bei flüssigen Produkten mit einem wasserunlöslichen Lösungsmittel extrahiert.
-
- R1 und R2 die oben erwähnte Bedeutung haben,
- R5 Wasserstoff oder eine Methylgruppe und
- n Werte von 1 bis 4 bedeutet.
- Die Anzahl der angelagerten Oxyalkylen-Einheiten (n) ist in weiten Grenzen variabel.
- Bevorzugt kann n die Werte 1 oder 2 annehmen.
-
- n Werte von 1 bis 4 annimmt und
- R4 ein Wasserstoffatom oder eine Methylgruppe bedeutet.
- Die erfindungsgemäßen (Meth)Acrylsäureester (I) werden aus den Hydroxylverbindungen der Formel (V) durch Veresterung beziehungsweise durch Umsetzung mit Isocyanatoalkyl(meth)-acrylaten erhalten.
- Zur Veresterung können (Meth)-Acrylsäure, (Meth)acrylsäurechlorid, (Meth)-Acrylsäureanhydrid oder (Meth)Acrylsäureester niederer Alkohole eingesetzt werden. Die Veresterung erfolgt vorzugsweise mit (Meth)Acrylsäure in Anwesenheit eines sauren Katalysators, zum Beispiel p-Toluolsulfonsäure, Schwefelsäure oder Ionenaustauschern in der He-Form in einem Lösungsmittel, das mit Wasser nicht mischbar ist, zum Beispiel Toluol, Chloroform Xylol usw.
- Die Veresterung kann beispielsweise wie folgt durchgeführt werden:
- Die Hydroxylverbindung und ein Überschuß von (Meth)-Acrylsäure werden in einem Lösungsmittel suspendiert oder gelöst und mit dem sauren Katalysator sowie einem Polymerisations-Inhibitor versetzt. Das während der Veresterung gebildete Wasser wird durch azeotrope Destillation aus dem Gleichgewicht entfernt. Die Reaktion wird im allgemeinen im Temperaturbereich von 50°C bis etwa 120°C (Siedepunkt des azeotropen Gemisches etwa 100°C) durchgeführt.
- Geeignete Polymerisations-Inhibitoren sind beispielsweise 2,6-Di-tert.- Butyl-4-methyl-phenol, Methylenblau und Hydrochinon in einer Menge von 0,01 bis 1 Gew.-%. Nach beendeter Veresterung wird nicht umgesetzte (Meth)-Acrylsäure durch Extraktion mit einer basischen wäßrigen Lösung entfernt. Der Inhibitor wird beispielsweise durch Zusatz von Adsorbentien abgetrennt. Die erfindungsgemäßen Reaktionsprodukte werden durch Abdestillieren der Lösungsmittel isoliert.
-
- Z eine geradkettige oder verzweigte C2- bis C8-Alkylenkette und
- R6 ein Wasserstoffatom oder eine Methylgruppe bedeuten. Geeignete Isocyanatoalkyl(meth)acrylate sind 2-Isocyanatoethylmethacrylat, 2-Isocyanatopropylmethacrylat und 1,2-Dimethyl-3-isocyanatopropylacrylat.
- Die Umsetzung zum Urethan erfolgt vorzugsweise unter Wasserausschluß in einem inerten Lösungsmittel. Beispiele für geeignete Lösungsmittel sind: Chloroform, Tetrahydrofuran, Dioxan, Methylenchlorid, Toluol und Acetonitril. Bevorzugte Lösungsmittel sind Chloroform, Tetrahydrofuran und Acetonitril.
- Die Umsetzung wird im allgemeinen im Temperaturbereich von 20 bis 100°C, vorzugsweise 30 bis 70°C durchgeführt. Zur Beschleunigung der Umsetzung werden vorzugseise zinnhaltige Katalysatoren wie Dibutylzinndilaurat oder Zinn(II)-octoat verwendet. Andere geeignete Katalysatoren sind Verbindungen mit tert. Aminogruppen und Titanverbindungen. Im allgemeinen wird der Katalysator in einer Menge von 0,01 bis 2,5 Gew.-X, bevorzugt von 0,1 bis 1,5 Gew.-%, bezogen auf die Gesamtmenge der Reaktanden, eingesetzt.
- Die Umsetzung zum Urethan wird im allgmeinen in Gegenwart von 0,01 bis 0,2 Gew.-% eines Polymerisations-Inhibitors, beispielsweise 2,6-Di-tert.-Butyl-4-methylphenol bei Normaldruck durchgeführt. Es ist aber auch möglich, das erfindungsgemäße Verfahren bei einem Unter- oder Überdruck durchzuführen.
- Die Reaktion kann beispielsweise wie folgt durchgeführt werden:
- Ein Isocyanatoalkyl(meth)acrylat (VII) und eine Hydroxylverbindung (V) werden in dem Lösungsmittel gelöst oder suspendiert und unter Rühren mit dem Katalysator versetzt.
- Nach Zugabe des Polymerisations-Inhibitors wird die Reaktionslösung auf eine Temperatur zwischen 20 und 100°C erwärmt.
- Der zeitliche Verlauf der Umsetzung kann beispielsweise durch Messung der IR-Spektren verfolgt werden. Nach vollständiger Umsetzung der Isocyanatgruppen werden die Reaktionsprodukte durch Entfernen des Lösungsmittels isoliert. Eine vorherige Reinigung mit Hilfe von Adsorbentien, beispielsweise Aktivkohle, Bleicherde, Kieselgel oder Aluminiumoxid ist möglich.
- Für die Anwendung als Monomere für Zahnfüllmassen oder Beschichtungsmittel (Zahnlacke) im Dentalbereich können die erfindungsgemäßen (Meth)-Acrylsäureester der Formel 1 mit an sich bekannten Monomeren gemischt werden, um beispielsweise die Viskosität dem Verwendungszweck anzupassen. Viskositäten im Bereich von 60 bis 10000 mPas sind dabei bevorzugt. Dies ist dadurch erreichbar, daß man den erfindungsgemäßen Monomeren gegebenenfalls ein Comonomer niedrigerer Viskosität als Reaktivverdünner zumischt. Die erfindungsgemäßen Verbindungen werden in der Mischung mit Comonomeren mit einem Anteil von ca. 30 bis ca. 90 Gew.-% eingesetzt, wobei ein Anteil von 50 bis 90 Gew.-% besonders bevorzugt ist.
- Im Rahmen der vorliegenden Erfindung ist es ebenfalls möglich, Mischungen verschiedener erfindungsgemäßer (Meth)-Acrylsäureester einzusetzen.
- Es ist auch möglich, Monomermischungen einzusetzen, die mehrere Comonomere als Reaktivverdünner enthalten.
- Beispielsweise seien die folgenden Comonomere genannt:
- Triethylenglykoldimethacrylat, Tetraethylenglykoldimethacrylat, 1,12-Dodecandioldimethacrylat, 1,6-Hexandioldimethacrylat, Diethylenglykoldimethacrylat, (Meth)acrylsäureester ethoxylierter oder propoxylierter hydroxylgruppenhaltiger Tricyclo[5.2.1.02,6]decan-Derivate (vgl. DE-OS 2 931 925 und 2 931 926). Insbesondere werden Comonomere bevorzugt, die bei 13 mbar einen Siedepunkt über 100°C besitzen.
- Die erfindungsgemäßen (Meth)-Acrylsäureester lassen sich, gegebenenfalls in Mischung mit dem genannten Monomeren, mit an sich bekannten Methoden aushärten (G. M. Brauer, H. Argentar, Am. Chem. Soc., Symp. Ser. 212, S 359-371 (1983)). Für die sogenannte Redoxpolymerisation ist ein System aus einer peroxidischen Verbindung und einem Reduktionsmittel, beispielsweise auf Basis tertiärer aromatischer Amine, geeignet, wobei die peroxidhaltige und aminhaltige Monomermischung bis zur Verwendung getrennt gelagert werden müssen, um eine vorzeitige Polymerisation zu verhindern.
- Beispiele für geeignete Peroxide sind:
- Dibenzoylperoxid, Dilauroylperoxid und Di-Chlorbenzoylperoxid.
- Als tertiäre aromatische Amine seien beispielsweise N,N-Dimethyl-p-toluidin, Bis-(2-hydroxyethyl)-p-toluidin, Bis(2-hydroxyethyl)-3,5-dimethylanilin und das in der DE-PS 2 759 239 beschriebene N-Methyl-N-(2-Methylcarbamoyl- oxypropyl)-3,5-dimethylanilin genannt.
- Die Konzentration des Peroxids bzw. des Amins werden vorteilhaft so gewählt, daß sie 0,1 bis 5 Gew.-%, bevorzugt 0,5 bis 3 Gew.-%, bezogen auf die Monomermischung betragen.
- Die erfindungsgemäßen Monomeren können auch durch Bestrahlung mit UV-Licht oder sichtbarem Licht (beispielsweise im Wellenlängenbereich von 230 bis 650 nm) zur Polymerisation gebracht werden.
- Es handelt sich dabei um ein Einkomponentensystem. Der Vorteil gegenüber redoxhärtenden Zweikomponentensystemen besteht darin, daß die Aushärtung der Monomermischung nicht durch Inhomogenitäten beeinträchtigt wird, die beim Redoxsystem durch unzureichende Durchmischung der beiden Komponenten verursacht werden können.
- Als Initiatoren für die photoinitiierte Polymerisation eignen sich beispielsweise Benzil, Benzildimethylketal, Benzoinmonoalkylether, Benzophenon, p-Methoxybenzophenon, Fluorenon, Thioxanthon, Phenanthrenchinon und 2,3-Bornandion (Campherchinon), gegebenenfalls in Gegenwart von synergistisch wirkenden Photoaktivatoren, wie N,N-Dimethylaminoethylmethacrylat, Triethanolamin, 4-N,N-Di- methylaminobenzolsulfonsäurebisallylamid. Die Durchführung des Photopolymerisationsverfahrens ist beispielsweise in der DE-PS 3 135 115 beschrieben.
- Neben den oben beschriebenen Initiatoren können den erfindungsgemäßen (Meth)-Acrylsäureestern an sich für diesen Einsatzzweck bekannte Lichtschutzmittel und Polymerisations-Inhibitoren zugesetzt werden.
- Das Lichtschutzmittel und der Polymerisations-Inhibitor werden im allgemeinen in einer Menge von 0,01 bis 0,50 Gew.-Teilen, bezogen auf 100 Gew.-Teile der Monomermischung eingesetzt. Die Monomermischungen können ohne Zusatz von Füllstoffen als Beschichtungsmittel (Zahnlacke) eingesetzt werden.
- Bei der Verwendung als Zahnfüllmassen setzt man den erhaltenen Monomermischungen im allgemeinen Füllstoffe zu. Um einen hohen Füllgrad erreichen zu können, sind Monomermischungen, die eine Viskosität im Bereich von 60 bis 10000 mPas besitzen, besonders vorteilhaft. Den die erfindungsgemäßen Verbindungen der Formel I enthaltenden Monomermischungen können vorzugsweise anorganische Füllstoffe zugemischt werden. Beispielsweise seien Bergkristall, Quarzit, Kristobalit, Quarzglas, hochdisperse Kieselsäure, Aluminiumoxid und Glaskeramiken, beispielsweise Lanthan und Zirkon enthaltende Glaskeramiken (DE-OS 23 47 591) genannt.
- Die anorganischen Füllstoffe werden zur Verbesserung des Verbundes zur Polymermatrix des Polymethacrylats vorzugsweise mit einem Haftvermittler vorbehandelt. Die Haftvermittlung kann beispielsweise durch eine Behandlung mit Organosiliciumverbindungen erreicht werden (Plueddemann, Progress in Organic coatings, 11, 297 bis 308 (1983)). Bevorzugt wird 3-Methacryloyloxypropyl-trimethoxysilan eingesetzt.
- Die Füllstoffe für die erfindungsgemäßen Zahnfüllmassen weisen im allgemeinen einen mittleren Teilchendurchmesser von 0,01 bis 100 µm, vorzugsweise von 0,05 bis 50 µm auf, besonders bevorzugt 0,05 bis 5 µm. Es kann auch vorteilhaft sein, mehrere Füllstoffe nebeneinander einzusetzen, die einen voneinander verschiedenen Teilchendurchmesser besitzen.
- Der Anteil der erfindungsgemäßen (Meth)-Acrylsäureester in den Füllmassen beträgt im allgemeinen 5 bis 85 Gew.-X, bezogen auf die Füllmasse.
- Der Füllstoffanteil in den Zahnfüllmassen beträgt im allgemeinen 5 bis 85 Gew.-%, vorzugsweise 50 bis 80 Gew.-%.
- Für die Herstellung der Zahnfüllmassen werden die Komponenten unter Verwendung von an sich bekannten Knetmaschinen verarbeitet.
-
- A) Herstellung von 1,2-Bis[4-(2-Hydroxyethoxy)phenyl]-1,1,2,2-tetrafluorethan
- B) Herstellung von 1,2-Bis[4-(2-Hydroxyethoxyethoxy)-pheny]-1,1,2,2-'tetrafluorethan
- Herstellung von 1,2-Bis-[4-(2-Methacryloyloxy-ethoxy)-phenyl]-1,1,-2,2-tetrafluorethan
- 37,4 g (0,1 mol) 1,2-Bis-[4-(2-Hydroxy-ethoxy)phenyl]-1,1,2,2,-tetrafluorethan
- 25,8 g (0,3 mol) Methacrylsäure
- 1 g p-Toluolsulfonsäure und
- 0,3 g Methylenblau
- werden in 100 ml Toluol suspendiert. Bei 110°C wird durch azeotrope Destillation das Wasser ausgekreist, wobei durch die Suspension Luft geleitet wurde. Nach beendeter Wasserabscheidung wird mit Bleicherde ausgerührt, abgesaugt und das Filtrat mit Natriumhydrogencarbonat-Lösung extrahiert. Die organische Phase wird mit Zellstoffmehl verrührt und abgesaugt. Anschließend wird mit Natriumchlorid-Lösung neutral gewaschen. Die organische Phase wird über Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit.
- Ausbeute: 39,3 g (77 %)
- Schmelzpunkt: 84 bis 85°C
- GC-Analyse: 97 %
- Herstellung von 1,2-Bis-[4-(2-Methacryloyloxy-ethoxy- ethoxy)phenylll,1,2,2-tetrafluorethan
- 46,2 g (0,1 mol) 1,2-Bis-[4-(2-Hydroxy-ethoxyethoxy)-phenyl)1,1,2,2-tetrafluorethan
- 25,8 g (0,3 mol) Methacrylsäure
- 1 g p-Toluolsulfonsäure und
- 0,3 g Methylenblau werden in
- 150 ml Toluol suspendiert.
- Unter Einleiten von Luft wird während 24 Stunden das Reaktionswasser kontinuierlich ausgekreist. Nach beendeter Reaktion wird mit Bleicherde ausgerührt, abgesaugt und das Filtrat mit Natriumhydrogencarbonat-Lösung extrahiert. Die organische Phase wird mit Zellstoffmehl verrührt und abgesaugt. Anschließend wird mit Natriumchlorid-Lösung neutral gewaschen. Die Toluolphase wird über Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit.
- Ausbeute: 53,5 g (89,5 %) Schmelzpunkt: 64 bis 66°C 1H-NMR (CDC13) [ppm]: 1,95 (-CH3, 6H), 4,5 - 3,7 (-CH2-, 16H), 5,5 - 5,65 und 6,2 - 6,05 (=CH2, 4H), 6,75 - 7,5 (1,4-disubstituierter Phenylrest, 8H)
- Herstellung von 1,2-Bis[4-(2-Methacryloyloxyethyl- carbamoyloxy-ethoxyethoxy)phenyl]-1,1,2,2-tetrafluorethan 4,62 g (10 mmol) 1,2-Bis-[4-(2-Hydroxyethoxyethoxy)-phenyl]-1,1,2,2-tetrafluorethan werden in 30 ml Chloroform gelöst.
- 0,03 g Zinn(II)octoat und 0,003 g 2,6-Di-tert.-Butyl-4-methylphenol werden zugegeben. Langsam werden 3,1 g (20 mmol) 2-Isocyanatoethylmethacrylat bei Raumtemperatur zugetropft. Nach beendeter Zugabe des Isocyanats wird die Reaktionsmischung bei 50°C gerührt, bis die IR-Absorption der NCO-Bande bei 2200 cm-1 verschwunden ist (etwa 5 Stunden Reaktionszeit). Das Produkt wird durch Entfernen des Lösungsmittels im Vakuum isoliert. Das Urethan ist eine farblose, viskose Flüssigkeit , die beim Abkühlen unter 10°C nach mehreren Tagen kristallin wird.
- Ausbeute: 7,6 g (98,4 %) Die erwartete Struktur wurde durch das 1H-NMR-Spektrum bestätigt.
- Herstellung von 1,2-[4-(2-Methacryloyloxyethoxyethoxy)-4'-(2-acryloyloxy-ethoxyethoxy)]-diphenyl-1,1,2,2-tetrafluorethan
- 46,2 g (0,1 mol) 1,2-Bis-[4-(2-Hydroxyethoxyethoxy)-phenyl]-1,1,2,2-tetrafluorethan
- 12,9 g (0,15 mol) Methacrylsäure
- 10,8 g (0,15 mol) Acrylsäure
- 1 g p-Toluolsulfonsäure und
- 0,3 g Methylenblau
- Die Reaktion und die Aufarbeitung werden analog zu Beispiel 3 geführt. Das Monomer ist nach vollständiger Entfernung des Lösungsmittels eine farblose, viskose Flüssigkeit.
- Ausbeute: 51,7 g
- Herstellung von Beschichtungs-Lösungen
- In einer Lösung aus dem in Beispiel 5 genannten Monomer (80 Gew.-Teile) und Triethylenglykoldimethacrylat (20 Gew.-Teile) werden 2,00 Gew.-% Di-Benzoylperoxid und 0,04 Gew.-% 2,6-Di-tert.-Butyl-4-methylphenol gelöst.
- In einer zweiten, kein Peroxid enthaltenden, sonst aber gleich zusammengesetzten Mischung werden 2,2 Gew.-X N-Methyl-N-(2-Methylcarbamoyloxy-propyl)-3,5-dimethylanilin gelöst.
- Eine Mischung aus gleichen Teilen der beiden zuvor beschriebenen Lösungen härtet in 2 bis 3 Minuten aus.
- In einer Monomermischung aus 80 Gew.-Teilen Monomer aus Beispiel 5 und 20 Gew.-Teilen Triethylenglykoldimethacrylat werden 0,5 Gew.-% 4-N,N-Dimethylaminobenzol- sulfonsäure-bis-allylamid, 0,125 Gew.-X Benzildimethylketal, 0,2 Gew.-% Bicyclo[2,2,1]-1,7,7-trimethyl-heptan-2,3-dion (2,3-Bornandion) und 0,04 Gew.-% 2,6-Di- tert.-Butyl-4-methylphenol gelöst.
- Beim Belichten mit einer Dentallampe härtet die Flüssigkeit aus (Belichtungszeit 40 Sekunden).
- Beispiel 6 wurde unter Verwendung des Monomers aus Beispiel 4 wiederholt.
- Die ausgehärteten Beschichtungslösungen aus Beispielen 6 und 7 sind transparent und weisen eine hohe Härte auf.
- Aminpaste: In einer Monomer-Mischung von 80 Gewichtsteilen der erfindungsgemäßen Verbindung aus Beispiel 5 und 20 Gewichtsteilen Triethylenglykoldimethacrylat werden 2,2 Gew.-% N-Methyl-N-(2-Methylcarbamoyloxypropyl)-3,5-dimethylanilin und 0,04 Gew.-% des Polymerisations-Inhibitors aus Beispiel 6 gelöst. 5 g dieser Lösung werden mit 15 g einer handelsüblichen Glaskeramik mit einem mittleren Teilchendurchmesser von 4 µm, die mit 3-Methacryloyloxypropyl-trimethoxysilan silanisiert wurde, zu einer Paste verarbeitet.
- Peroxidpaste: In einer Mischung von 80 Gewichtsteilen der erfindungsgemäßen Verbindung aus Beispiel 5 und 20 Gewichtsteilen Triethylenglykoldimethacrylat werden 2,0 Gew.-X Dibenzoylperoxid gelöst. 5 g dieser Lösung werden mit 15 g einer handelsüblichen Glaskeramik mit einem mittleren Teilchendurchmesser von 4 µm, die mit 3-Methacryloyloxypropyl-trimethoxysilan silanisiert wurde, zu einer Paste verarbeitet.
- Eine Mischung von gleichen Teilen Aminpaste und Peroxidpaste härtet innerhalb von 2 bis 3 Minuten aus.
- Herstellung eines lichthärtenden Zahnfüllungsmaterials
- In einer Mischung aus 80 Gewichtsteilen Monomer aus Beispiel 5 und 20 Gewichtsteilen Triethylenglykoldimethacrylat werden 0,2 Gewe-% 2,3-Bornandion, 0,125 Gew.-% Benzildimethylketal, 0,5 Gew.-X 4-N,N-Dimethylamino- benzolsulfonsäure-bis-allylamid und 0,04 Gew.-X 2,6-Di- tert.-Butyl-4-Methylphenol gelöst.
- 5 g dieser Lösung werden mit 15 g des in Beispiel 8 beschriebenen Füllstoffs zu einer Paste verarbeitet (75 % Füllstoffgehalt).
- Die Aushärtung erfolgt durch Belichtung mit einer Dentallampe. Bei einer Belichtungszeit von 40 Sekunden beträgt die Aushärtungstiefe 6,1 mm.
- Beispiel 9 wurde unter Verwendung von Verbindung aus Beispiel 4 wiederholt.
- An dem ausgehärteten Beschichtungsmittel aus dem Beispiel 6 wurden Messungen der Oberflächenspannung durchgeführt. Mittels eines Video- Systems wurde das dynamische Benetzungsverhalten von Flüssigkeiten auf den Festkörperoberflächen bestimmt. Die Oberflächenspannungen wurden aus den Anfangsrandwinkeln von 5 Prüfflüssigkeiten berechnet. Die Ergebnisse sind in der Tabelle 2 zusammengestellt.
gefunden.
in Gegenwart einer starken Base verethert und das Reaktionsprodukt mit (Meth)acrylsäure und/oder seinen reaktiven Derivaten verestert oder mit Isocyanatoalkyl-(meth)-acrylaten umsetzt.
werden in 250 ml Toluol suspendiert und 24 Stunden unter Rückfluß erhitzt.
Claims (8)
enthalten.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19853516256 DE3516256A1 (de) | 1985-05-07 | 1985-05-07 | (meth)-acrylsaeureester und ihre verwendung |
| DE3516256 | 1985-05-07 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| EP0201031A2 true EP0201031A2 (de) | 1986-11-12 |
| EP0201031A3 EP0201031A3 (en) | 1988-06-01 |
| EP0201031B1 EP0201031B1 (de) | 1989-08-02 |
Family
ID=6269957
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP86105902A Expired EP0201031B1 (de) | 1985-05-07 | 1986-04-29 | (Meth)-Acrylsäureester und ihre Verwendung |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US4665217A (de) |
| EP (1) | EP0201031B1 (de) |
| JP (1) | JPS61263947A (de) |
| DE (2) | DE3516256A1 (de) |
Cited By (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005117808A1 (en) | 2004-05-17 | 2005-12-15 | 3M Innovative Properties Company | Acid-reactive dental fillers, compositions, and methods |
| US7026367B2 (en) | 2003-09-26 | 2006-04-11 | 3M Innovative Properties Company | Photoiniators having triarylsulfonium and arylsulfinate ions |
| US7030169B2 (en) | 2003-09-26 | 2006-04-18 | 3M Innovative Properties Company | Arylsulfinate salts in initiator systems for polymeric reactions |
| US7090721B2 (en) | 2004-05-17 | 2006-08-15 | 3M Innovative Properties Company | Use of nanoparticles to adjust refractive index of dental compositions |
| US7156911B2 (en) | 2004-05-17 | 2007-01-02 | 3M Innovative Properties Company | Dental compositions containing nanofillers and related methods |
| WO2007017152A2 (en) | 2005-08-05 | 2007-02-15 | 3M Espe Ag | Dental compositions containing a surface-modified filler |
| US7250452B2 (en) | 2003-09-26 | 2007-07-31 | 3M Innovative Properties Company | Dental compositions and methods with arylsulfinate salts |
| WO2008033911A2 (en) | 2006-09-13 | 2008-03-20 | 3M Innovative Properties Company | Dental compositions including organogelators, products, and methods |
| WO2009045752A2 (en) | 2007-10-01 | 2009-04-09 | 3M Innovative Properties Company | Orthodontic composition with polymeric fillers |
| US7576144B2 (en) | 2004-07-14 | 2009-08-18 | 3M Innovative Properties Company | Dental compositions containing carbosilane monomers |
| US7649029B2 (en) | 2004-05-17 | 2010-01-19 | 3M Innovative Properties Company | Dental compositions containing nanozirconia fillers |
| US7699605B2 (en) | 2003-08-12 | 2010-04-20 | 3M Espe Ag | Self-etching emulsion dental compositions and methods |
| EP2239275A1 (de) | 2006-05-31 | 2010-10-13 | 3M Innovative Properties Company | Polymerisierbare Zusammensetzungen enthaltend Salze aus Barbitursäure-Derivaten |
| EP2260828A2 (de) | 2004-11-16 | 2010-12-15 | 3M Innovative Properties Co. | Dentalfüllstoffe, Verfahren, Zusammensetzungen mit einem Caseinat |
| US8071662B2 (en) | 2005-12-29 | 2011-12-06 | 3M Innovative Properties Company | Dental compositions with surface-treated filler for shelf stability |
| US8076389B2 (en) | 2006-12-28 | 2011-12-13 | 3M Innovative Properties Company | Adhesive composition for hard tissue |
| US8084515B2 (en) | 2004-07-14 | 2011-12-27 | 3M Innovative Properties Company | Dental compositions containing carbosilane polymers |
| EP2401997A2 (de) | 2004-11-16 | 2012-01-04 | 3M Innovative Properties Company | Dentale Zusammensetzungen mit Calzium und Phosphor-freisetzendem Glas |
| EP2407142A1 (de) | 2002-12-30 | 2012-01-18 | 3M Innovative Properties Company | Verwendung von polymerisierbare Bisphosphonsäuren zur Behandlung von Zahnoberflächen die nicht mit Phosphorsäure vorbehandelt sind |
| WO2012021442A1 (en) | 2010-08-11 | 2012-02-16 | 3M Innovative Properties Company | Coated dental crows and method of making the same |
| WO2012021438A1 (en) | 2010-08-11 | 2012-02-16 | 3M Innovative Properties Company | Aesthetic and abrasion resistant coated dental articles and methods of making the same |
| WO2012021434A2 (en) | 2010-08-11 | 2012-02-16 | 3M Innovative Properties Company | Polymer coated dental articles and method of making the same |
| US8207238B2 (en) | 2007-11-01 | 2012-06-26 | 3M Innovative Properties Company | Dental compositions and initiator systems with color-stable amine electron donors |
| WO2012091902A1 (en) | 2010-12-30 | 2012-07-05 | 3M Innovative Properties Company | Bondable dental assemblies and methods including a compressible material |
| US8263681B2 (en) | 2006-12-28 | 2012-09-11 | 3M Innovative Properties Company | Dental compositions with natural tooth fluorescence |
| WO2012129143A1 (en) | 2011-03-24 | 2012-09-27 | 3M Innovative Properties Company | Dental adhesive comprising a coated polymeric component |
| US8465284B2 (en) | 2004-07-08 | 2013-06-18 | 3M Innovative Properties Company | Dental methods, compositions, and kits including acid-sensitive dyes |
| US8710114B2 (en) | 2004-11-16 | 2014-04-29 | 3M Innovative Properties Company | Dental fillers including a phosphorus containing surface treatment, and compositions and methods thereof |
| US8722759B2 (en) | 2008-10-15 | 2014-05-13 | 3M Innovative Properties Company | Fillers and composite materials with zirconia and silica nanoparticles |
| US8722760B2 (en) | 2004-08-11 | 2014-05-13 | 3M Innovative Properties Company | Self-adhesive compositions including a plurality of acidic compounds |
| WO2014151650A1 (en) | 2013-03-19 | 2014-09-25 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| WO2014209680A2 (en) | 2013-06-28 | 2014-12-31 | 3M Innovative Properties Company | Acid-modified nanoparticles, dual part polymerizable compositions, and methods |
| WO2015051095A1 (en) | 2013-10-04 | 2015-04-09 | 3M Innovative Properties Company | Dental mill blank |
| US9205029B2 (en) | 2008-10-15 | 2015-12-08 | 3M Innovative Properties Company | Dental compositions with fluorescent pigment |
| WO2015200007A1 (en) | 2014-06-24 | 2015-12-30 | 3M Innovative Properties Company | Adhesive precursor composition, two-part adhesive kit, and method of making an adhesive composition |
| WO2016014218A1 (en) | 2014-07-22 | 2016-01-28 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| WO2016044151A1 (en) | 2014-09-16 | 2016-03-24 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| US9339352B2 (en) | 2007-12-13 | 2016-05-17 | 3M Innovative Properties Company | Orthodontic article having partially hardened composition and related method |
| WO2016105974A1 (en) | 2014-12-22 | 2016-06-30 | 3M Innovative Properties Company | Sterically hindered amine and oxyalkyl amine light stabilizers |
| WO2016105993A1 (en) | 2014-12-22 | 2016-06-30 | 3M Innovative Properties Company | Sterically hindered alkyl and oxyalkyl amine light stabilizers |
| WO2016140950A1 (en) | 2015-03-05 | 2016-09-09 | 3M Innovative Properties Company | Composite material having ceramic fibers |
| EP3108848A1 (de) | 2006-10-23 | 2016-12-28 | 3M Innovative Properties Company | Zahnmedizinische artikel, verfahren und kits mit einem komprimierbaren material |
| US9943465B2 (en) | 2006-12-13 | 2018-04-17 | 3M Innovative Properties Company | Methods of using a dental composition having an acidic component and a photobleachable dye |
| US10137061B2 (en) | 2004-11-16 | 2018-11-27 | 3M Innovative Properties Company | Dental fillers and compositions including phosphate salts |
| US10344169B2 (en) | 2014-09-30 | 2019-07-09 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| WO2021191773A1 (en) | 2020-03-25 | 2021-09-30 | 3M Innovative Properties Company | Dental appliance with graphic image |
| WO2022064292A1 (en) | 2020-09-25 | 2022-03-31 | 3M Innovative Properties Company | Photopolymerizable compositions and reaction products thereof |
| WO2022144843A1 (en) | 2020-12-30 | 2022-07-07 | 3M Innovative Properties Company | Bondable orthodontic assemblies and methods for bonding |
| WO2022162488A1 (en) | 2021-01-29 | 2022-08-04 | 3M Innovative Properties Company | Dental appliances from multilayer films having discrete structures covered by an ion permeable release layer |
| WO2022195364A1 (en) | 2021-03-17 | 2022-09-22 | 3M Innovative Properties Company | Polymerizable 4,4'-spirobi[chromane]-2,2'-diones and curable compositions including the same |
| WO2022263987A1 (en) | 2021-06-16 | 2022-12-22 | 3M Innovative Properties Company | Free-radically polymerizable copolymer, free-radically polymerizable composition containing the same, and polymerized reaction product therefrom |
| WO2023031719A1 (en) | 2021-09-01 | 2023-03-09 | 3M Innovative Properties Company | Free-radically polymerizable composition, method of polymerizing the same, and polymerized composition |
| WO2023073444A1 (en) | 2021-10-28 | 2023-05-04 | 3M Innovative Properties Company | Photopolymerizable composition, methods of bonding and sealing, and at least partially polymerized composition |
| WO2023111722A1 (en) | 2021-12-14 | 2023-06-22 | 3M Innovative Properties Company | Curable precursor of an adhesive composition |
Families Citing this family (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3516257A1 (de) * | 1985-05-07 | 1986-11-13 | Bayer Ag, 5090 Leverkusen | (meth)-acrylsaeureester und ihre verwendung |
| JPH0794364B2 (ja) * | 1988-04-28 | 1995-10-11 | 株式会社ニコン | 歯科用樹脂組成物 |
| DE4005231A1 (de) * | 1990-02-20 | 1991-08-22 | Bayer Ag | Dentalwerkstoffe |
| EP0762214A1 (de) | 1995-09-05 | 1997-03-12 | Agfa-Gevaert N.V. | Lichtempfindliches Element, das eine Bildaufbauschicht und eine photopolymerisierbare Schicht enthält |
| DE10126432A1 (de) * | 2001-05-31 | 2002-12-05 | Bayer Ag | Fluor enthaltende Bisphenole, deren Herstellung, deren Vor- und Zwischenprodukte sowie die Verwendung der Fluor enthaltenden Bisphenole |
| US20050203217A1 (en) * | 2002-04-30 | 2005-09-15 | Pomrink Gregory J. | Stabilizers for polymerizable biocompatible materials |
| JP4485117B2 (ja) * | 2002-06-27 | 2010-06-16 | 日東電工株式会社 | 保護剥離用フィルム |
| US7134875B2 (en) | 2002-06-28 | 2006-11-14 | 3M Innovative Properties Company | Processes for forming dental materials and device |
| US6773261B2 (en) | 2002-06-28 | 2004-08-10 | 3M Innovative Properties Company | Processes for forming dental materials |
| US20040122126A1 (en) * | 2002-12-20 | 2004-06-24 | Dong Wu | Free-radical initiator systems containing enzymes, compositions, and methods |
| DE10261241A1 (de) * | 2002-12-20 | 2004-07-15 | 3M Espe Ag | Dentalmaterial mit bakteriostatischen und/oder bakteriziden Substanzen |
| US20040120901A1 (en) * | 2002-12-20 | 2004-06-24 | Dong Wu | Dental compositions including enzymes and methods |
| US7064152B2 (en) * | 2003-09-26 | 2006-06-20 | 3M Innovative Properties Company | Arylsulfinate salts in photoinitiator systems for polymerization reactions |
| JP4617837B2 (ja) * | 2003-11-21 | 2011-01-26 | チッソ株式会社 | フッ化アルキレンを有する重合性を有する液晶性化合物およびその重合体 |
| US20060204452A1 (en) * | 2005-03-10 | 2006-09-14 | Velamakanni Bhaskar V | Antimicrobial film-forming dental compositions and methods |
| US20060205838A1 (en) * | 2005-03-10 | 2006-09-14 | Velamakanni Bhaskar V | Hardenable antimicrobial dental compositions and methods |
| CN101217927A (zh) | 2005-05-09 | 2008-07-09 | 3M创新有限公司 | 含有杂化单体的牙科组合物 |
| EP1787627A1 (de) * | 2005-11-17 | 2007-05-23 | 3M Innovative Properties Company | Antimikrobielles Zahnabdruckmaterial |
| US8026296B2 (en) | 2005-12-20 | 2011-09-27 | 3M Innovative Properties Company | Dental compositions including a thermally labile component, and the use thereof |
| US7896650B2 (en) * | 2005-12-20 | 2011-03-01 | 3M Innovative Properties Company | Dental compositions including radiation-to-heat converters, and the use thereof |
| US20070142498A1 (en) * | 2005-12-20 | 2007-06-21 | Brennan Joan V | Dental compositions including thermally responsive additives, and the use thereof |
| US7776940B2 (en) * | 2005-12-20 | 2010-08-17 | 3M Innovative Properties Company | Methods for reducing bond strengths, dental compositions, and the use thereof |
| WO2007079144A1 (en) * | 2005-12-29 | 2007-07-12 | 3M Innovative Properties Company | Dental compositions with a water scavenger |
| WO2007079070A1 (en) * | 2005-12-29 | 2007-07-12 | 3M Innovative Properties Company | Dental compositions and initiator systems with polycyclic aromatic component |
| US9539065B2 (en) | 2006-10-23 | 2017-01-10 | 3M Innovative Properties Company | Assemblies, methods, and kits including a compressible material |
| CN101529957B (zh) * | 2006-11-01 | 2012-07-04 | 富士通株式会社 | 无线通信装置和无线通信方法 |
| EP2114350A1 (de) * | 2006-12-28 | 2009-11-11 | 3M Innovative Properties Company | (meth)acryloyl-haltige stoffe, zusammensetzungen und verfahren |
| US8647426B2 (en) * | 2006-12-28 | 2014-02-11 | 3M Innovative Properties Company | Dental filler and methods |
| WO2009076491A2 (en) * | 2007-12-13 | 2009-06-18 | 3M Innovative Properties Company | Remineralizing compositions and methods |
| EP2133063A1 (de) * | 2008-06-10 | 2009-12-16 | 3M Innovative Properties Company | Initiatorsystem mit Biphenylen-Derivaten, Herstellungsverfahren und Verwendung dafür |
| CN102196799B (zh) * | 2008-09-04 | 2013-02-06 | 3M创新有限公司 | 含有联苯二(甲基)丙烯酸酯单体的牙科用组合物 |
| EP2341885A2 (de) * | 2008-09-30 | 2011-07-13 | 3M Innovative Properties Company | Kieferorthopädische zusammensetzung mit wärmemodifizierten mineralien |
| BRPI0914464A2 (pt) * | 2008-10-22 | 2015-10-27 | 3M Innovative Properties Co | "composição dentária endurecível, artigos dentários e monômero bifenil di(met)acrilato" |
| WO2010068359A1 (en) * | 2008-12-11 | 2010-06-17 | 3M Innovative Properties Company | Surface-treated calcium phosphate particles suitable for oral care and dental compositions |
| WO2011087832A1 (en) | 2009-12-22 | 2011-07-21 | 3M Innovative Properties Company | Dental compositions, mill blocks, and methods |
| WO2012027091A1 (en) | 2010-08-11 | 2012-03-01 | 3M Innovative Properties Company | Dental articles including a ceramic and microparticle coating and method of making the same |
| CN104870573A (zh) | 2012-12-20 | 2015-08-26 | 3M创新有限公司 | 三有机硼烷-氨基官能化纳米粒子、组合物和方法 |
| DE112014004558T5 (de) * | 2013-10-02 | 2016-06-23 | Daikin Industries, Ltd | Flour-haltige komplexe Verbindung und Produktionsverfahren für Flour-haltige organische Verbindung, das diese verwendet |
| WO2016105990A1 (en) | 2014-12-22 | 2016-06-30 | 3M Innovative Properties Company | Sterically hindered amine and oxyalkyl amine light stabilizers |
| US20170283444A1 (en) | 2014-12-22 | 2017-10-05 | 3M Innovative Properties Company | Sterically hindered amine and oxyalkyl amine light stabilizers |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2647890A1 (de) * | 1975-10-23 | 1977-05-05 | Toyo Ink Mfg Co | Haertbare ueberzugszusammensetzung |
-
1985
- 1985-05-07 DE DE19853516256 patent/DE3516256A1/de not_active Withdrawn
-
1986
- 1986-04-16 US US06/852,600 patent/US4665217A/en not_active Expired - Fee Related
- 1986-04-29 EP EP86105902A patent/EP0201031B1/de not_active Expired
- 1986-04-29 DE DE8686105902T patent/DE3664765D1/de not_active Expired
- 1986-05-02 JP JP61101221A patent/JPS61263947A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2647890A1 (de) * | 1975-10-23 | 1977-05-05 | Toyo Ink Mfg Co | Haertbare ueberzugszusammensetzung |
Cited By (72)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2407142A1 (de) | 2002-12-30 | 2012-01-18 | 3M Innovative Properties Company | Verwendung von polymerisierbare Bisphosphonsäuren zur Behandlung von Zahnoberflächen die nicht mit Phosphorsäure vorbehandelt sind |
| EP2279722A1 (de) | 2003-08-12 | 2011-02-02 | 3M Innovative Properties Company | Selbstätzende dentale Zusammensetzungen und Verfahren |
| US8029286B2 (en) | 2003-08-12 | 2011-10-04 | 3M Innovative Properties Company | Self-etching dental compositions and methods |
| US7699605B2 (en) | 2003-08-12 | 2010-04-20 | 3M Espe Ag | Self-etching emulsion dental compositions and methods |
| US7026367B2 (en) | 2003-09-26 | 2006-04-11 | 3M Innovative Properties Company | Photoiniators having triarylsulfonium and arylsulfinate ions |
| US7030169B2 (en) | 2003-09-26 | 2006-04-18 | 3M Innovative Properties Company | Arylsulfinate salts in initiator systems for polymeric reactions |
| US7465758B2 (en) | 2003-09-26 | 2008-12-16 | 3M Innovative Properties Company | Dental compositions and methods with arylsulfinate salts |
| US7250452B2 (en) | 2003-09-26 | 2007-07-31 | 3M Innovative Properties Company | Dental compositions and methods with arylsulfinate salts |
| WO2005117808A1 (en) | 2004-05-17 | 2005-12-15 | 3M Innovative Properties Company | Acid-reactive dental fillers, compositions, and methods |
| US7156911B2 (en) | 2004-05-17 | 2007-01-02 | 3M Innovative Properties Company | Dental compositions containing nanofillers and related methods |
| US7649029B2 (en) | 2004-05-17 | 2010-01-19 | 3M Innovative Properties Company | Dental compositions containing nanozirconia fillers |
| US7090722B2 (en) | 2004-05-17 | 2006-08-15 | 3M Innovative Properties Company | Acid-reactive dental fillers, compositions, and methods |
| US7090721B2 (en) | 2004-05-17 | 2006-08-15 | 3M Innovative Properties Company | Use of nanoparticles to adjust refractive index of dental compositions |
| US8465284B2 (en) | 2004-07-08 | 2013-06-18 | 3M Innovative Properties Company | Dental methods, compositions, and kits including acid-sensitive dyes |
| US7576144B2 (en) | 2004-07-14 | 2009-08-18 | 3M Innovative Properties Company | Dental compositions containing carbosilane monomers |
| US8084515B2 (en) | 2004-07-14 | 2011-12-27 | 3M Innovative Properties Company | Dental compositions containing carbosilane polymers |
| US8722760B2 (en) | 2004-08-11 | 2014-05-13 | 3M Innovative Properties Company | Self-adhesive compositions including a plurality of acidic compounds |
| EP2260828A2 (de) | 2004-11-16 | 2010-12-15 | 3M Innovative Properties Co. | Dentalfüllstoffe, Verfahren, Zusammensetzungen mit einem Caseinat |
| US8710114B2 (en) | 2004-11-16 | 2014-04-29 | 3M Innovative Properties Company | Dental fillers including a phosphorus containing surface treatment, and compositions and methods thereof |
| EP2401997A2 (de) | 2004-11-16 | 2012-01-04 | 3M Innovative Properties Company | Dentale Zusammensetzungen mit Calzium und Phosphor-freisetzendem Glas |
| US8957126B2 (en) | 2004-11-16 | 2015-02-17 | 3M Innovative Properties Company | Dental compositions with calcium phosphorus releasing glass |
| US10137061B2 (en) | 2004-11-16 | 2018-11-27 | 3M Innovative Properties Company | Dental fillers and compositions including phosphate salts |
| US8278368B2 (en) | 2004-11-16 | 2012-10-02 | 3M Innnovatve Properties Company | Dental fillers, methods, compositions including a caseinate |
| WO2007017152A2 (en) | 2005-08-05 | 2007-02-15 | 3M Espe Ag | Dental compositions containing a surface-modified filler |
| US8071662B2 (en) | 2005-12-29 | 2011-12-06 | 3M Innovative Properties Company | Dental compositions with surface-treated filler for shelf stability |
| US8236871B2 (en) | 2006-05-31 | 2012-08-07 | 3M Innovative Properties Company | Polymerizable compositions containing salts of barbituric acid derivatives |
| EP2239275A1 (de) | 2006-05-31 | 2010-10-13 | 3M Innovative Properties Company | Polymerisierbare Zusammensetzungen enthaltend Salze aus Barbitursäure-Derivaten |
| US8552086B2 (en) | 2006-09-13 | 2013-10-08 | 3M Innovative Properties Company | Dental compositions including organogelators, products, and methods |
| EP2377507A2 (de) | 2006-09-13 | 2011-10-19 | 3M Innovative Properties Company | Dentalzusammensetzungen mit organischen Geliermitteln, Produkte und Verfahren |
| WO2008033911A2 (en) | 2006-09-13 | 2008-03-20 | 3M Innovative Properties Company | Dental compositions including organogelators, products, and methods |
| US8445558B2 (en) | 2006-09-13 | 2013-05-21 | 3M Innovative Properties Company | Dental compositions including organogelators, products, and methods |
| EP4056144A2 (de) | 2006-10-23 | 2022-09-14 | 3M Innovative Properties Company | Zahnmedizinische artikel, verfahren und kits mit einem komprimierbaren material |
| EP3669816A1 (de) | 2006-10-23 | 2020-06-24 | 3M Innovative Properties Company | Zahnmedizinische artikel, verfahren und kits mit einem komprimierbaren material |
| EP3108848A1 (de) | 2006-10-23 | 2016-12-28 | 3M Innovative Properties Company | Zahnmedizinische artikel, verfahren und kits mit einem komprimierbaren material |
| US9943465B2 (en) | 2006-12-13 | 2018-04-17 | 3M Innovative Properties Company | Methods of using a dental composition having an acidic component and a photobleachable dye |
| US8263681B2 (en) | 2006-12-28 | 2012-09-11 | 3M Innovative Properties Company | Dental compositions with natural tooth fluorescence |
| US8076389B2 (en) | 2006-12-28 | 2011-12-13 | 3M Innovative Properties Company | Adhesive composition for hard tissue |
| WO2009045752A2 (en) | 2007-10-01 | 2009-04-09 | 3M Innovative Properties Company | Orthodontic composition with polymeric fillers |
| EP2859876A2 (de) | 2007-11-01 | 2015-04-15 | 3M Innovative Properties Company | Dentale Zusammensetzungen und Initiator-Systeme mit farbstabilen Amin-Elektrondonatoren |
| US8207238B2 (en) | 2007-11-01 | 2012-06-26 | 3M Innovative Properties Company | Dental compositions and initiator systems with color-stable amine electron donors |
| US9339352B2 (en) | 2007-12-13 | 2016-05-17 | 3M Innovative Properties Company | Orthodontic article having partially hardened composition and related method |
| US8722759B2 (en) | 2008-10-15 | 2014-05-13 | 3M Innovative Properties Company | Fillers and composite materials with zirconia and silica nanoparticles |
| US9205029B2 (en) | 2008-10-15 | 2015-12-08 | 3M Innovative Properties Company | Dental compositions with fluorescent pigment |
| EP3243499A1 (de) | 2008-10-15 | 2017-11-15 | 3M Innovative Properties Co. | Dentale zusammensetzungen mit fluoreszierendem pigment |
| WO2012021442A1 (en) | 2010-08-11 | 2012-02-16 | 3M Innovative Properties Company | Coated dental crows and method of making the same |
| WO2012021438A1 (en) | 2010-08-11 | 2012-02-16 | 3M Innovative Properties Company | Aesthetic and abrasion resistant coated dental articles and methods of making the same |
| WO2012021434A2 (en) | 2010-08-11 | 2012-02-16 | 3M Innovative Properties Company | Polymer coated dental articles and method of making the same |
| EP3649980A1 (de) | 2010-12-30 | 2020-05-13 | 3M Innovative Properties Co. | Dentale bondingfähige anordnungen mit einem komprimierbaren material |
| WO2012091902A1 (en) | 2010-12-30 | 2012-07-05 | 3M Innovative Properties Company | Bondable dental assemblies and methods including a compressible material |
| WO2012129143A1 (en) | 2011-03-24 | 2012-09-27 | 3M Innovative Properties Company | Dental adhesive comprising a coated polymeric component |
| WO2014151650A1 (en) | 2013-03-19 | 2014-09-25 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| WO2014209680A2 (en) | 2013-06-28 | 2014-12-31 | 3M Innovative Properties Company | Acid-modified nanoparticles, dual part polymerizable compositions, and methods |
| WO2015051095A1 (en) | 2013-10-04 | 2015-04-09 | 3M Innovative Properties Company | Dental mill blank |
| WO2015200007A1 (en) | 2014-06-24 | 2015-12-30 | 3M Innovative Properties Company | Adhesive precursor composition, two-part adhesive kit, and method of making an adhesive composition |
| WO2016014218A1 (en) | 2014-07-22 | 2016-01-28 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| US10351642B2 (en) | 2014-07-22 | 2019-07-16 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| WO2016044151A1 (en) | 2014-09-16 | 2016-03-24 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| US10413935B2 (en) | 2014-09-16 | 2019-09-17 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| US10344169B2 (en) | 2014-09-30 | 2019-07-09 | 3M Innovative Properties Company | Free-radical polymerization methods and articles thereby |
| WO2016105993A1 (en) | 2014-12-22 | 2016-06-30 | 3M Innovative Properties Company | Sterically hindered alkyl and oxyalkyl amine light stabilizers |
| WO2016105974A1 (en) | 2014-12-22 | 2016-06-30 | 3M Innovative Properties Company | Sterically hindered amine and oxyalkyl amine light stabilizers |
| US10369086B2 (en) | 2015-03-05 | 2019-08-06 | 3M Innovative Properties Company | Composite material having ceramic fibers |
| WO2016140950A1 (en) | 2015-03-05 | 2016-09-09 | 3M Innovative Properties Company | Composite material having ceramic fibers |
| WO2021191773A1 (en) | 2020-03-25 | 2021-09-30 | 3M Innovative Properties Company | Dental appliance with graphic image |
| WO2022064292A1 (en) | 2020-09-25 | 2022-03-31 | 3M Innovative Properties Company | Photopolymerizable compositions and reaction products thereof |
| WO2022144843A1 (en) | 2020-12-30 | 2022-07-07 | 3M Innovative Properties Company | Bondable orthodontic assemblies and methods for bonding |
| WO2022162488A1 (en) | 2021-01-29 | 2022-08-04 | 3M Innovative Properties Company | Dental appliances from multilayer films having discrete structures covered by an ion permeable release layer |
| WO2022195364A1 (en) | 2021-03-17 | 2022-09-22 | 3M Innovative Properties Company | Polymerizable 4,4'-spirobi[chromane]-2,2'-diones and curable compositions including the same |
| WO2022263987A1 (en) | 2021-06-16 | 2022-12-22 | 3M Innovative Properties Company | Free-radically polymerizable copolymer, free-radically polymerizable composition containing the same, and polymerized reaction product therefrom |
| WO2023031719A1 (en) | 2021-09-01 | 2023-03-09 | 3M Innovative Properties Company | Free-radically polymerizable composition, method of polymerizing the same, and polymerized composition |
| WO2023073444A1 (en) | 2021-10-28 | 2023-05-04 | 3M Innovative Properties Company | Photopolymerizable composition, methods of bonding and sealing, and at least partially polymerized composition |
| WO2023111722A1 (en) | 2021-12-14 | 2023-06-22 | 3M Innovative Properties Company | Curable precursor of an adhesive composition |
Also Published As
| Publication number | Publication date |
|---|---|
| DE3516256A1 (de) | 1986-11-13 |
| EP0201031B1 (de) | 1989-08-02 |
| JPS61263947A (ja) | 1986-11-21 |
| EP0201031A3 (en) | 1988-06-01 |
| DE3664765D1 (en) | 1989-09-07 |
| US4665217A (en) | 1987-05-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0201031B1 (de) | (Meth)-Acrylsäureester und ihre Verwendung | |
| EP0209700B1 (de) | (Meth)-acrylsäure-Derivate von Tricyclodecanen und ihre Verwendung | |
| EP0201778B1 (de) | (Meth)-Acrylsäureester und ihre Verwendung | |
| EP0254185B1 (de) | Urethangruppen enthaltende (Meth)-acrylsäurederivate von Tricyclo [5.2.1.02.6]decanen | |
| EP0206074B1 (de) | (Meth)-acrylsäureester und ihre Verwendung | |
| EP0254950B1 (de) | (Meth)-acrylsäureester | |
| EP0264551B1 (de) | Urethangruppen enthaltende (Meth)-acrylsäurederivate | |
| EP0693487B1 (de) | Di(meth)acrylate mit cyclischen Carbonatgruppen | |
| EP0779290A1 (de) | Urethan-(Meth)acrylate mit cyclischen Carbonatgruppen und deren Verwendung zur Herstellung von Dentalwerkstoffen oder lithographischen Druckplatten | |
| EP0073995A1 (de) | Photopolymerisierbare Massen, deren Verwendung für zahnärztliche Zwecke, sowie Verfahren zur Herstellung von Zahnersatzteilen, Zahnfüllungen und Überzügen | |
| EP0321841B1 (de) | Ester-Urethan-(Meth)-acrylsäurederivate | |
| DE102004061925A1 (de) | Selbstätzende Dentalmaterialien auf Basis von (Meth)acrylamidphosphaten | |
| EP0400383B1 (de) | Harnstoffgruppen enthaltende (Meth)-Acrylsäure-Derivate von Triisocyanaten und ihre Verwendung | |
| EP0443370B1 (de) | Dentalwerkstoffe | |
| EP0266589B1 (de) | (Meth)-Acrylsäure-Derivate von Triisocyanaten und ihre Verwendung | |
| EP0273245B1 (de) | (Meth)-Acrylsäure-Derivate von Triisocyanaten und ihre Verwendung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 19860429 |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): BE CH DE FR GB IT LI NL |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): BE CH DE FR GB IT LI NL |
|
| 17Q | First examination report despatched |
Effective date: 19890116 |
|
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): BE CH DE FR GB IT LI NL |
|
| GBT | Gb: translation of ep patent filed (gb section 77(6)(a)/1977) | ||
| ITF | It: translation for a ep patent filed |
Owner name: ING. C. GREGORJ S.P.A. |
|
| REF | Corresponds to: |
Ref document number: 3664765 Country of ref document: DE Date of ref document: 19890907 |
|
| ET | Fr: translation filed | ||
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |
|
| 26N | No opposition filed | ||
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: CH Payment date: 19910416 Year of fee payment: 6 |
|
| ITTA | It: last paid annual fee | ||
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: NL Payment date: 19910430 Year of fee payment: 6 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 19920325 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19920327 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: BE Payment date: 19920416 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GB Payment date: 19920421 Year of fee payment: 7 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: LI Effective date: 19920430 Ref country code: CH Effective date: 19920430 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Effective date: 19921101 |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee | ||
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Effective date: 19930429 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: BE Effective date: 19930430 |
|
| BERE | Be: lapsed |
Owner name: BAYER A.G. Effective date: 19930430 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Effective date: 19931229 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Effective date: 19940101 |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 19930429 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: IT Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES;WARNING: LAPSES OF ITALIAN PATENTS WITH EFFECTIVE DATE BEFORE 2007 MAY HAVE OCCURRED AT ANY TIME BEFORE 2007. THE CORRECT EFFECTIVE DATE MAY BE DIFFERENT FROM THE ONE RECORDED. Effective date: 20050429 |